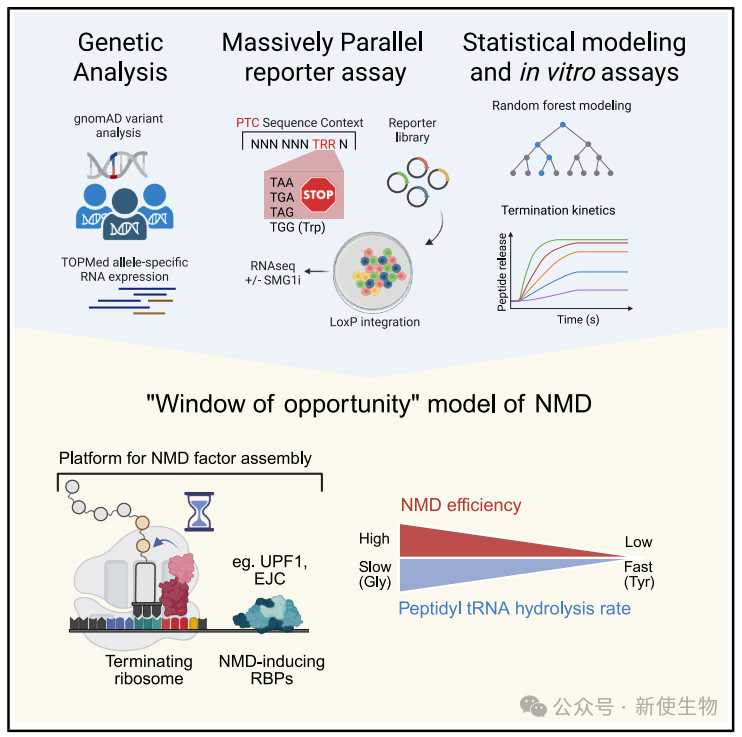
含有提前终止密码子的转录本在无义介导的mRNA降解(NMD)中的效率存在不可预测的差异。
最近的一项研究表明,终止密码子前的甘氨酸残基会延长翻译终止窗口,从而增强NMD活性。这一发现为NMD效率的变异性提供了新的机制解释,并有助于临床变异的更准确解读。
点击图片查看详细解读
2025年7月9日,爱丁堡大学遗传与癌症研究所Javier F.Cáceres团队针对这篇论文在Cell Genomics上发表了一篇题为“Stop codon context modulates NMD efficiency through translation termination kinetics”的点评文章。
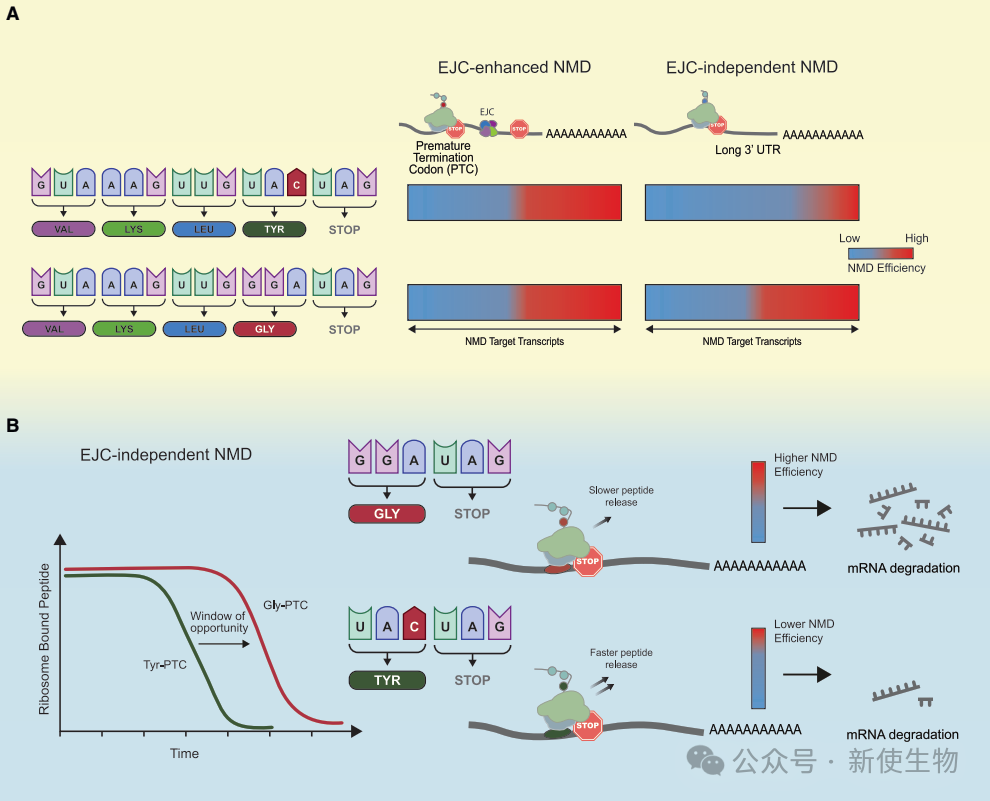
无义介导的mRNA降解(NMD)是一种转录后质量监控机制,能识别并降解含提前终止密码子(PTC)的mRNA,防止有害截短蛋白的产生。尽管NMD的核心因子已基本明确,但其如何区分正常终止与提前终止仍是未解之谜,因其活性与翻译终止的准确性和动力学密切相关。在哺乳动物中,终止密码子下游50–55个核苷酸处若残留外显子连接复合体(EJC),常作为NMD的重要激活信号。部分PTC转录本还可通过不依赖EJC的机制被降解,可能与外显子或3′ UTR长度相关,但这些路径尚不清楚。当前认为,PTC处终止效率低下是激活NMD的关键,受翻译装置、mRNA序列特征及终止增强因子(如PABC1)等多因素共同调控。然而,NMD效率在不同转录本、组织和个体间差异显著,仍缺乏可靠预测模型。目前对NMD是否被激活的预测准确率仅为50%–70%,这限制了对致病突变影响的判断。因此,深入理解影响NMD效率的机制,对于遗传病机制研究与靶向治疗开发具有重要意义。在本期的Cell Genomics中,Sujatha Jagannathan团队系统性研究发现,提前终止密码子(PTC)前的氨基酸类型显著影响NMD效率,其中甘氨酸(Gly)在PTC上游显著富集,提示序列背景可能调控NMD活性。通过TOPMed项目的数据分析和高通量报告系统验证,证实在非EJC依赖机制中,PTC前为甘氨酸可显著增强NMD活性,而EJC依赖型NMD对此不敏感。作者进一步结合机器学习,发现翻译终止时肽链释放速率是NMD效率的重要预测因子。体外实验表明甘氨酸对应的释放速率最慢,有利于NMD的启动,表明翻译终止动力学与NMD密切相关。该研究首次揭示局部序列与终止动力学共同决定NMD效率,为解释NMD变异性、精准解读致病突变及开发NMD调控疗法提供了新机制和方向,未来还需探索这些规律在不同生理和病理状态下的适用性。开创性的建库技术使得Ribo-seq核糖体印迹分析(QEZ-seq®)具有超高的分辨率,且适用于哺乳动物、植物、真菌等多类物种。
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com
点击图片查看
点击图片查看



 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们