导读
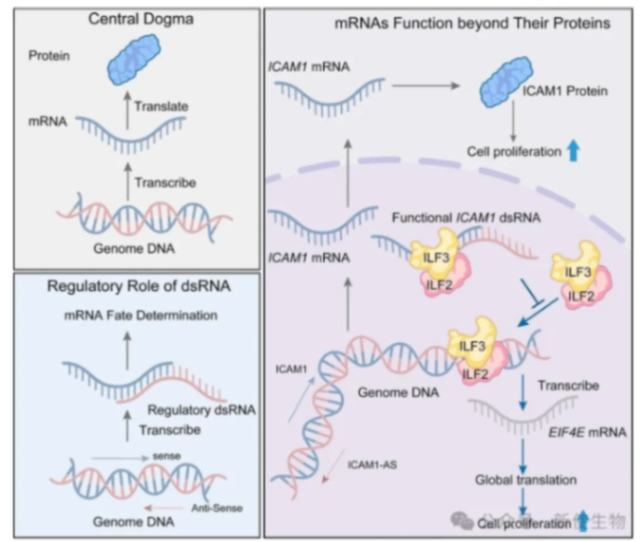
分子生物学的中心法则阐述了遗传信息从DNA流向mRNA再到蛋白质的过程,明确了mRNA作为蛋白质合成模板的核心地位。然而,非编码RNA的发现极大地丰富和挑战了我们对基因表达调控的传统认知。
尽管如此,我们对RNA分类和功能的理解仍存在显著空白。近年来研究发现,一些传统上被认为是编码蛋白的mRNA,在特定细胞或组织中也展现出非编码功能。
ICAM1作为一个经典的癌基因,被认为促进肿瘤进展,但也有报道称其在某些癌症中发挥抑癌作用,其双重角色的分子机制尚不清楚。因此,探究mRNA是否能在同一细胞中独立于其编码的蛋白质发挥功能,以及如何发挥功能,是当前RNA生物学领域一个重要且悬而未决的问题。
2026年1月22日,东南大学高山团队在Molecular Cell上发表了一篇题为“ICAM1 mRNA entraps ILF2/ILF3 to inhibit transcription of EIF4E and global protein synthesis”的论文。该研究发现ICAM1 mRNA作为一种非编码RNA,能够抑制细胞增殖,这与其编码蛋白促增殖的功能完全相反。

文章索引
【标题】ICAM1 mRNA entraps ILF2/ILF3 to inhibit transcription of EIF4E and global protein synthesis
【发表期刊】 Molecular Cell
【发表日期】 2026年1月22日
【作者及团队】东南大学高山团队
【IF】16.6
研究结果
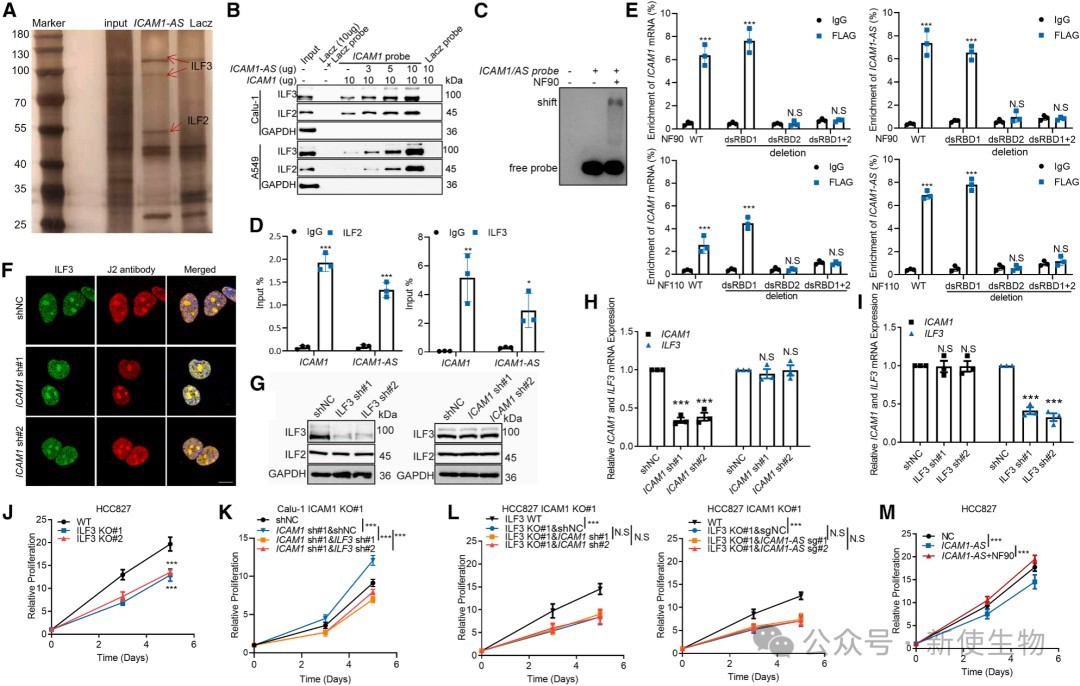
一、ICAM1的mRNA和蛋白功能相反,其mRNA独立发挥抑癌作用
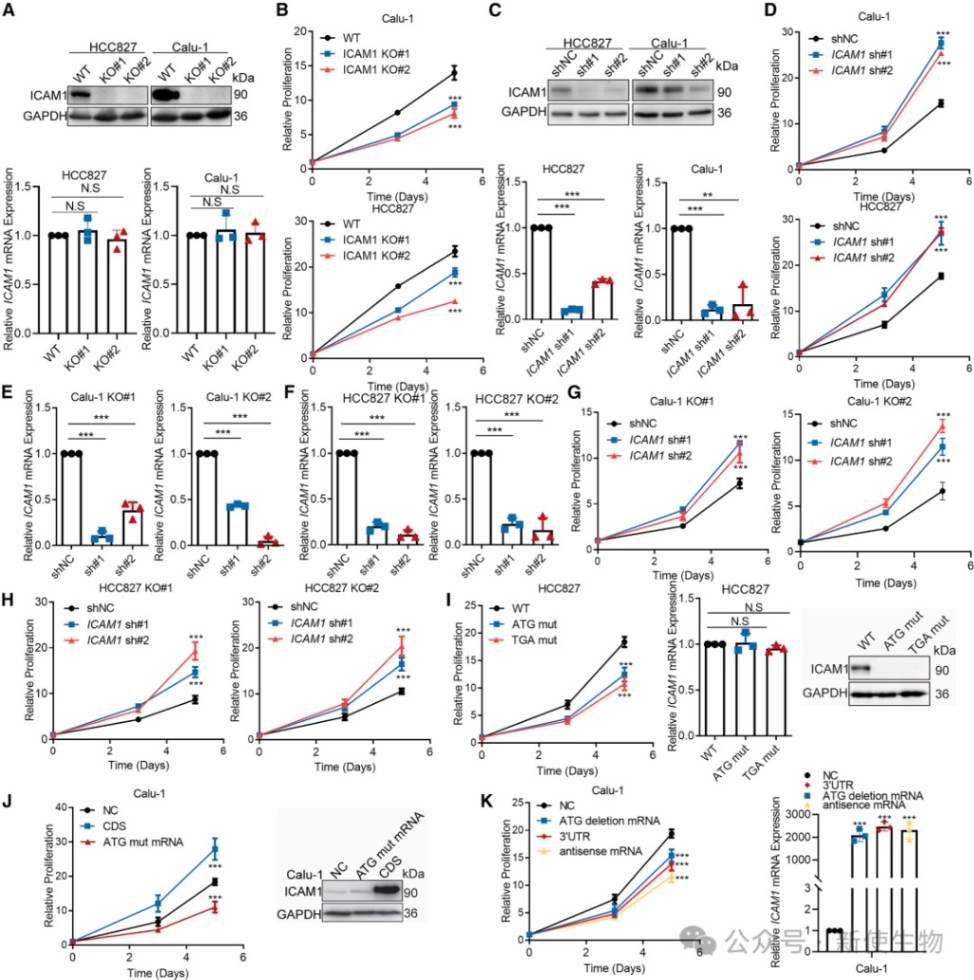
通过CRISPR-Cas9技术敲除(KO)ICAM1蛋白会抑制细胞增殖,而通过shRNA敲低(KD)ICAM1 mRNA则显著促进细胞增殖。
进一步在蛋白敲除的细胞中敲低其mRNA,同样观察到增殖加速,这直接证明了ICAM1 mRNA本身具有独立于其编码蛋白的抑制细胞增殖的功能。
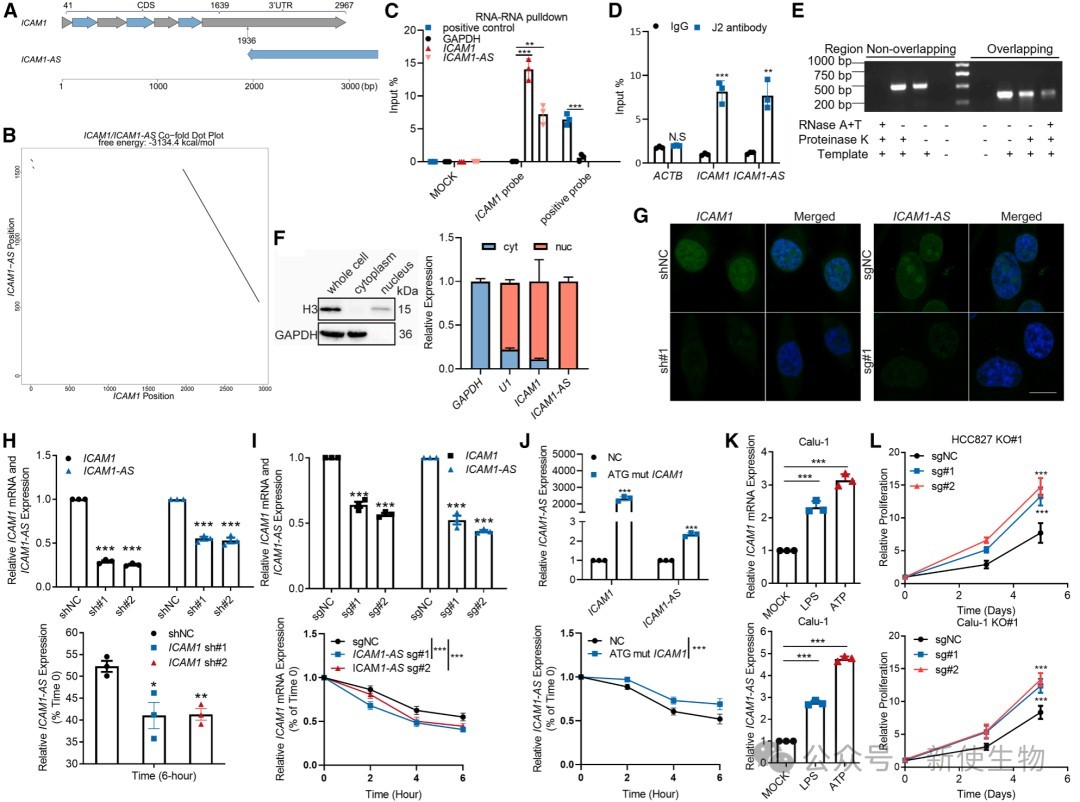
二、ICAM1 mRNA与反义转录本ICAM1-AS形成dsRNA发挥非编码功能
通过生物信息学分析、RNA pull-down和RNA免疫共沉淀(RIP)等实验证实,ICAM1 mRNA在细胞核内与其天然反义转录本ICAM1-AS通过3' UTR区域互补配对,形成稳定的双链RNA(dsRNA)结构。
二者在表达上相互稳定,并协同发挥抑制细胞增殖的功能。
三、ICAM1/ICAM1-AS dsRNA通过结合ILF2/ILF3复合物调控细胞增殖
利用RNA pull-down结合质谱分析,发现ICAM1/ICAM1-AS dsRNA能够特异性结合dsRNA结合蛋白复合物ILF2/ILF3。
功能实验表明,ICAM1/ICAM1-AS对细胞增殖的抑制作用依赖于ILF3,证明该dsRNA通过捕获ILF2/ILF3来发挥其生物学功能。
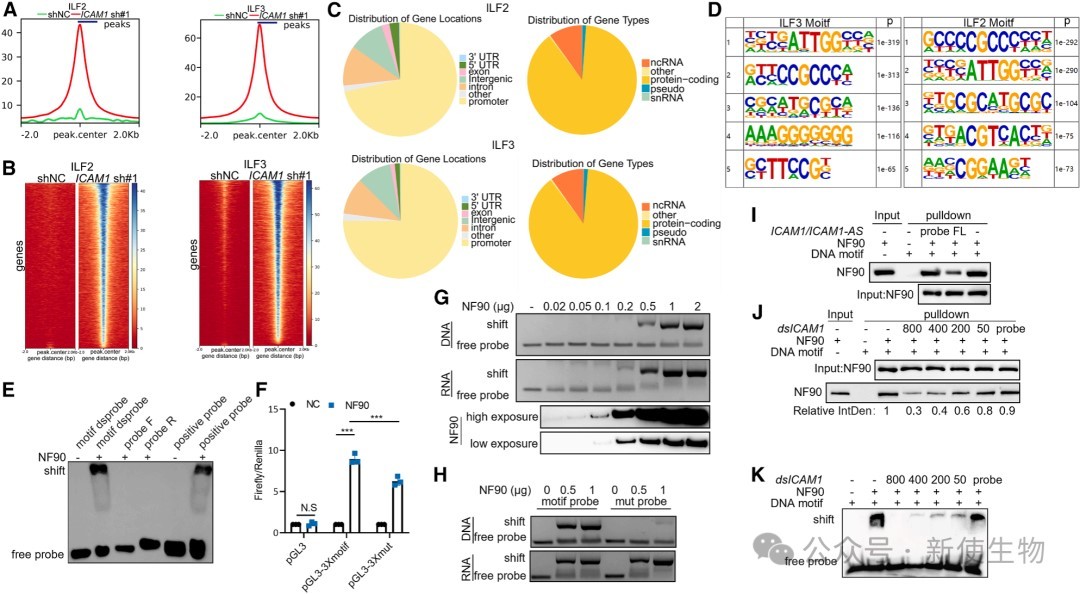
四、ICAM1/ICAM1-AS dsRNA竞争性抑制ILF2/ILF3的DNA结合能力
通过CUT&Tag和EMSA等实验发现,ICAM1/ICAM1-AS dsRNA的存在显著抑制了转录因子ILF2/ILF3与全基因组DNA(特别是启动子区域)的结合。
这种抑制效应具有长度依赖性,长的ICAM1/ICAM1-AS dsRNA比短dsRNA的竞争抑制能力更强。
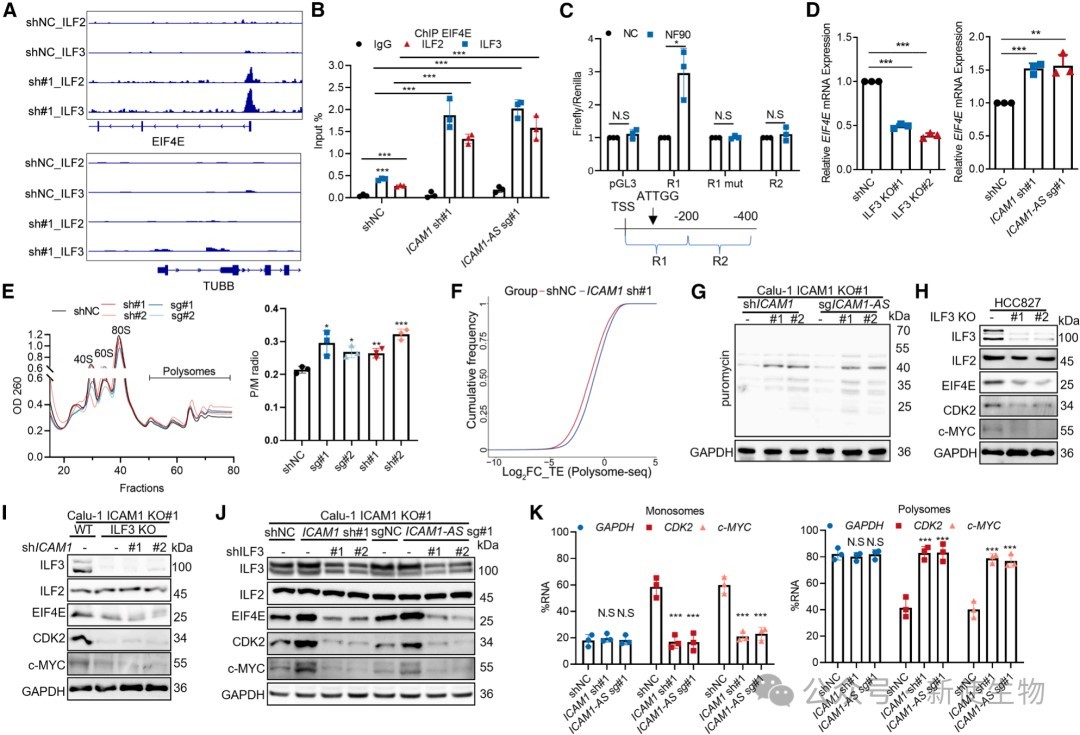
五、ICAM1/ICAM1-AS通过ILF2/ILF3-EIF4E轴抑制全局翻译
综合CUT&Tag和转录组学分析发现,ILF2/ILF3是翻译起始因子EIF4E的转录激活因子。
ICAM1/ICAM1-AS dsRNA通过诱捕ILF2/ILF3,解除了其对EIF4E启动子的结合与激活,从而下调EIF4E表达。
Polysome profiling多聚核糖体分析结合转录组测序和蛋白新生合成实验证实,这最终导致了全局蛋白质合成水平的降低和细胞增殖的抑制。
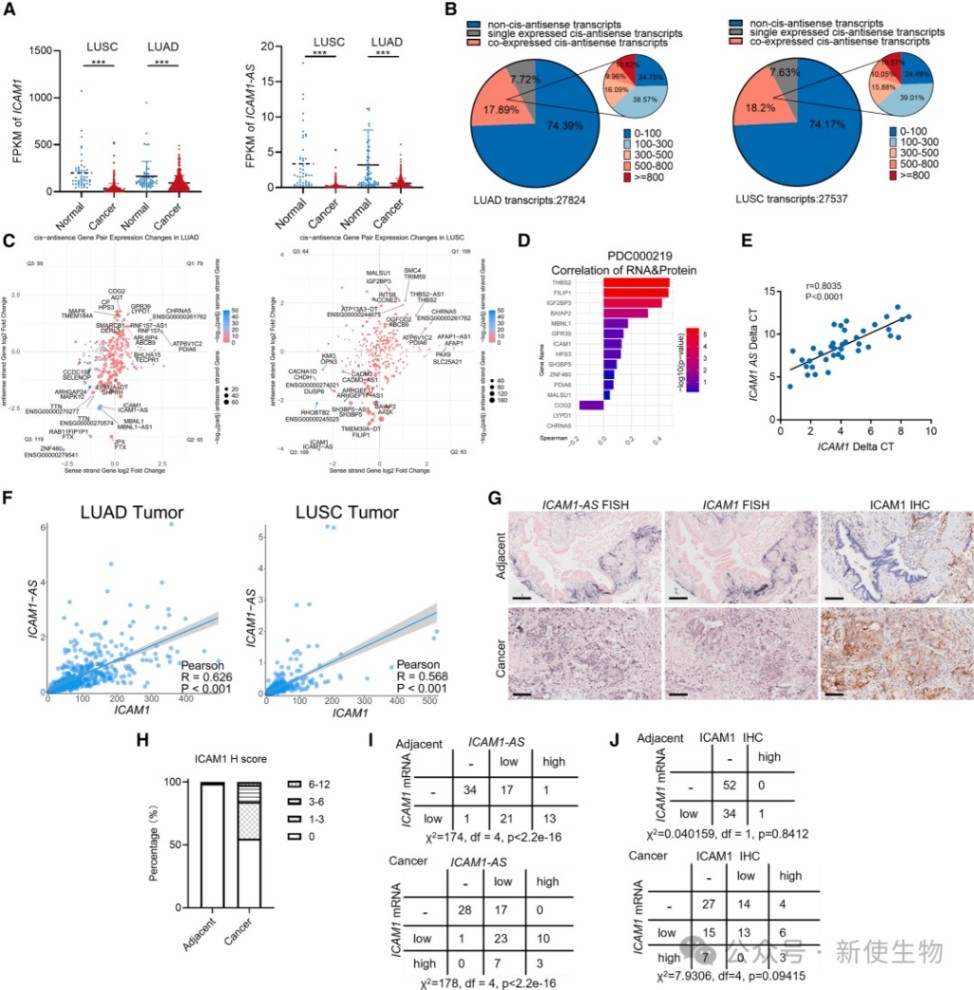
六、ICAM1/ICAM1-AS在肺癌中协同下调且独立于其蛋白表达
对TCGA数据库和临床样本的分析显示,在肺癌组织中,ICAM1 mRNA和ICAM1-AS的表达水平显著协同下调,而ICAM1蛋白的表达水平却异常升高,且mRNA与蛋白水平之间无显著相关性。
这揭示了ICAM1/ICAM1-AS-ILF2/ILF3调控轴在肺癌发生发展中的复杂作用和重要的临床指示意义。
总结
总之,本研究揭示了ICAM1 mRNA通过与其反义链形成dsRNA来隔离转录因子ILF2/ILF3,进而调控下游基因转录和全局翻译的全新分子机制。该发现不仅揭示了mRNA独立于其编码产物的非经典功能,也为理解基因功能、解读RNAi与CRISPR实验结果的差异性提供了新的视角。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们