导读
真核细胞内蛋白质的精确合成、折叠、组装等生命过程对维持细胞稳态至关重要。许多关键的蛋白质成熟过程在翻译的同时发生,即共翻译过程。
这些过程需要一系列共翻译因子与核糖体上新生的多肽链(nascent chains, NCs)进行动态、瞬时的相互作用。然而,由于这些相互作用的瞬时性,系统性地鉴定这些共翻译因子极具挑战性。
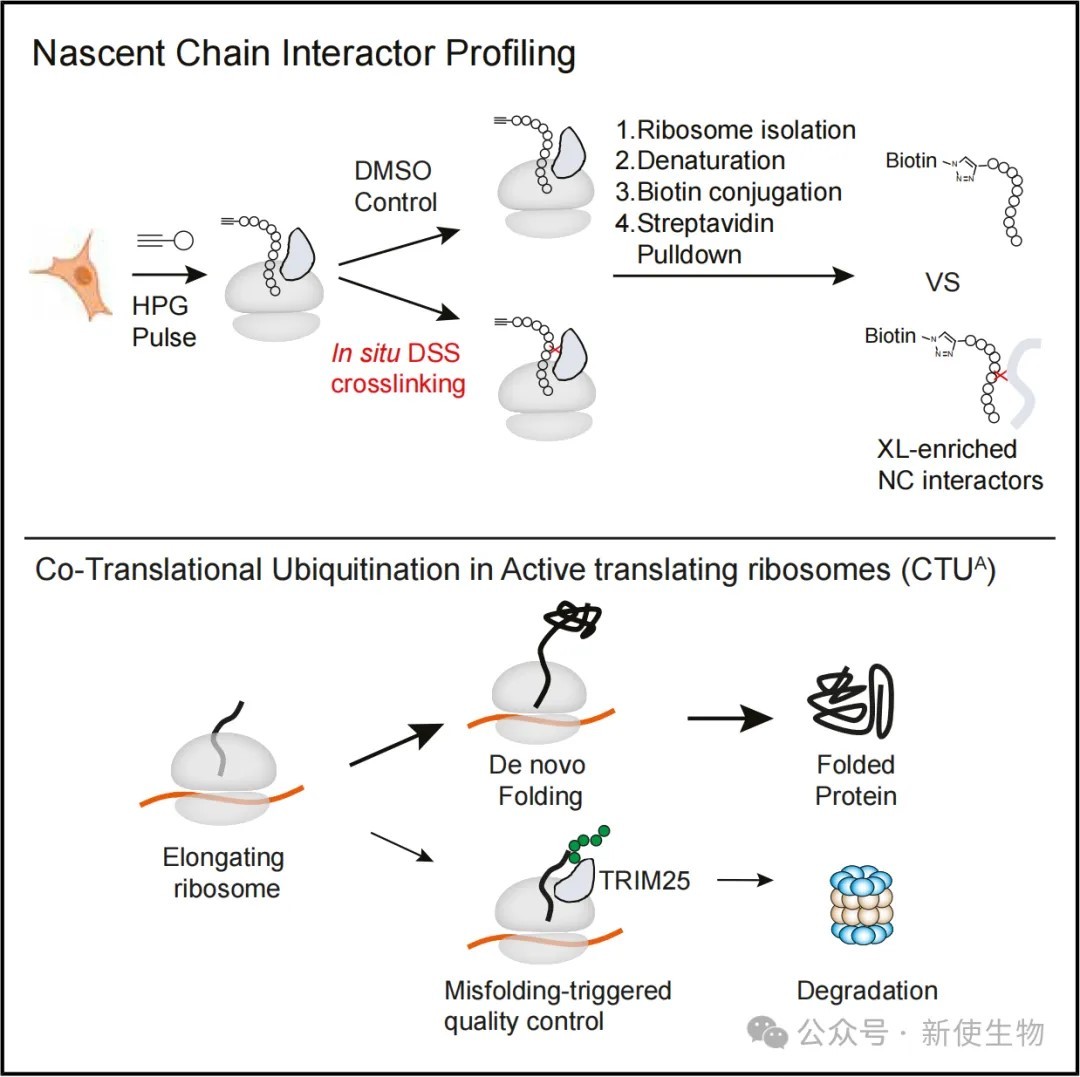
一个重要的共翻译质量控制途径是新生链的泛素化(CTUA),它能标记错误折叠的新生链以便降解。尽管CTUA途径非常重要,但在哺乳动物细胞中负责该过程的关键E3泛素连接酶仍不清楚,这阻碍了对其分子机制的深入理解。
2026年3月9日,新加坡国立大学的林哲望团队在Molecular Cell上发表了一篇题为“Global profiling of nascent chain interactors reveals TRIM25 as a co-translational E3 ubiquitin ligase”的论文。该研究开发了一种名为NCIP的创新蛋白质组学技术,首次在全蛋白质组范围内系统性地绘制了与新生肽链相互作用的蛋白图谱。

文章索引
【标题】 Global profiling of nascent chain interactors reveals TRIM25 as a co-translational E3 ubiquitin ligase
【发表期刊】 Molecular Cell
【发表日期】 2026年3月9日
【作者及团队】新加坡国立大学林哲望团队
【IF】 16.6
研究结果
一、NCIP方法能够特异性捕获并富集新生肽链的相互作用蛋白
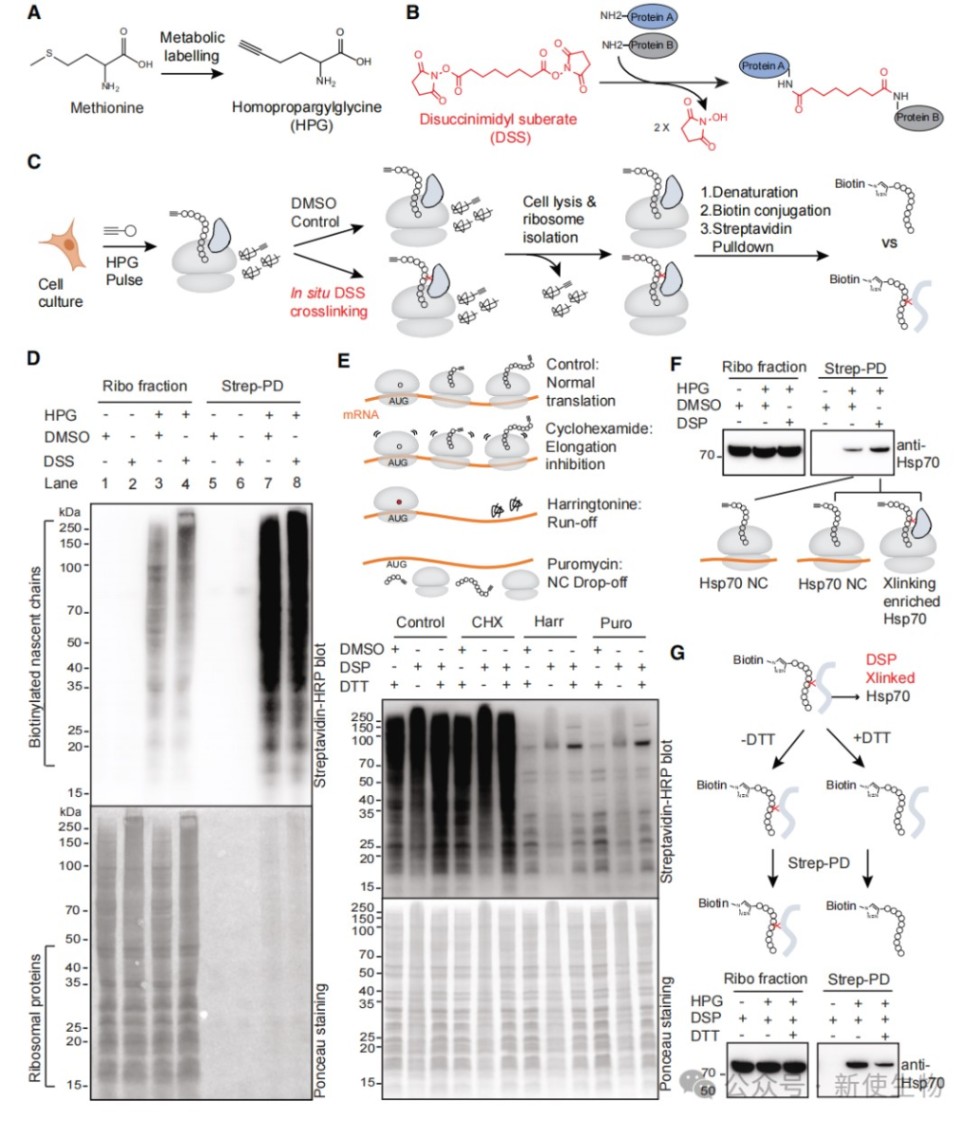
研究人员结合了非天然氨基酸标记(HPG)和化学交联技术,开发了NCIP(nascent-chain interactor profiling)方法来捕获新生链的相互作用蛋白。
实验证明,该方法能有效捕获新生肽链及其互作蛋白,并通过对已知共翻译伴侣Hsp70的验证,证实了其可靠性。
二、NCIP揭示了广泛的共翻译新生链相互作用蛋白
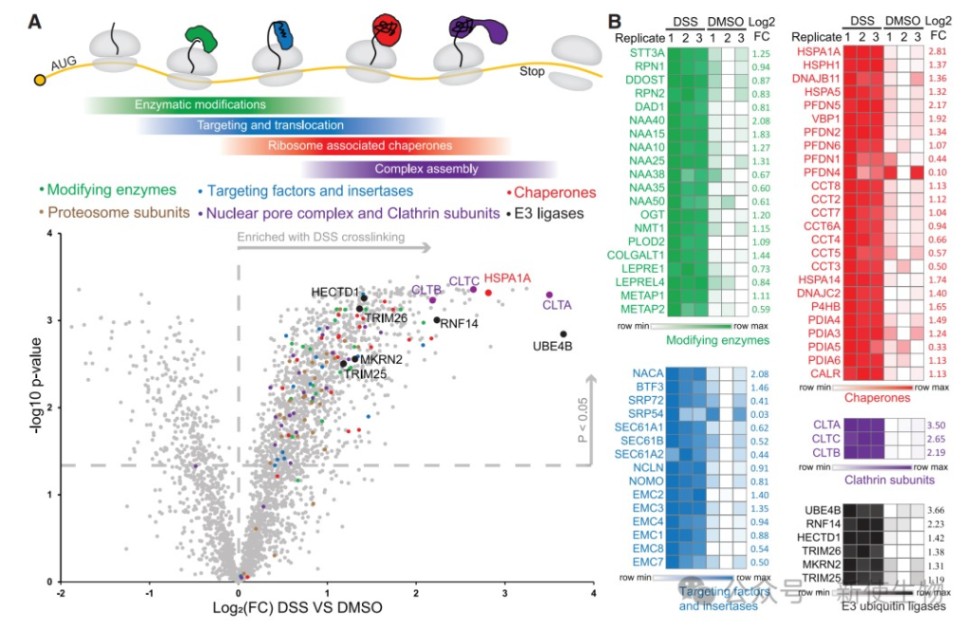
通过对293T细胞进行NCIP和定量蛋白质组学分析,研究人员鉴定出大量在交联后显著富集的蛋白。
这些蛋白包括了几乎所有已知的共翻译因子,如分子伴侣、蛋白靶向与转运因子、以及修饰酶等,证明了NCIP方法在系统性发现新生链相互作用物方面的强大能力。
三、NCIP数据支持多种蛋白质复合物的共翻译组装模型
NCIP分析发现多个蛋白质复合物的亚基被显著富集,提示它们可能通过共翻译途径进行组装。
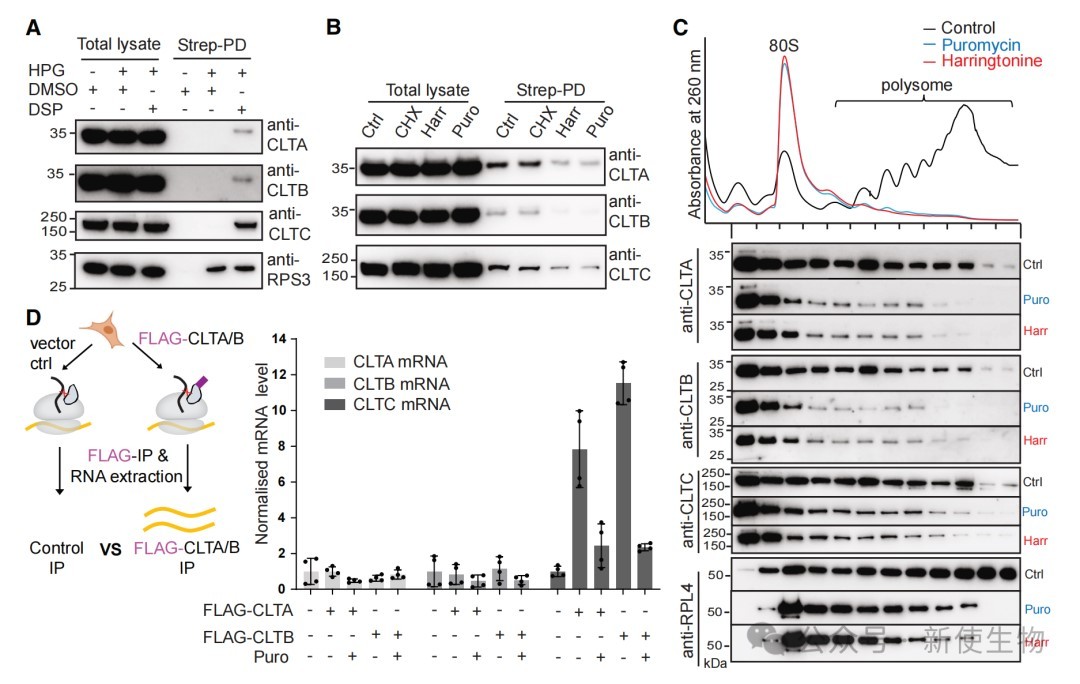
研究人员以新发现的网格蛋白(clathrin)复合物为例,通过免疫共沉淀偶联qPCR(RIP-qPCR)和Polysome profiling多聚核糖体分析等实验,证实成熟的网格蛋白亚基会与正在翻译的新生网格蛋白亚基相互作用,为该复合物的共翻译组装提供了直接证据。
四、NCIP鉴定出TRIM25是负责CTUA的主要E3泛素连接酶
NCIP数据鉴定出多个E3泛素连接酶是潜在的新生链相互作用蛋白。
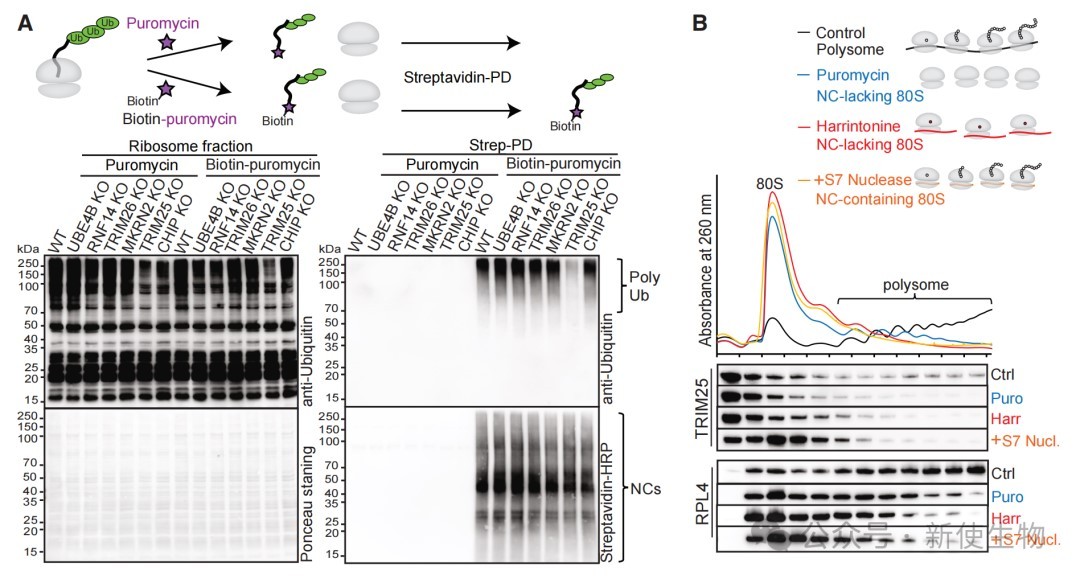
通过对候选E3连接酶进行CRISPR-Cas9基因敲除筛选,研究发现敲除TRIM25能够显著降低新生链的泛素化水平。
五、TRIM25通过泛素化错误折叠的新生链来维持蛋白质稳态
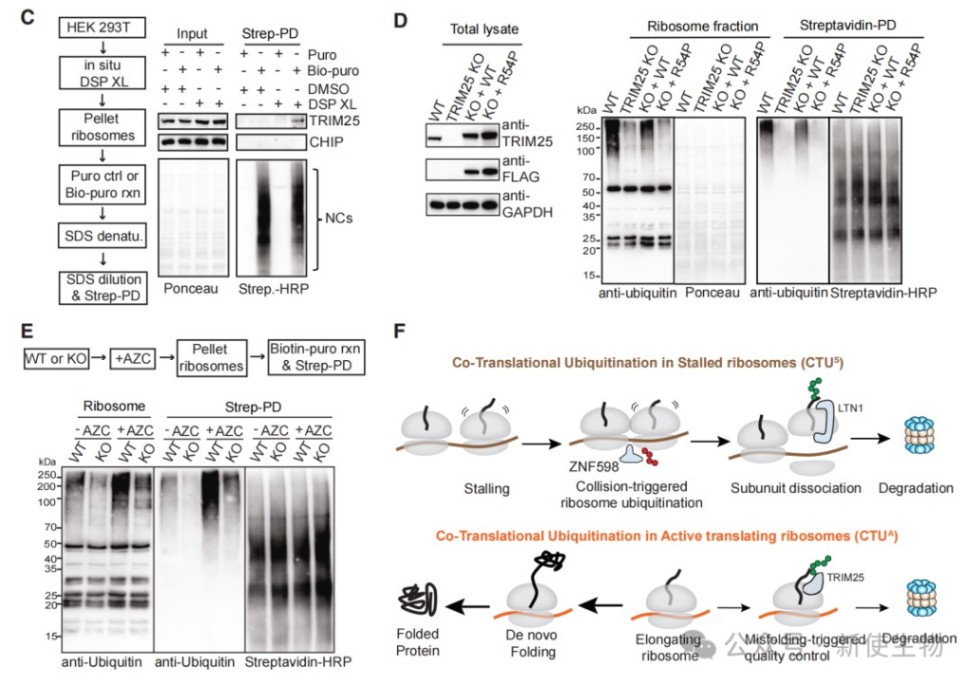
研究发现,使用药物诱导蛋白质错误折叠会显著增加新生链的泛素化,而这一过程严重依赖于TRIM25。
在TRIM25敲除的细胞中,错误折叠蛋白和不可溶蛋白聚集物的水平显著升高,表明TRIM25介导的CTUA是清除错误折叠蛋白、维持细胞蛋白质稳态的重要质量控制途径。
总结
本文通过开发一种名为NCIP的创新蛋白质组学技术,成功绘制了新生多肽链的共翻译相互作用图谱。该研究不仅证实了多种蛋白质复合物的共翻译组装模型,更重要的是鉴定出TRIM25是哺乳动物细胞中调控新生链质量控制(CTUA)的关键E3泛素连接酶,为理解细胞如何维持蛋白质稳态提供了新的分子机制。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们