导读
肺腺癌(LUAD)作为非小细胞肺癌中最常见的亚型,是全球癌症相关死亡的主要原因。尽管在靶向治疗和免疫治疗方面取得了进展,但许多患者最终会对一线治疗(如EGFR靶向药物)产生耐药性。
近年来,基因组中大量未被探索的遗传物质,包括长链非编码RNA(lncRNA)、微小RNA(miRNA)和环状RNA(circRNA),在人类疾病中的作用日益受到关注。除了非编码RNA,由隐蔽开放阅读框翻译而成的非经典蛋白质在癌症生物学中也发挥着重要作用。
circRNA因其稳定的环状结构而备受瞩目,其编码的蛋白质已被证实参与了肿瘤的发生发展及耐药机制。因此,深入研究这些非经典蛋白质的功能,对于揭示肿瘤进展机制并发现潜在的治疗靶点具有重要意义。
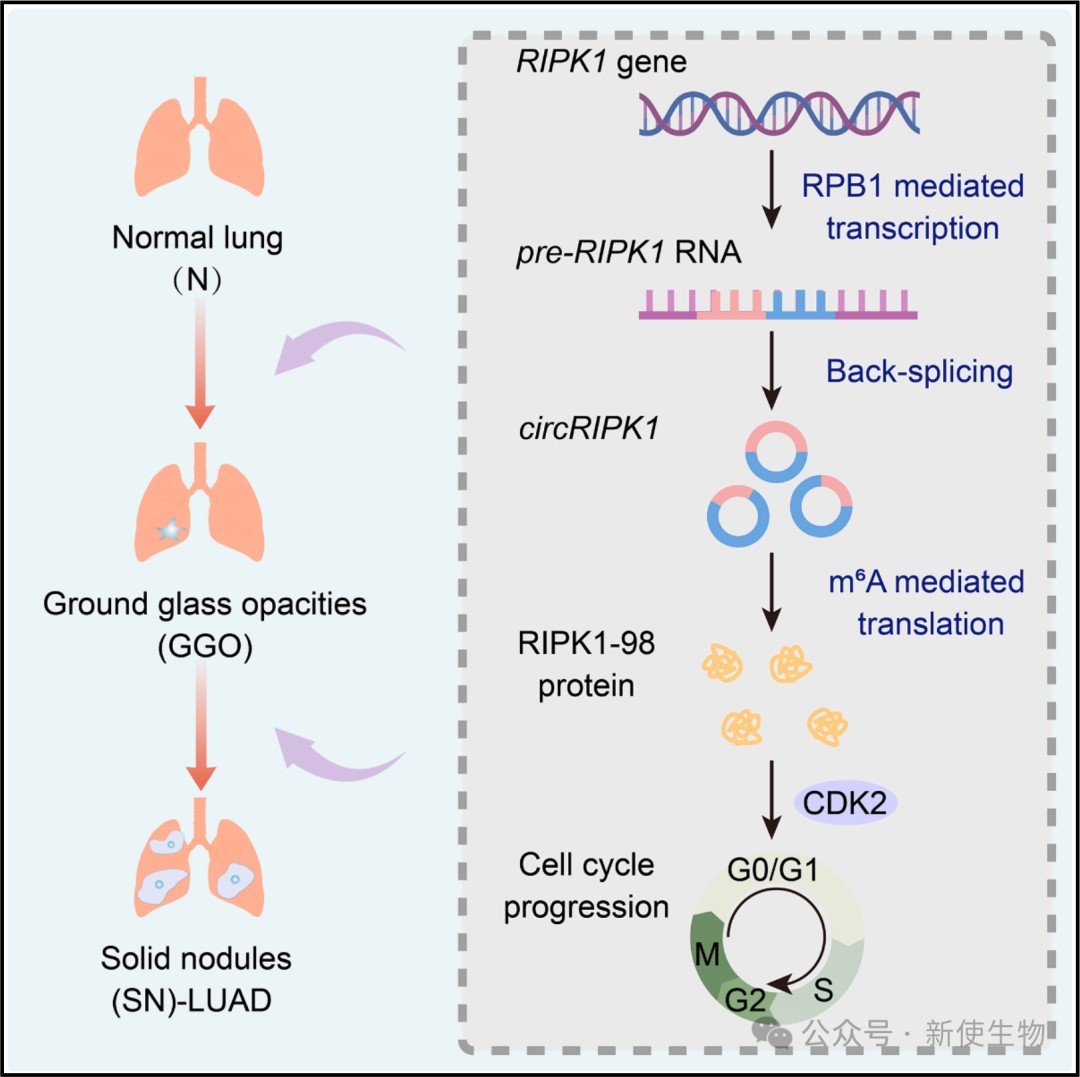
2026年3月19日,上海交通大学王佳谊、德克萨斯大学唐道林和上海交通大学石毅团队合作,在Developmental Cell上发表了一篇题为“CircRNA-encoded RIPK1-98 protein drives lung adenocarcinoma progression”的论文。该研究通过多组学方法在肺腺癌中鉴定出一系列由环状RNA编码的新型蛋白(cUEP),并发现其丰度随肿瘤恶化而显著增加。

文章索引
【标题】 CircRNA-encoded RIPK1-98 protein drives lung adenocarcinoma progression
【发表期刊】 Developmental Cell
【发表日期】 2026年3月19日
【作者及团队】上海交通大学王佳谊、德克萨斯大学唐道林和上海交通大学石毅团队
【IF】 8.7
研究结果
一、肺腺癌进展伴随着未知蛋白和circRNA的表达上调
研究人员通过蛋白质谱分析和环状RNA测序,在不同阶段肺腺癌样本中筛选出大量先前未知的蛋白质及其来源circRNA。
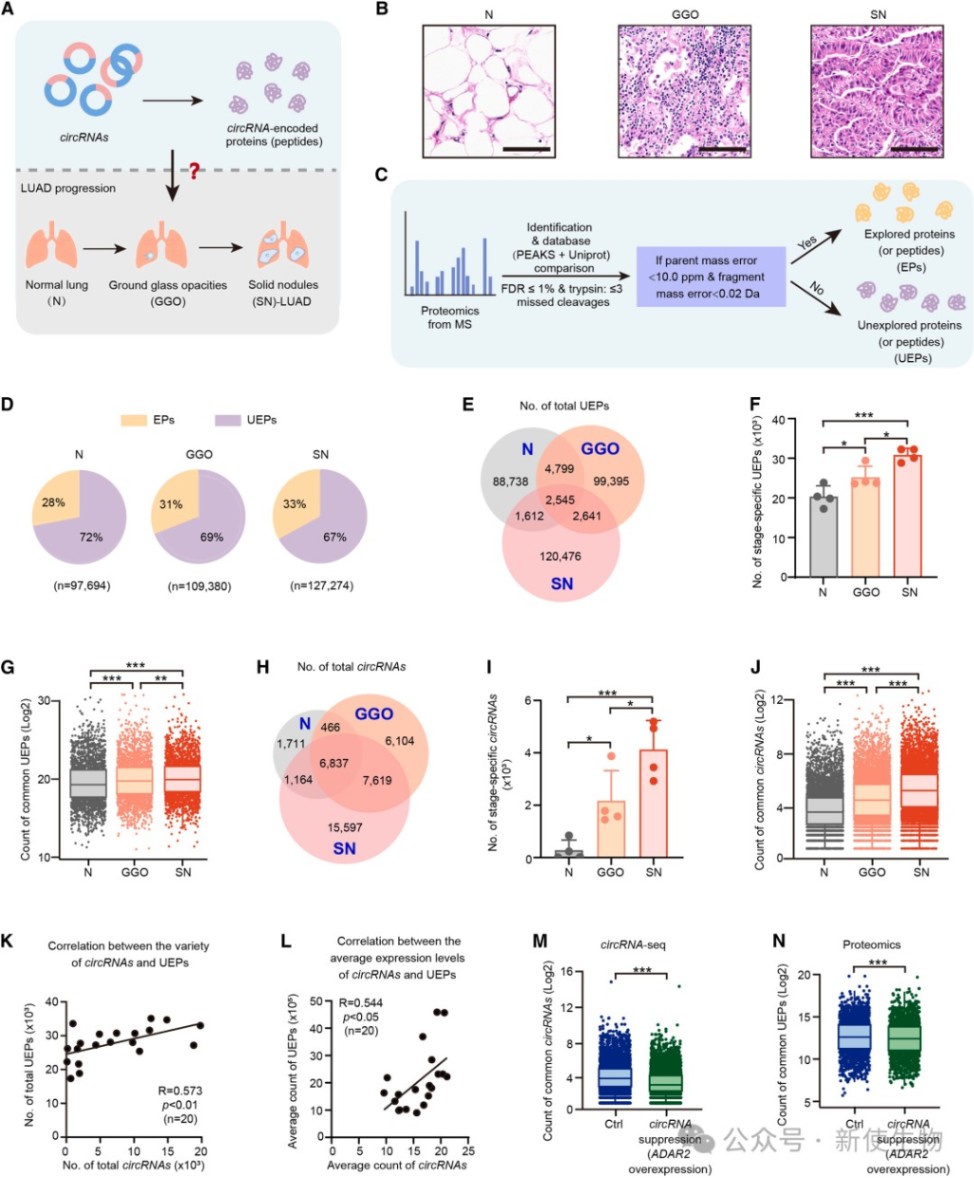
通过整合Polysome profiling多聚核糖体分析及质谱数据,作者证实了这些cUEP由circ-cUEP翻译而来,且其多样性和表达水平随肺腺癌进展而显著升高。
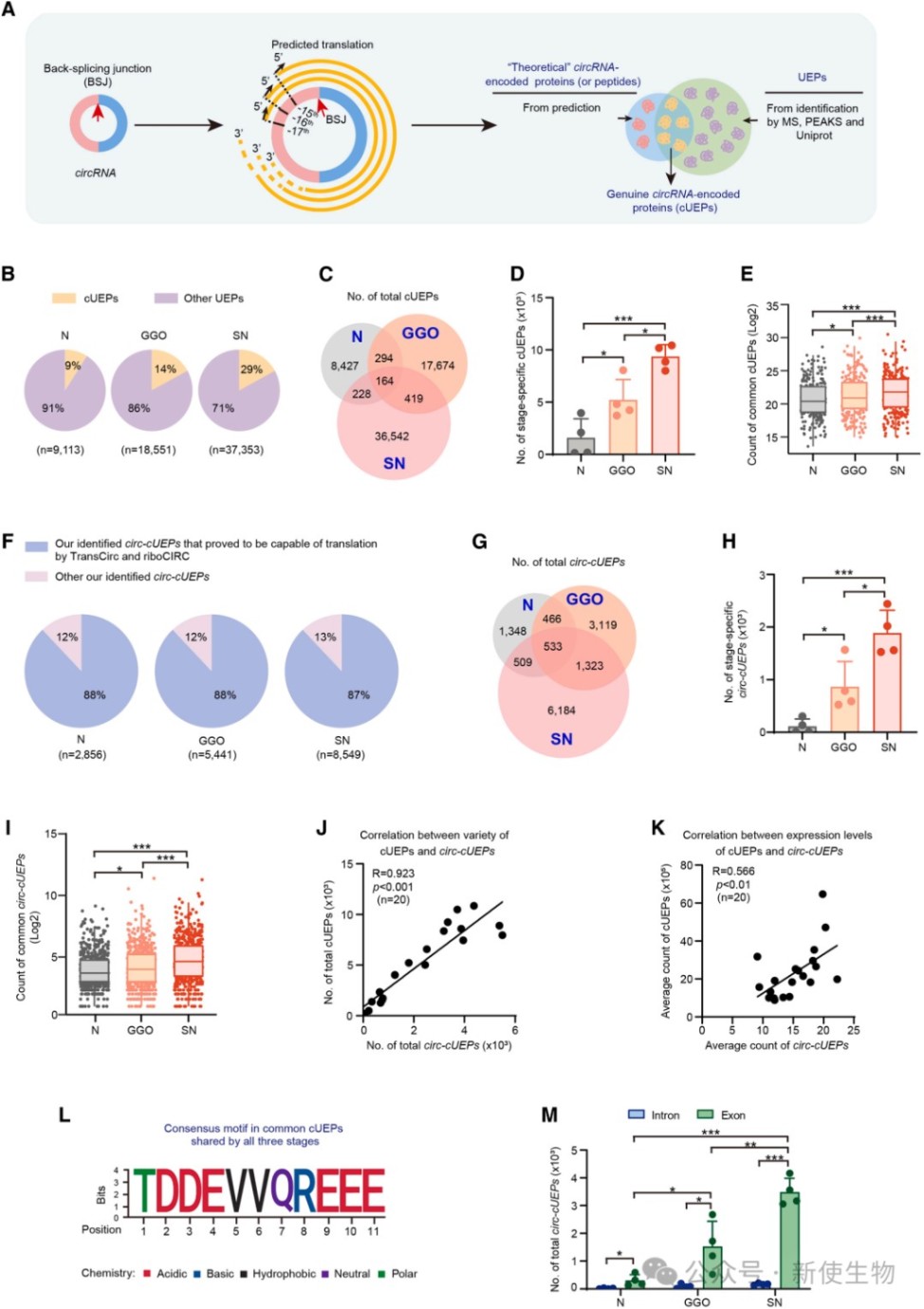
二、RPB1驱动的转录是cUEPs上调的关键
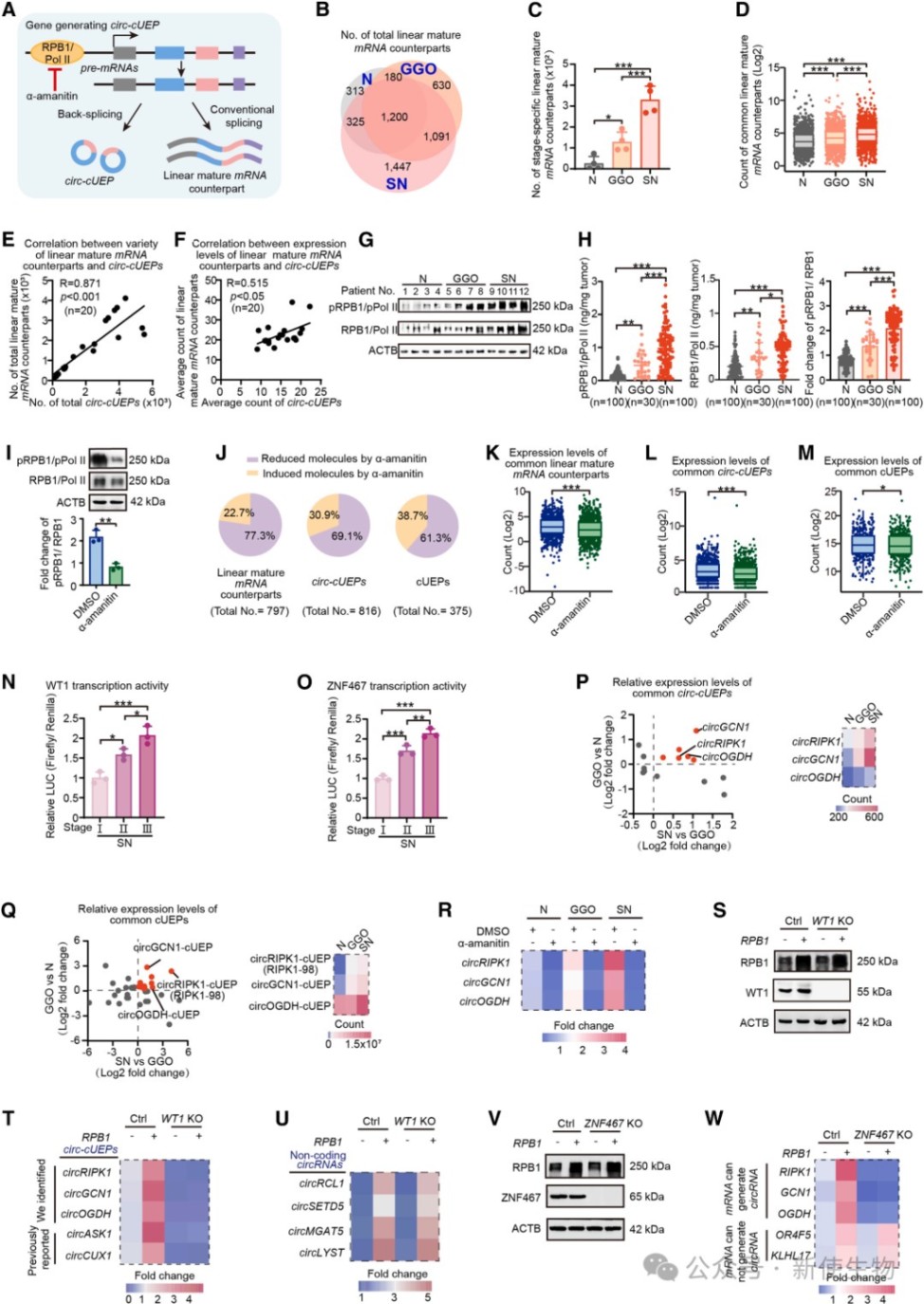
研究利用α-鹅膏蕈碱抑制实验证实,RNA聚合酶II亚基RPB1对前体mRNA的转录是产生这些circRNA及其编码蛋白的关键。
同时发现,转录因子WT1和ZNF467在肺腺癌进展中活性增强,负责驱动相关基因的表达。
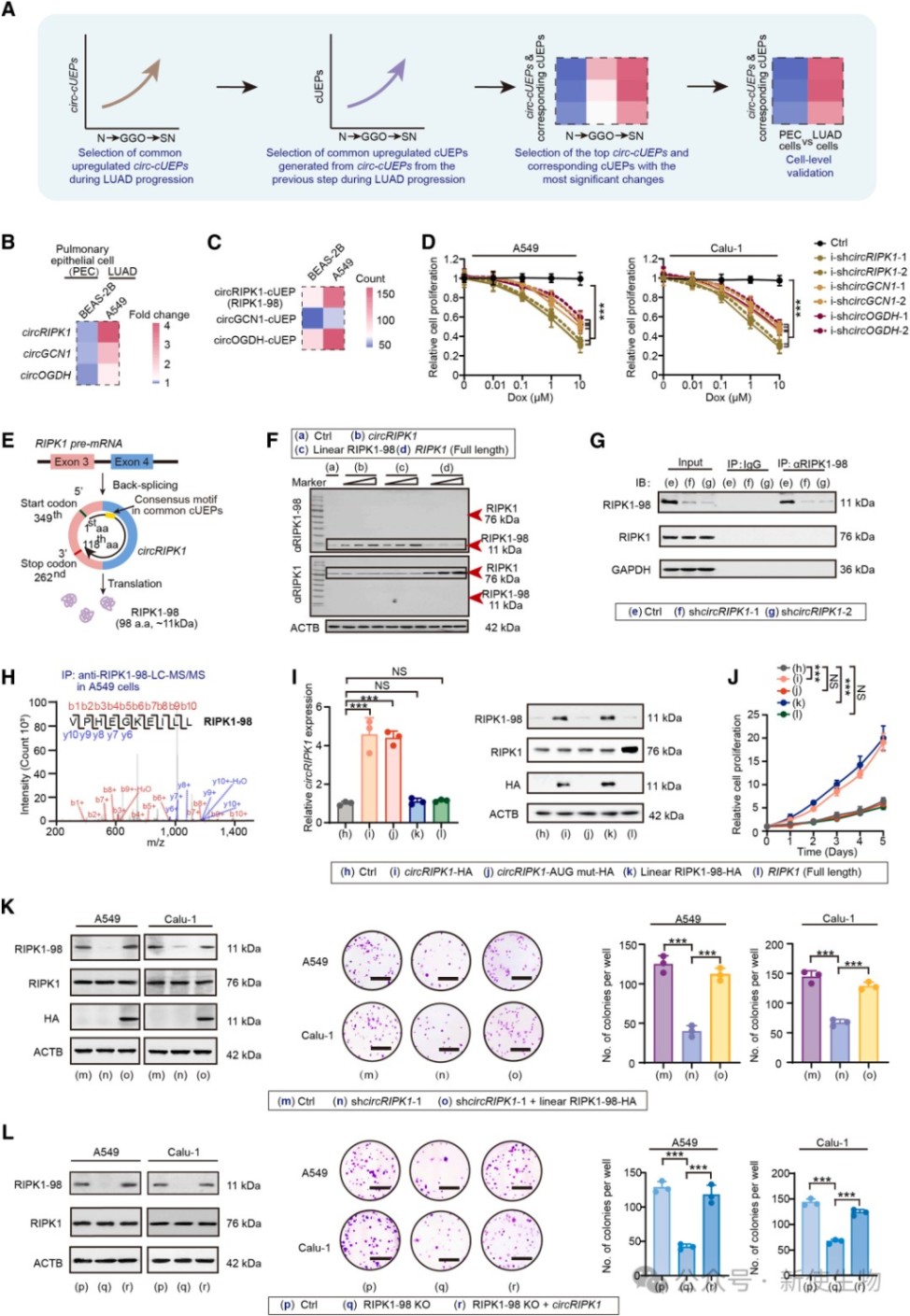
三、circRIPK1编码的RIPK1-98是促进肺腺癌细胞增殖的关键蛋白
通过功能筛选,研究确认了由circRIPK1编码的98个氨基酸的蛋白RIPK1-98能显著促进肺腺癌细胞增殖。
实验证明,该蛋白与母基因产生的RIPK1激酶功能完全不同,它是通过增强细胞群体的克隆形成能力来发挥癌基因作用的。
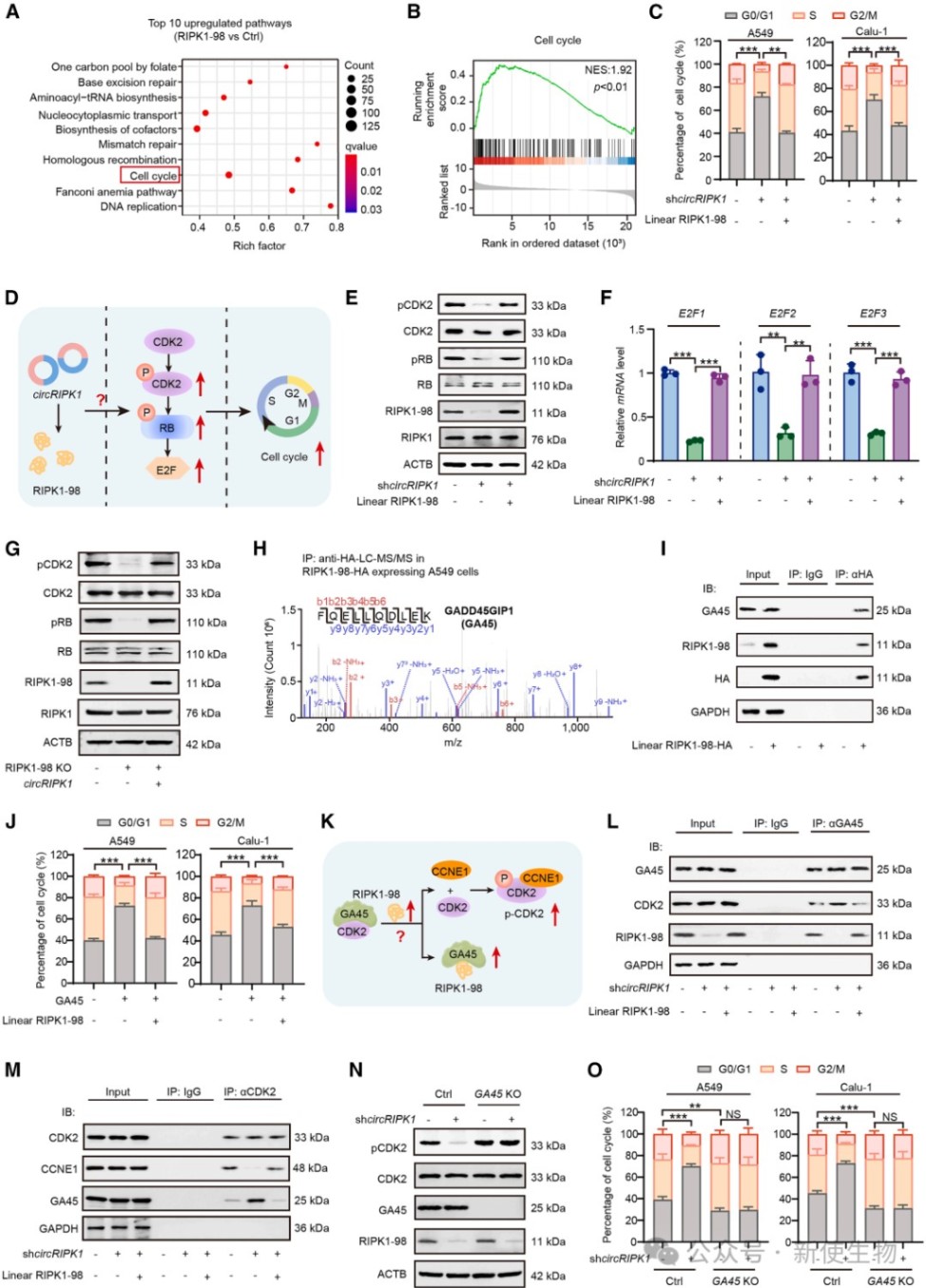
四、RIPK1-98通过竞争性结合GA45释放CDK2来加速细胞周期
机制研究显示,RIPK1-98能与细胞周期负调控因子GA45结合,从而竞争性地阻断GA45与CDK2的相互作用。
这种竞争使得CDK2得以释放并被磷酸化激活,进而通过RB/E2F信号通路推动细胞从G0/G1期向S期转化。
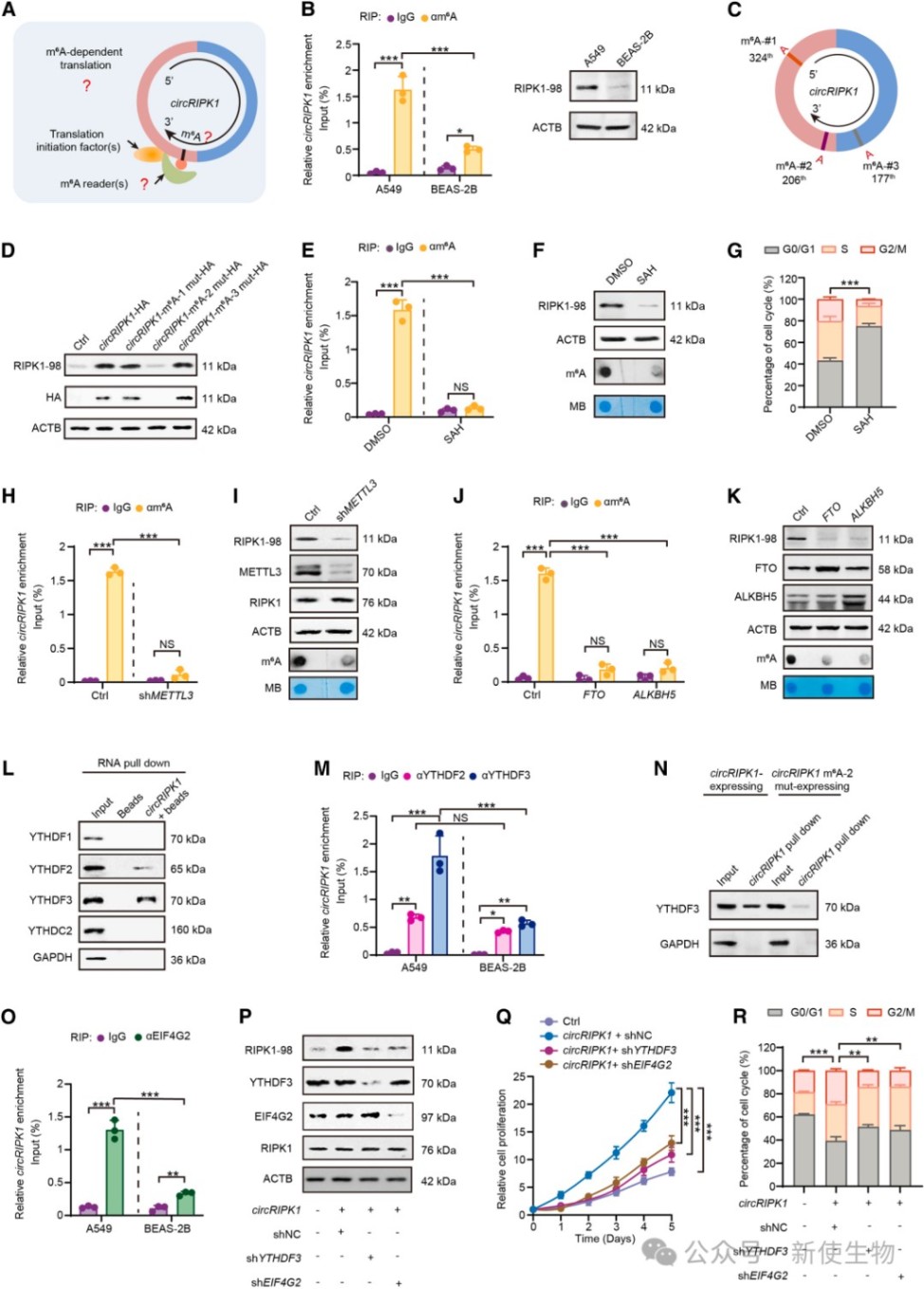
五、circRIPK1的翻译依赖于m⁶A修饰和YTHDF3介导的机制
研究发现circRIPK1通过其序列上的m⁶A修饰位点招募阅读器蛋白YTHDF3。
随后,该复合物进一步招募翻译起始因子EIF4G2,在多聚核糖体上启动RIPK1-98蛋白的非经典翻译过程。
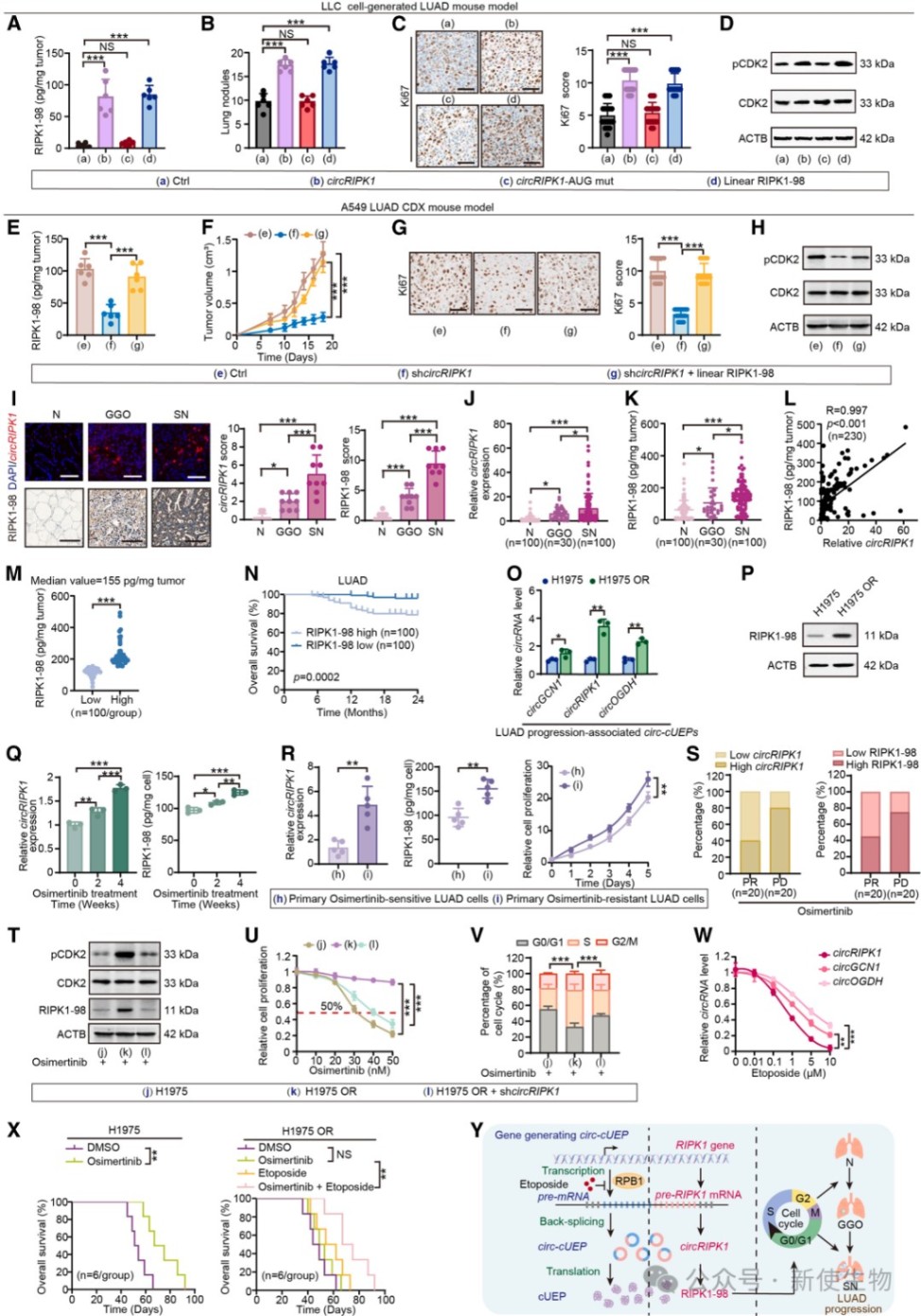
六、靶向RIPK1-98可抑制肿瘤生长并克服奥希莫替尼耐药
在动物模型和临床队列中,RIPK1-98水平与肿瘤生长速度及不良预后密切相关。
此外,下调RIPK1-98或联合应用RPB1抑制剂能显著逆转肺腺癌对奥希替尼的耐药性。
总结
本文揭示了肺腺癌中环状RNA编码蛋白组的动态变化特征,并深入解析了RIPK1-98蛋白驱动肿瘤细胞周期的分子机制。研究证明了通过干预该蛋白的转录或翻译水平,可以有效抑制肿瘤进展并克服靶向治疗耐药,具有重要的临床转化价值。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们