导读
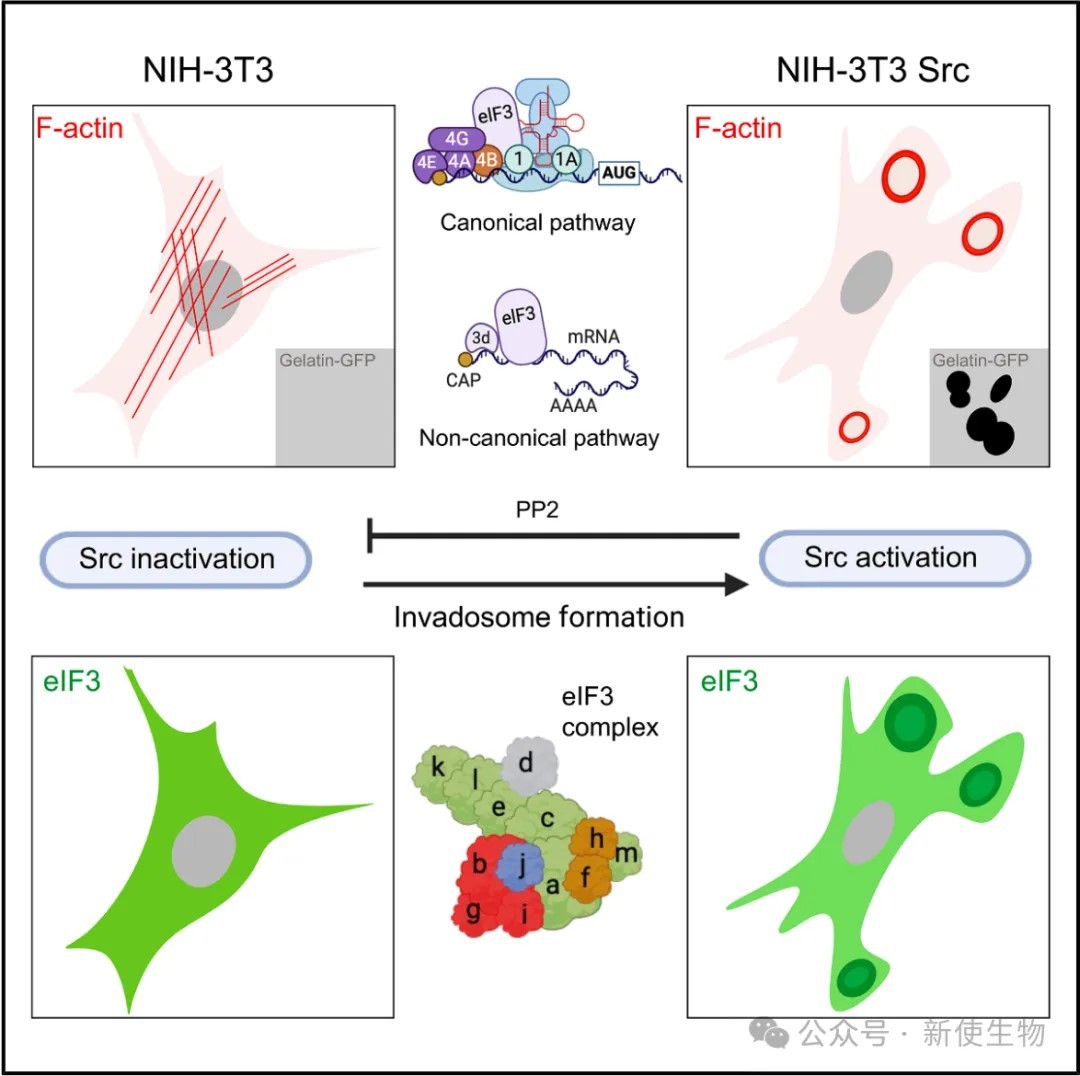
细胞外基质(ECM)的降解是癌细胞迁移和侵袭的关键步骤,最终导致肿瘤进展和转移。侵袭伪足(Invadosomes)是细胞中专门负责ECM重塑的动态F-肌动蛋白结构。
近年来的研究发现,侵袭伪足不仅是细胞骨架结构,还是局部mRNA翻译的热点区域,能够确保与细胞粘附和侵袭相关的蛋白质在特定空间内被合成。先前的研究已经证实,侵袭伪足中富含核糖体和多种翻译起始因子,特别是真核翻译起始因子3(eIF3)复合物的多个亚基。
eIF3亚基在多种癌症中表达异常,并与肿瘤侵袭和转移有关。Src是一种重要的酪氨酸激酶癌基因,已知其能够激活调控蛋白质合成的信号通路,但Src活性与翻译调控之间的直接联系仍不明确。
2026年3月24日,法国国家健康与医学研究院Frédéric Saltel和Benjamin Bonnard团队在Cell Reports上发表了一篇题为“Src promotes tumor cell invasion by hijacking the translation machineries”的论文。该研究发现,Src癌基因通过双重机制调控蛋白质合成,即同时激活经典的mTOR依赖的翻译途径和非经典的eIF3d依赖的翻译途径。

文章索引
【标题】Src promotes tumor cell invasion by hijacking the translation machineries
【发表期刊】Cell Reports
【发表日期】2026年3月24日
【作者及团队】法国国家健康与医学研究院Frédéric Saltel和Benjamin Bonnard团队
【IF】 6.9
研究结果
一、Src激酶活性调控蛋白质合成和特定eIF3亚基的表达
通过SUnSET实验和Src激酶抑制剂(PP2)处理,研究证实Src激酶活性正向调控整体蛋白质合成水平。
蛋白质组学分析进一步发现,Src的激活上调了多种翻译相关蛋白,特别是eIF3复合物的eIF3e、eIF3h等多个亚基的表达。
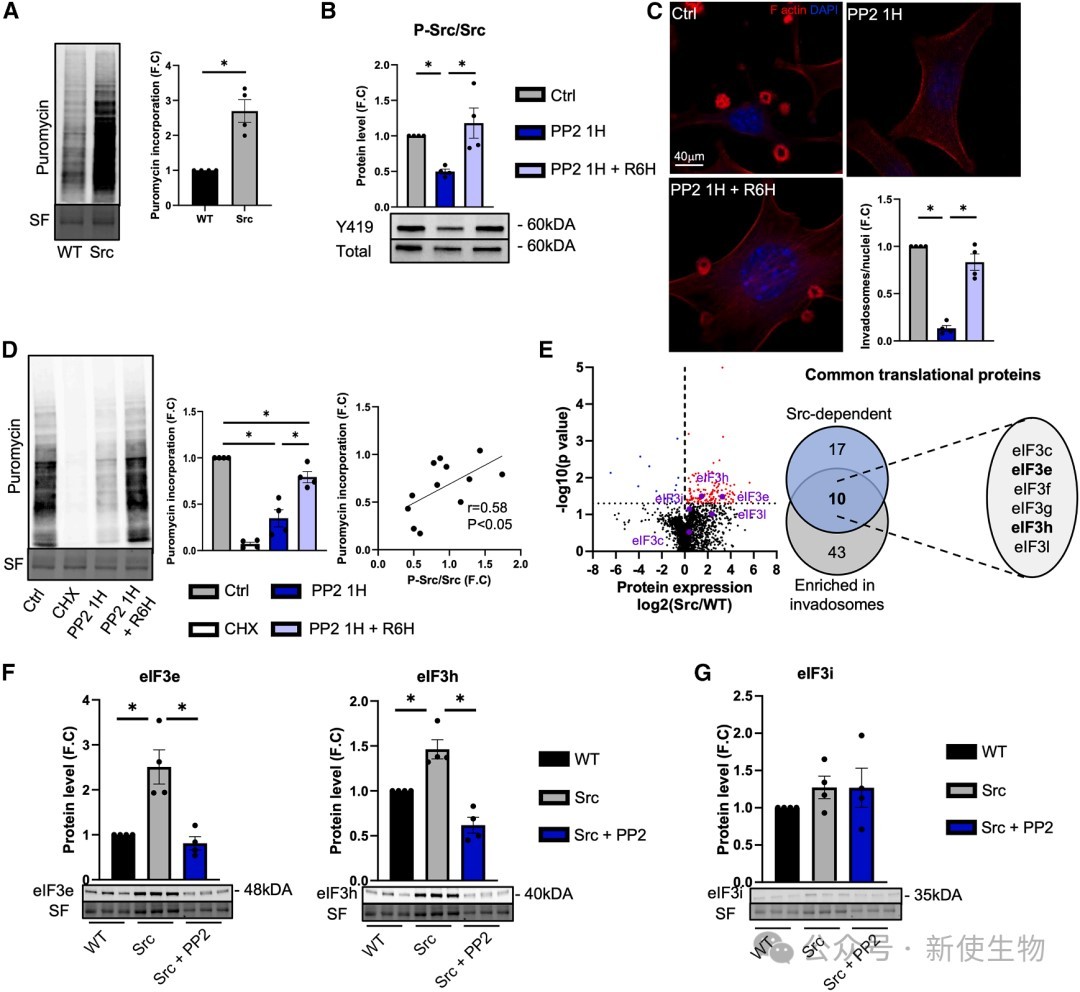
Polysome profiling多聚核糖体分析发现,PP2处理导致重多聚核糖体减少,同时60S和80S亚基组分相应增加。
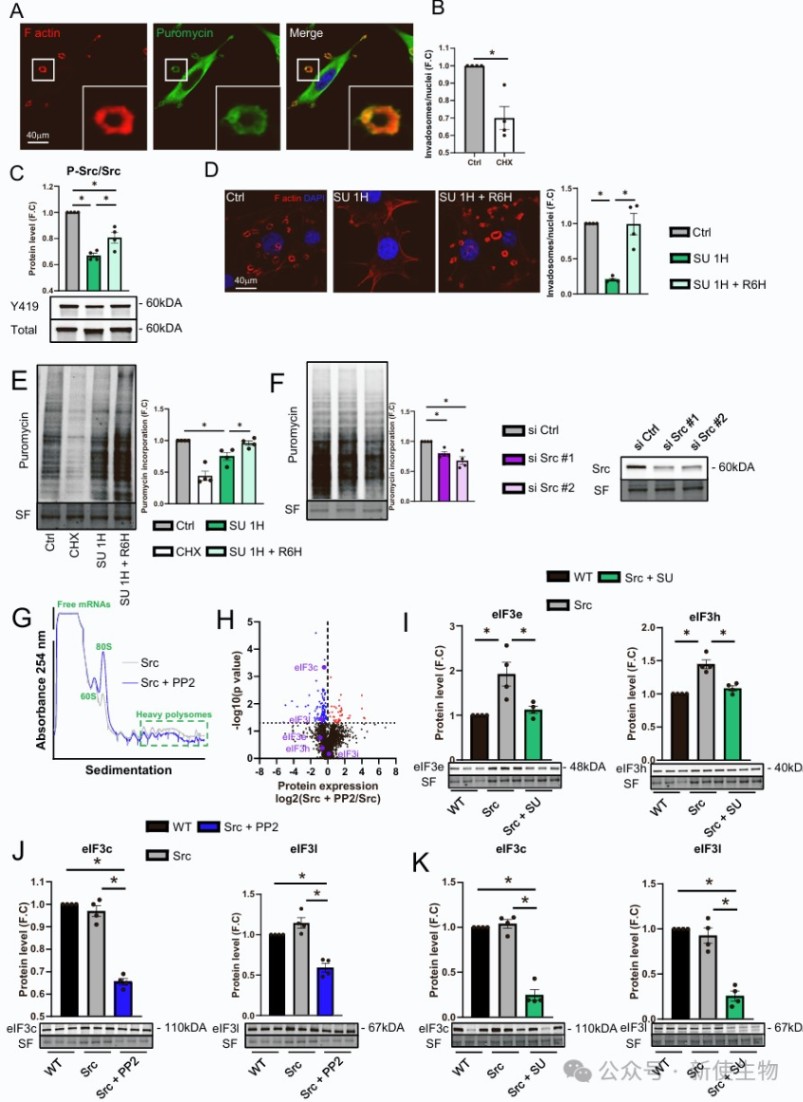
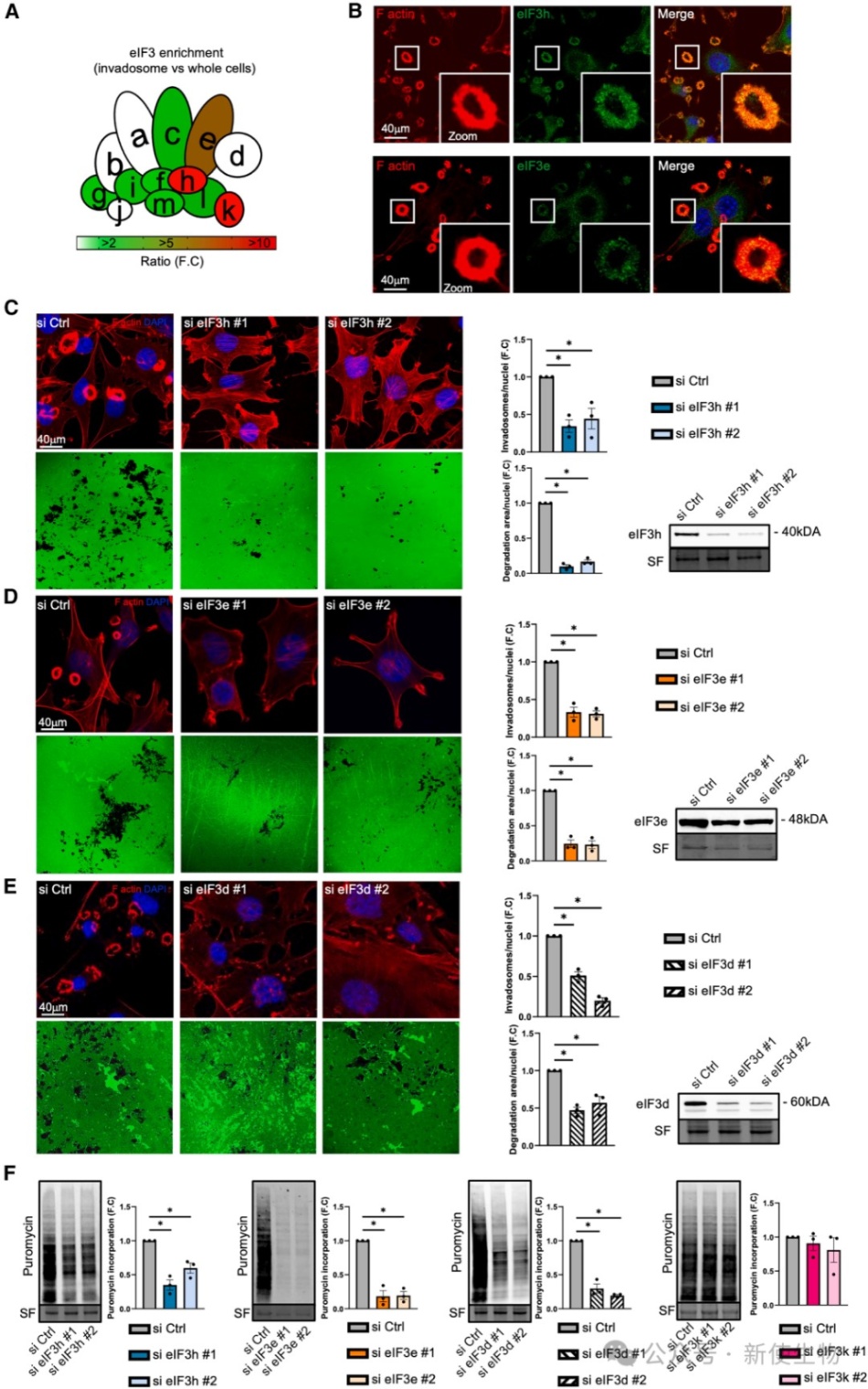
二、Src调控的eIF3亚基是侵袭伪足形成和功能的关键
利用siRNA技术分别敲低eIF3h、eIF3e和eIF3d后,细胞形成侵袭伪足的能力、降解细胞外基质的活性以及整体侵袭性均显著降低。
这表明这些受Src调控的eIF3亚基是侵袭伪足发挥其功能的必要分子。
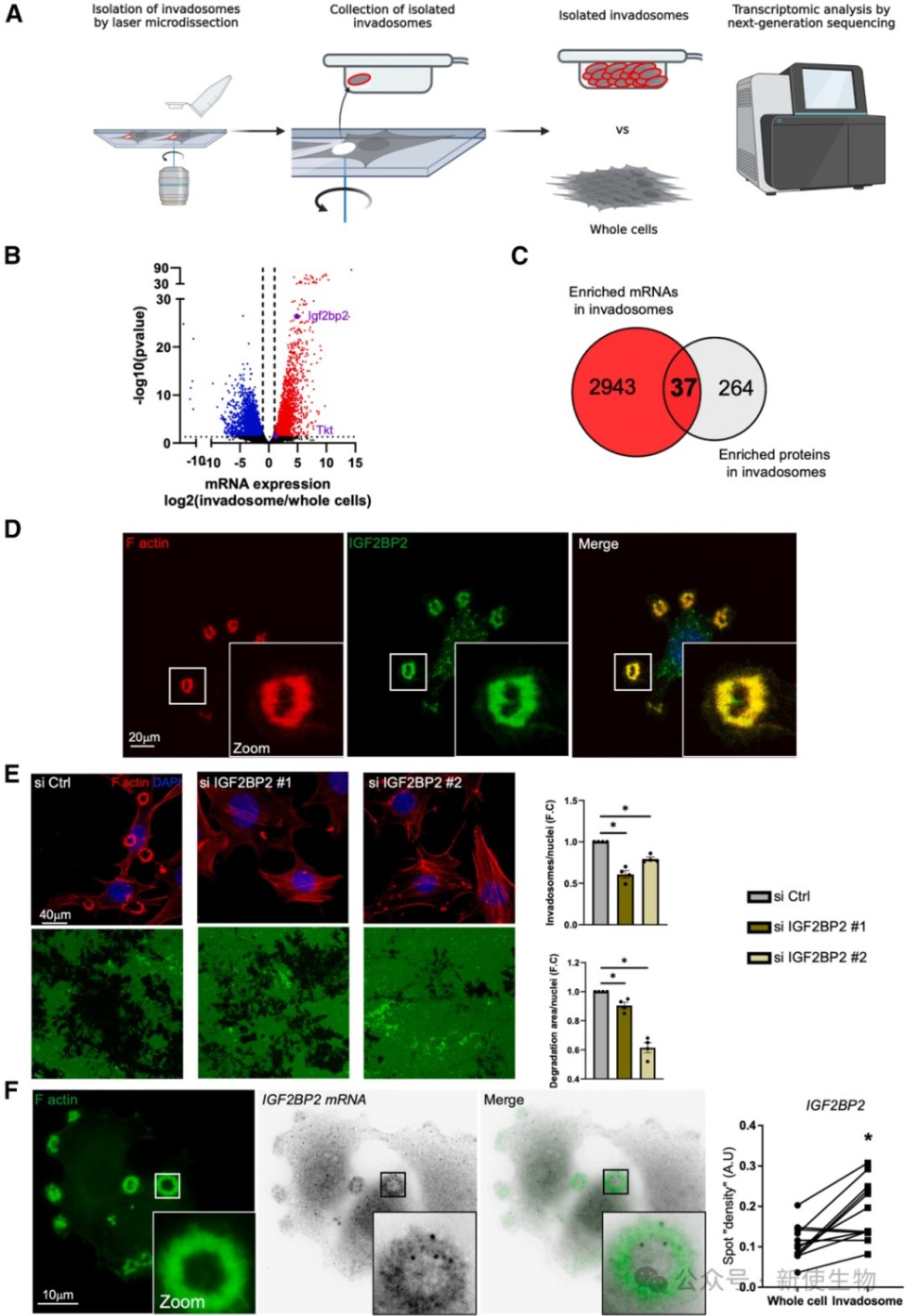
三、侵袭伪足是eIF3依赖性mRNA的局部翻译位点
通过对激光捕获的侵袭伪足进行转录组测序,研究鉴定出在侵袭伪足中富集的mRNAs,并发现其中IGF2BP2和TKT的翻译受eIF3调控。
功能实验证实,IGF2BP2和TKT的表达对于侵袭伪足的形成和细胞侵袭同样至关重要。
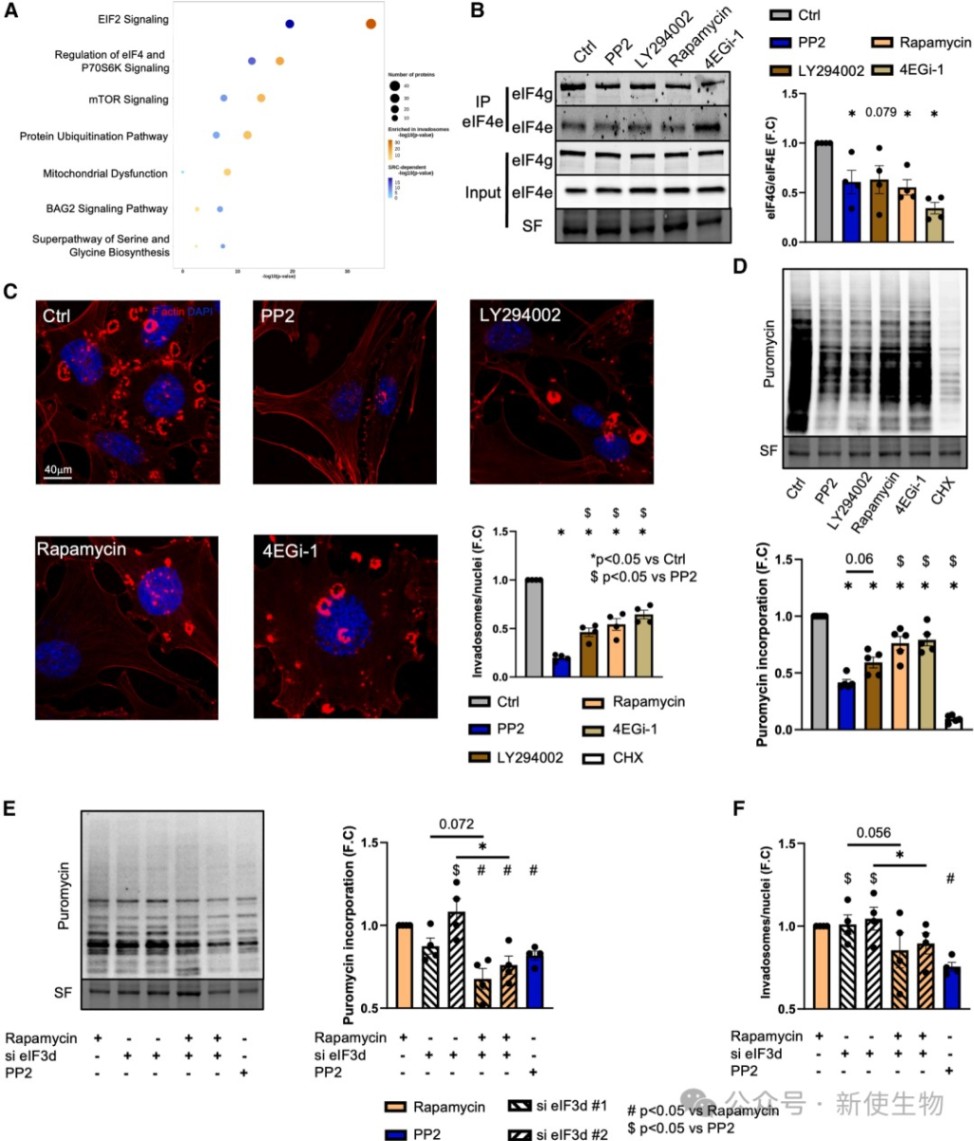
四、Src通过经典和非经典双重途径增强翻译起始
机制分析表明,Src通过激活PI3K/mTOR信号通路来增强经典的eIF4E依赖性翻译起始。
同时,Src还通过上调eIF3d的表达来驱动非经典的翻译起始,这两种机制共同协作以维持侵袭伪足的形成与功能。
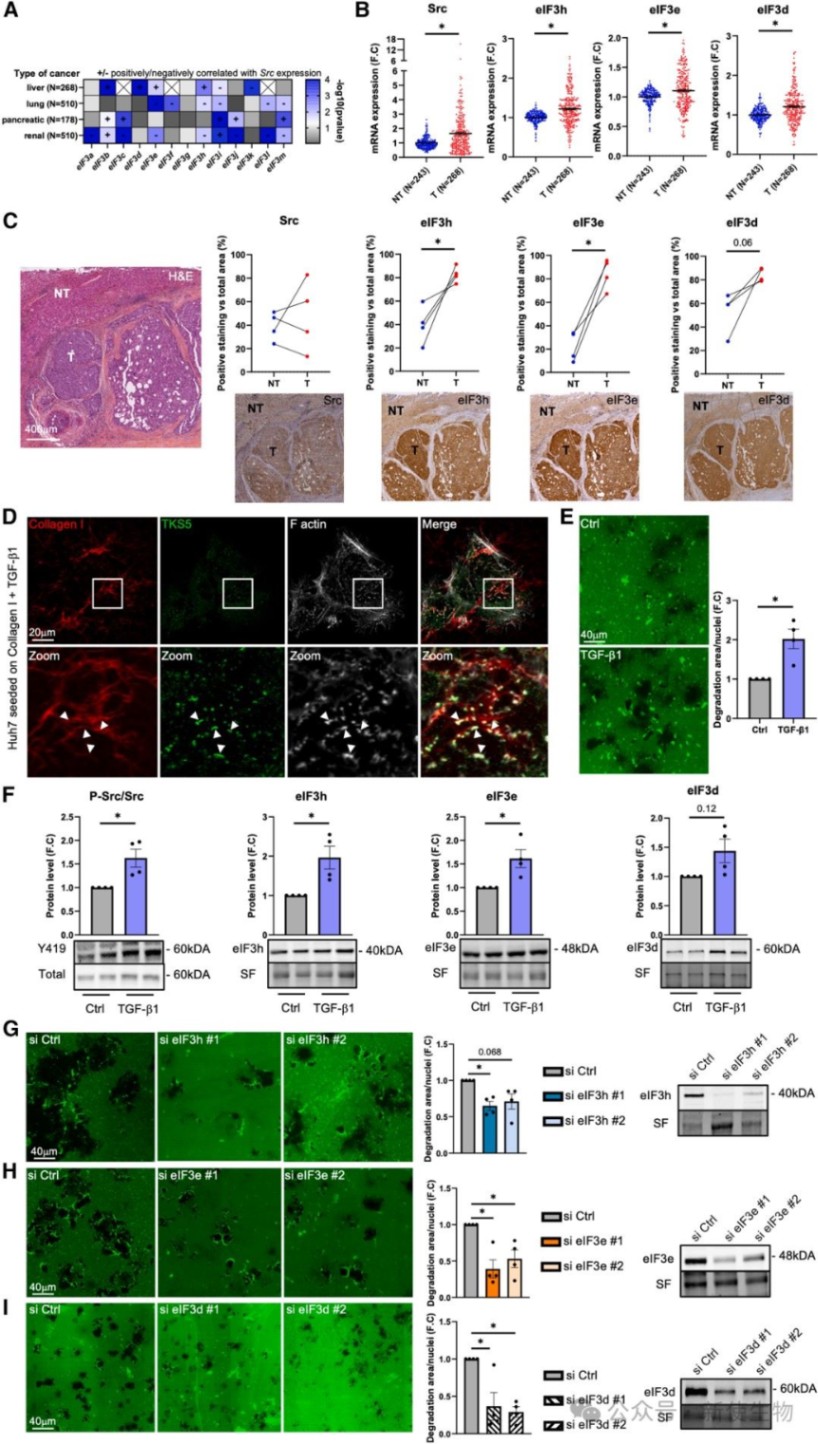
五、Src-eIF3h/e/d信号轴在肝细胞癌中富集并促进其侵袭性
在肝细胞癌(HCC)患者的临床样本数据中,Src、eIF3h、eIF3e和eIF3d的表达水平呈正相关,并与不良预后有关。
在HCC细胞系中,抑制eIF3h、eIF3e或eIF3d的表达能够有效阻断TGF-β1诱导的细胞侵袭和基质降解能力。
总结
本研究揭示了Src癌基因作为翻译起始的关键调控者,通过协同激活经典和非经典翻译途径,特异性地重塑翻译机器。这一过程对于侵袭伪足的形成、细胞外基质降解以及最终的肿瘤细胞侵袭至关重要,为理解肿瘤侵袭机制和开发潜在治疗靶点提供了新的视角。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们