导读
肺癌是全球癌症相关死亡的首要原因,其中肺腺癌(LUAD)作为主要亚型,治疗靶点有限且五年生存率极低。尽管靶向治疗和免疫检查点抑制剂等疗法取得了一定进展,但耐药性问题仍然是巨大的临床挑战,因此亟需深入理解LUAD的发病机制并探索新的治疗靶点。
近年来,转录组学和蛋白质组学研究揭示,许多曾被认为是“非编码”的长链非编码RNA(lncRNA)实际上可以通过其内部的非经典开放阅读框(ORF)翻译出具有生物学功能的微蛋白。这些lncRNA来源的微蛋白或多肽在肿瘤中的功能角色很大程度上尚不明确。
已有研究表明,这些微蛋白可以参与肿瘤的恶性进展,甚至可以作为肿瘤特异性抗原,为肿瘤的靶向治疗和免疫治疗提供了新的潜在方向。
2026年4月6日,南京医科大学聂凤琪、刘向华和孙明团队合作,在British Journal of Cancer上发表了题为“A novel microprotein L3EMP triggers lung adenocarcinoma progression by catalysing the deubiquitination of SIRT1”的论文。该研究发现并鉴定了一种由LINC00973编码的新型微蛋白L3EMP,它通过促进USP22介导的SIRT1去泛素化,激活AKT/ERK信号通路,从而驱动肺腺癌的恶性进展。

文章索引
【标题】A novel microprotein L3EMP triggers lung adenocarcinoma progression by catalysing the deubiquitination of SIRT1
【发表期刊】British Journal of Cancer
【发表日期】2026年4月6日
【作者及团队】南京医科大学聂凤琪、刘向华和孙明团队
【IF】6.8
研究结果
一、LINC00973编码新型微蛋白L3EMP
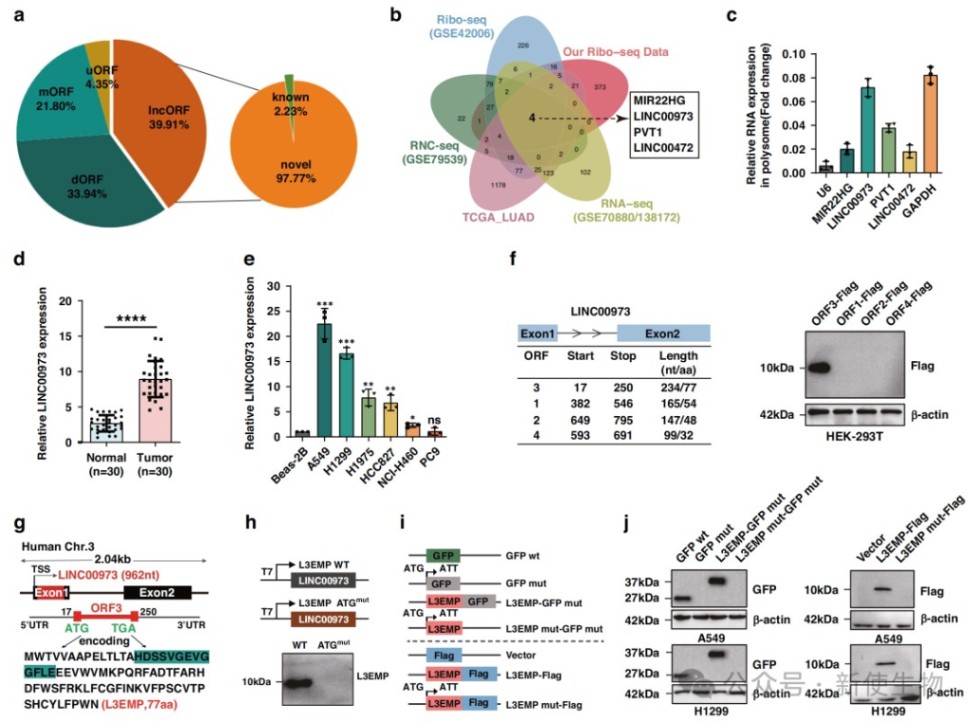
研究团队通过Ribo-seq核糖体印迹分析,发现lncRNA LINC00973具有编码潜力。
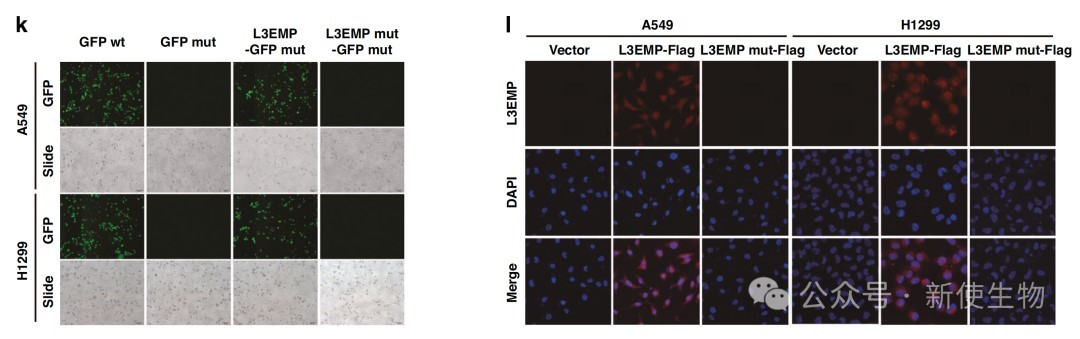
通过质谱、Western blot和荧光蛋白标记等实验,作者证实LINC00973可以翻译出一个77个氨基酸的新型微蛋白,并将其命名为L3EMP。
二、内源性L3EMP的高水平与LUAD患者的不良预后相关
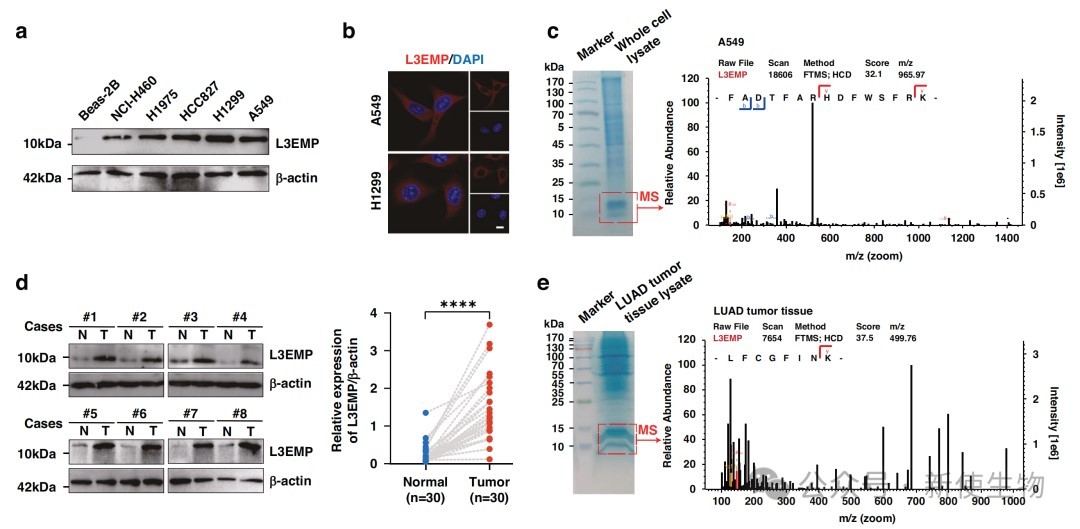
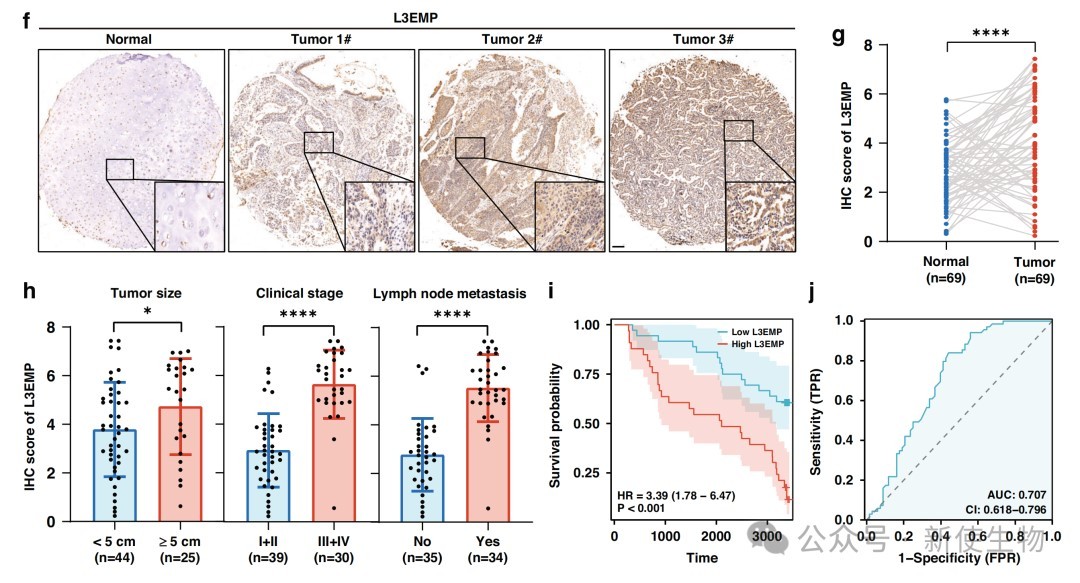
利用特异性抗体进行免疫组化与免疫荧光分析,发现L3EMP在肺腺癌组织中显著高表达,且主要定位于细胞核。
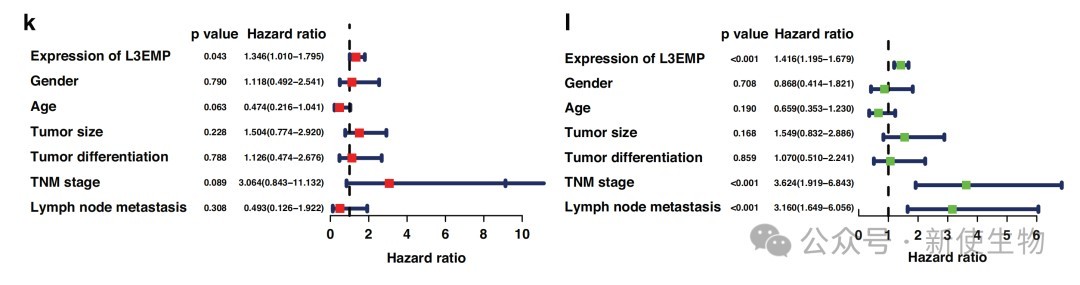
临床数据分析显示,L3EMP的高表达与肿瘤分期、淋巴结转移及患者生存期缩短密切相关,可作为独立的预后预测指标。
三、L3EMP促进肺腺癌细胞的增殖与转移
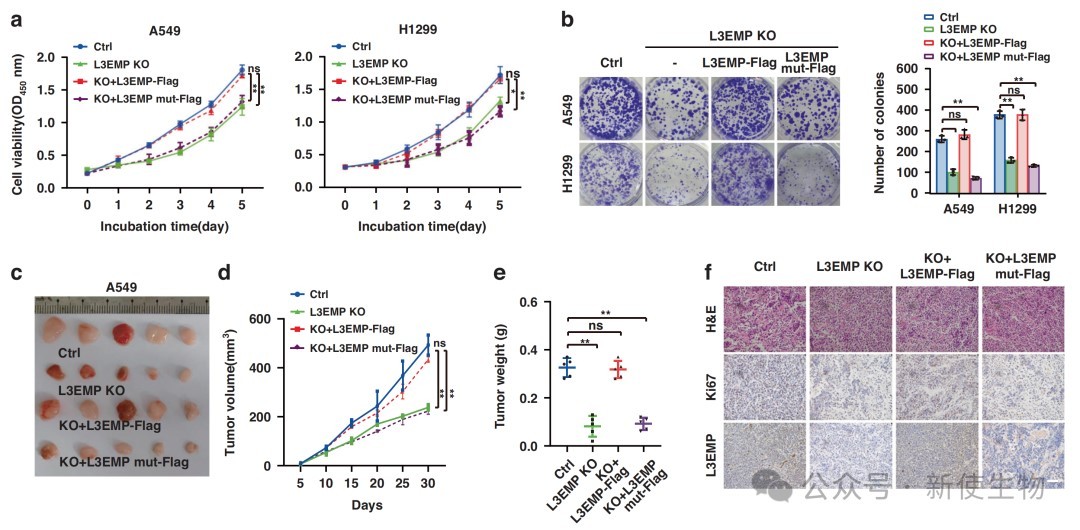
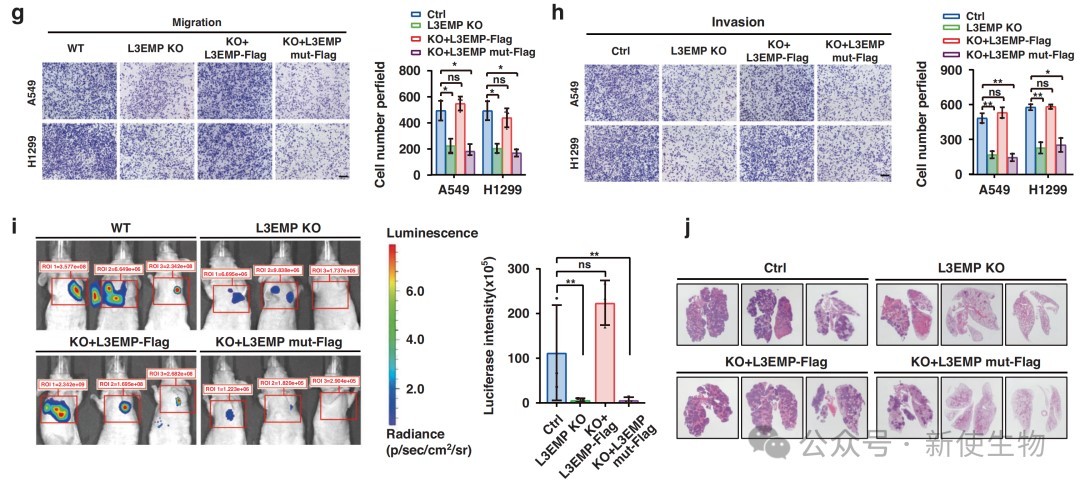
通过CRISPR/Cas9技术构建L3EMP敲除模型,实验结果表明L3EMP缺失显著抑制了肺腺癌细胞的体外增殖、迁移及侵袭能力。
体内异种移植瘤模型进一步证实,敲除L3EMP可显著减小肿瘤体积并抑制肺转移,且该表型可被野生型L3EMP回补。
四、L3EMP通过USP22介导的去泛素化稳定SIRT1
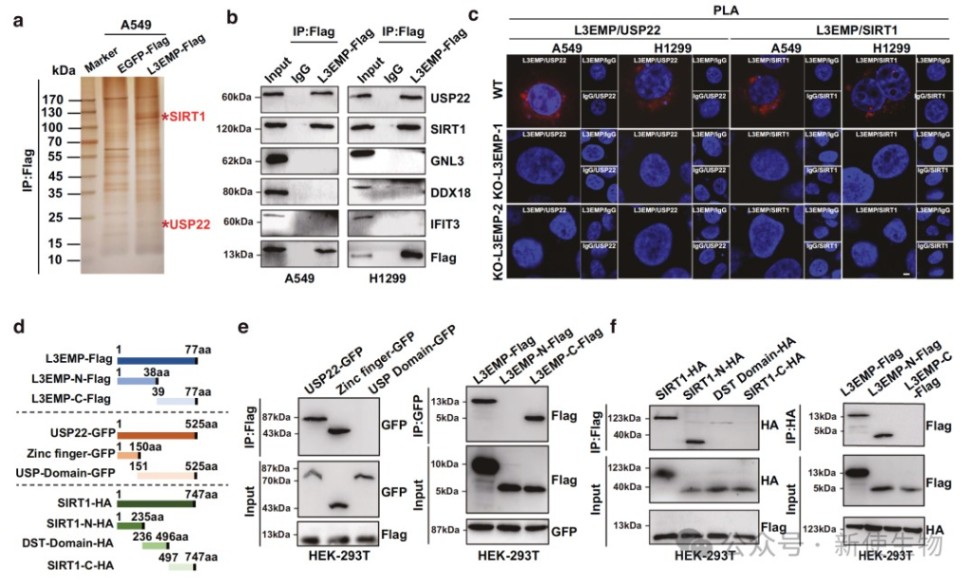
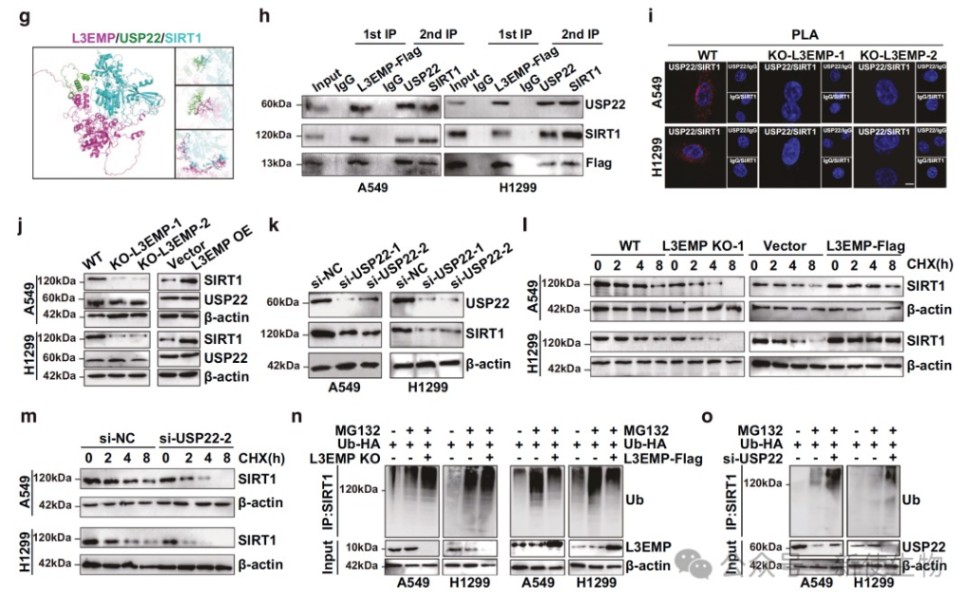
免疫共沉淀与质谱分析揭示L3EMP作为分子支架,增强了去泛素化酶USP22与底物SIRT1的相互作用。
L3EMP的存在减少了SIRT1的泛素化修饰并延长了其蛋白半衰期,从而维持了SIRT1在肺腺癌细胞中的高水平表达。
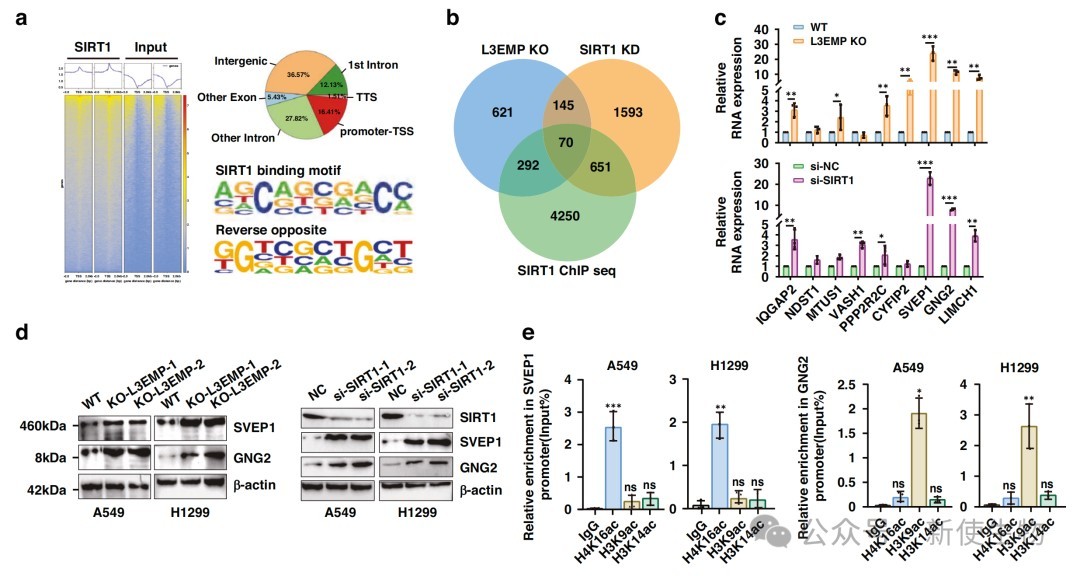
五、YY1/LINC00973-L3EMP正反馈回路驱动肿瘤进展
研究发现SIRT1通过去乙酰化修饰抑制SVEP1和GNG2的表达,进而激活AKT/ERK信号通路,促进YY1入核并转录激活LINC00973。
这一正反馈回路维持了L3EMP的高表达,持续推动肺腺癌的恶性表型。

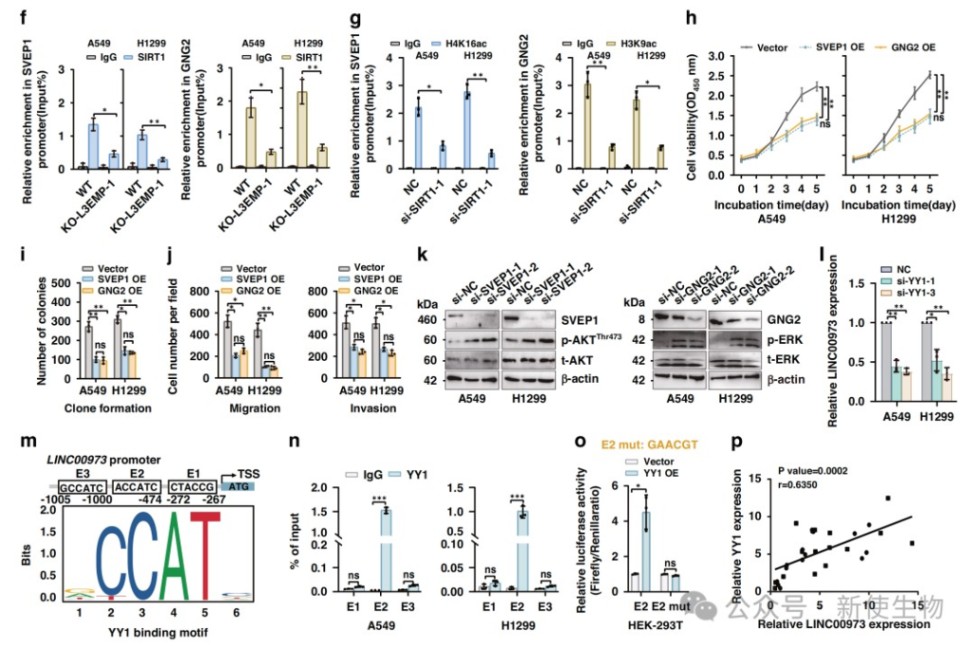
六、L3EMP作为新抗原具有疫苗开发潜力
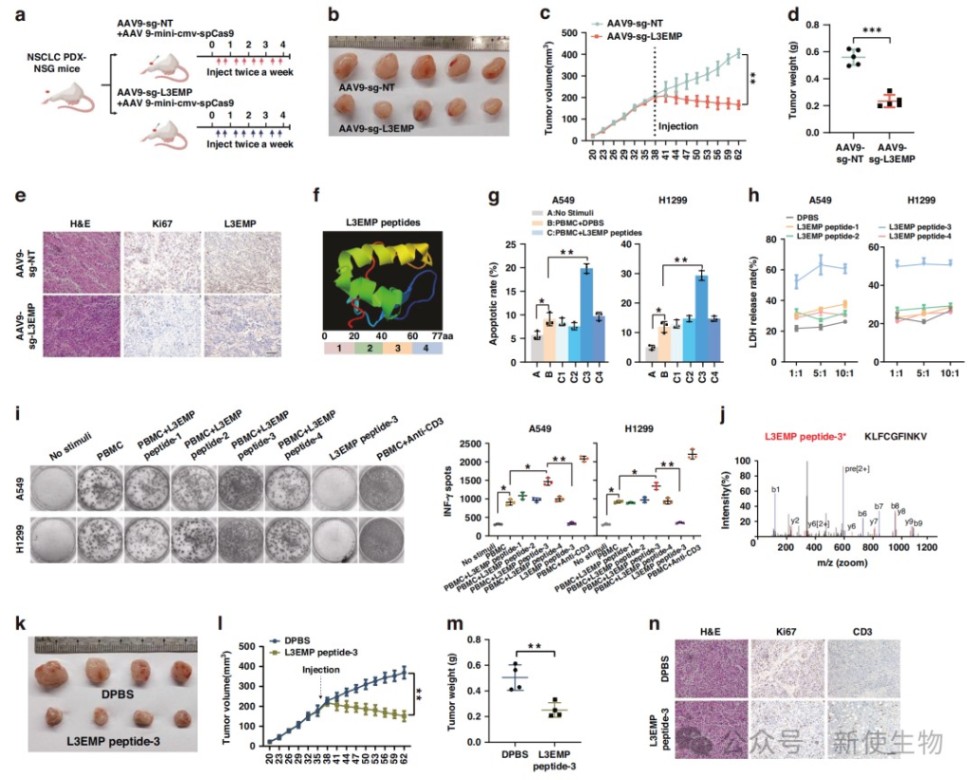
通过PDX模型验证了L3EMP作为治疗靶点的有效性,敲除L3EMP可显著抑制肿瘤生长。
此外,合成的L3EMP肽段能够诱导外周血单个核细胞产生免疫应答,并在人源化小鼠模型中增强T细胞浸润,显示出作为肿瘤疫苗抗原的潜力。
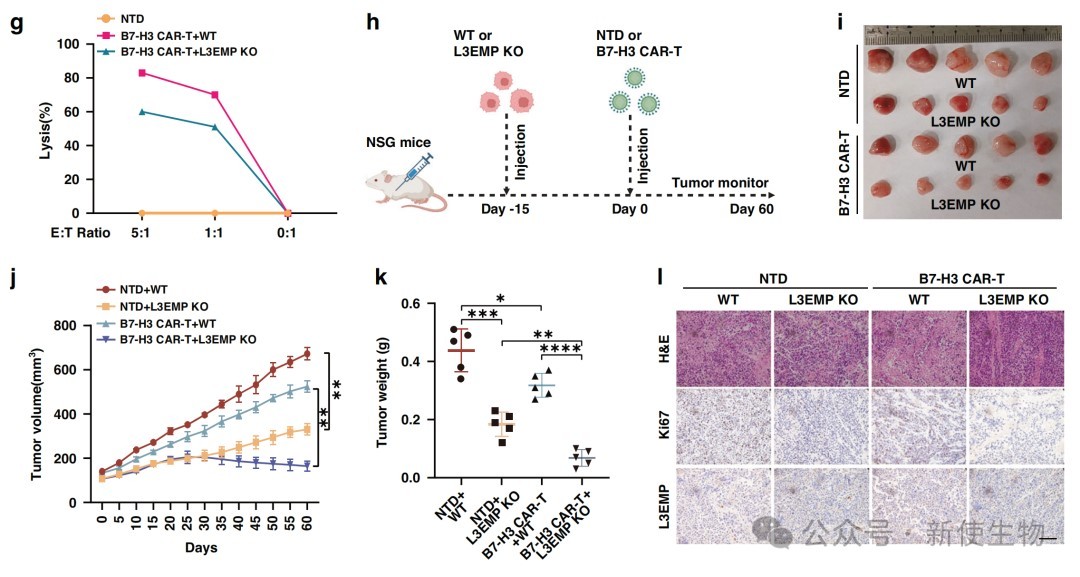
七、L3EMP敲除可增强B7-H3 CAR-T细胞的抗肿瘤疗效
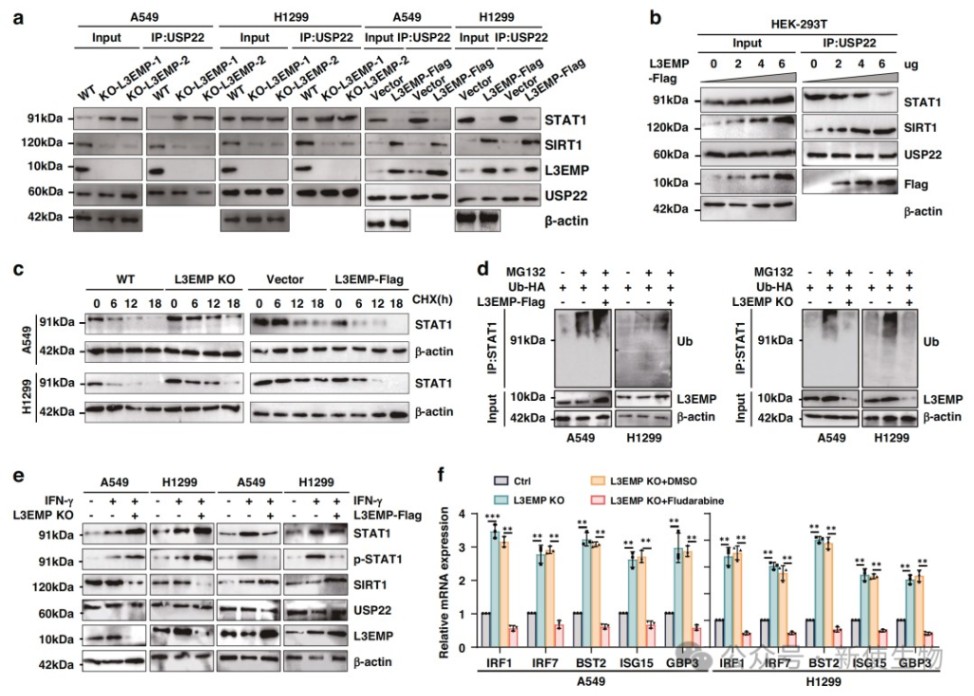
研究发现L3EMP通过竞争性结合USP22抑制了STAT1的去泛素化,而L3EMP敲除则通过激活IFN-γ/STAT1信号通路增强了肿瘤细胞对免疫攻击的敏感性。
体内外实验表明,L3EMP缺失与B7-H3 CAR-T细胞治疗具有协同效应,显著提高了抗肿瘤治疗的有效性。
总结
本研究鉴定了一个由lncRNA编码的促癌微蛋白L3EMP,并系统阐明了其通过稳定SIRT1蛋白、形成YY1介导的正反馈环路来驱动肺腺癌进展的分子机制。研究结果不仅揭示了L3EMP可作为肺腺癌治疗的直接靶点,还证明了其作为新抗原和增敏CAR-T疗法的潜力,为开发肺腺癌的创新性联合治疗策略提供了重要的理论依据和候选靶标。
点击图片查看 点击图片查看新使生物专业翻译组一站式服务平台 产品名称


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们