导读
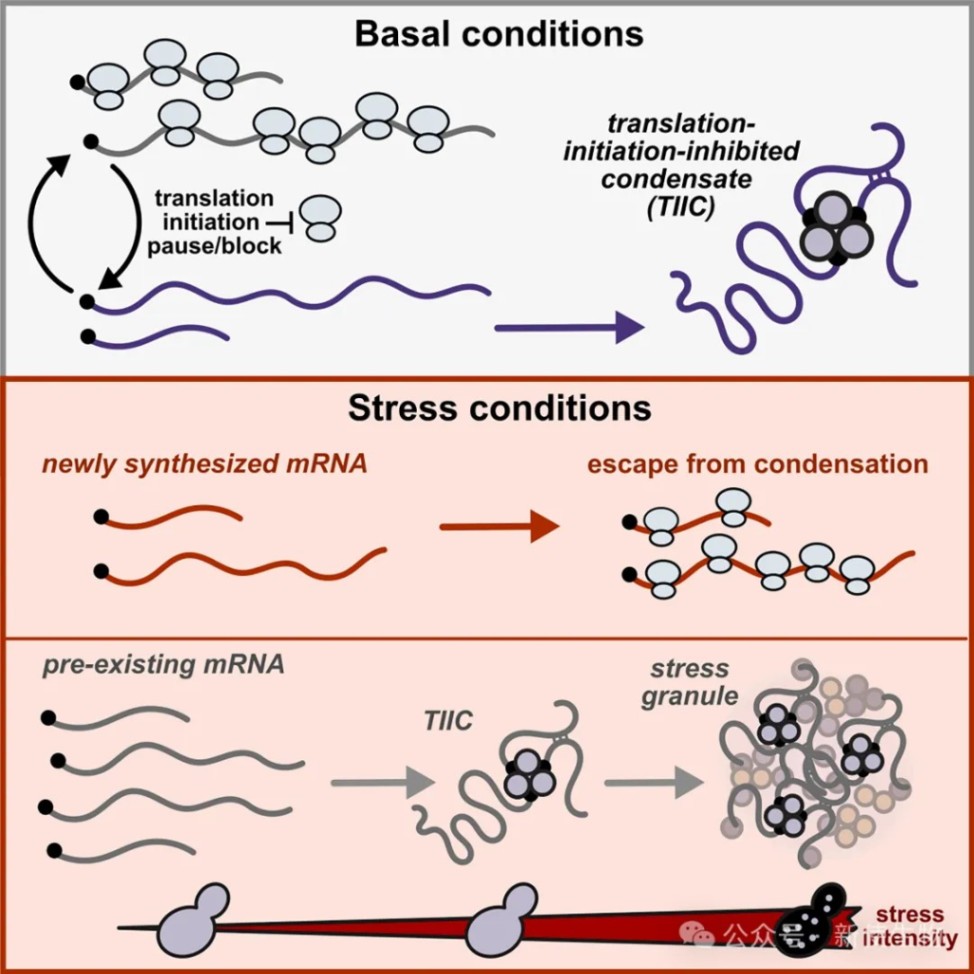
真核细胞在应对环境压力时会产生一系列保守的应激反应。这些反应包括翻译下调、应激响应转录程序激活以及细胞质中mRNA和蛋白质簇的形成。
当这些簇在显微镜下可见并与多聚腺苷酸结合蛋白等标记物共定位时,被称为应激颗粒(SGs)。应激颗粒是生物分子凝聚体的复杂实例,它们是缺乏明确化学计量关系的无膜结构,通过一系列过程形成并浓缩特定类型的生物分子。
尽管在多种系统中保守存在,但应激颗粒的功能及其与伴随的转录和翻译响应之间的关系仍不清楚。早期研究表明,应激颗粒招募多种RNA结合蛋白以及应激前存在的mRNA,但将在应激期间产生的mRNA排除在外。
2025年11月25日,芝加哥大学D. Allan Drummond与爱丁堡大学Edward W.J. Wallace团队在Molecular Cell发表了题为“Transcriptome-wide mRNP condensation precedes stress granule formation and excludes new mRNAs”的论文。研究发现,在酵母细胞中,绝大多数mRNA在压力下都会发生相分离,这一过程并不强烈依赖于mRNA长度,且往往在可见的SGs形成之前就已发生。

文章索引
【标题】Transcriptome-wide mRNP condensation precedes stress granule formation and excludes new mRNAs
【发表期刊】Molecular Cell
【发表日期】2025年11月25日
【作者及团队】芝加哥大学D. Allan Drummond与爱丁堡大学Edward W.J. Wallace团队
【IF】16.6
研究结果
一、Sed-seq技术实现了转录组尺度的mRNA凝聚测量
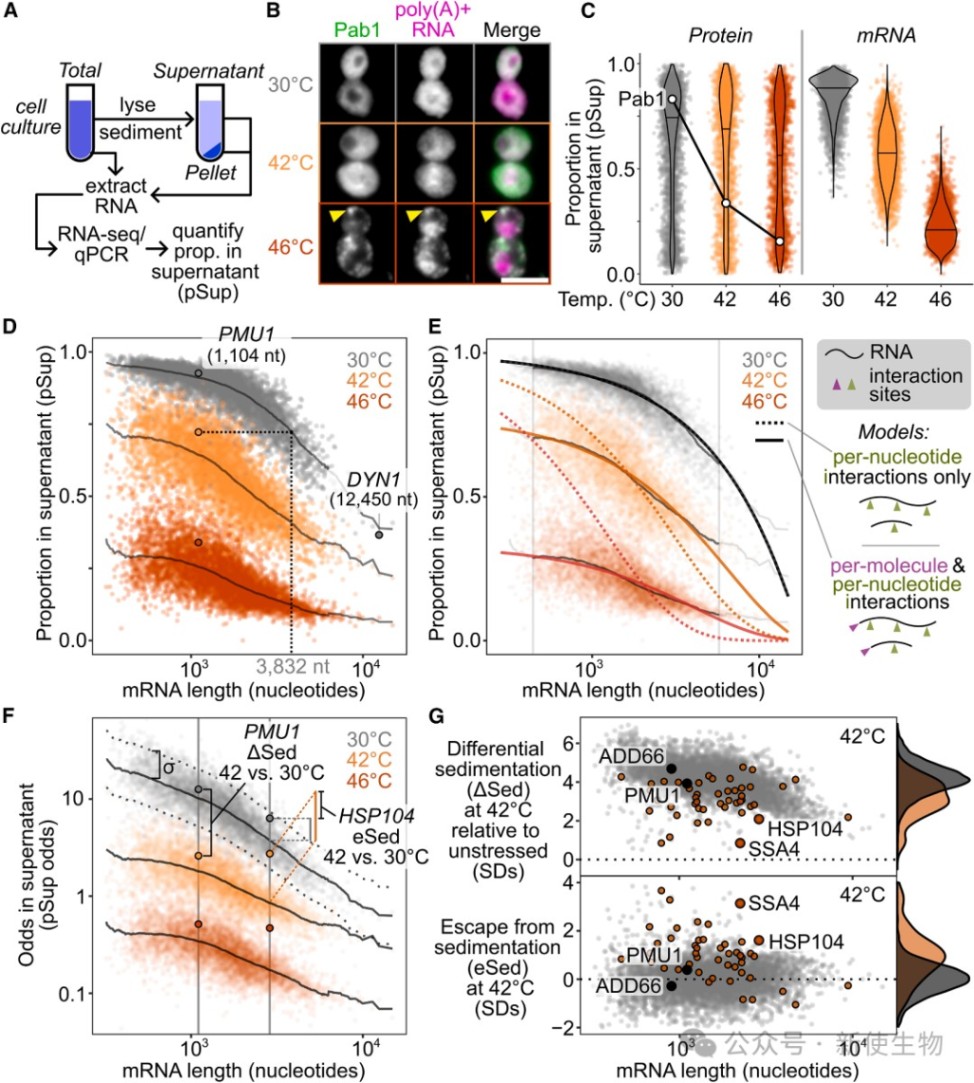
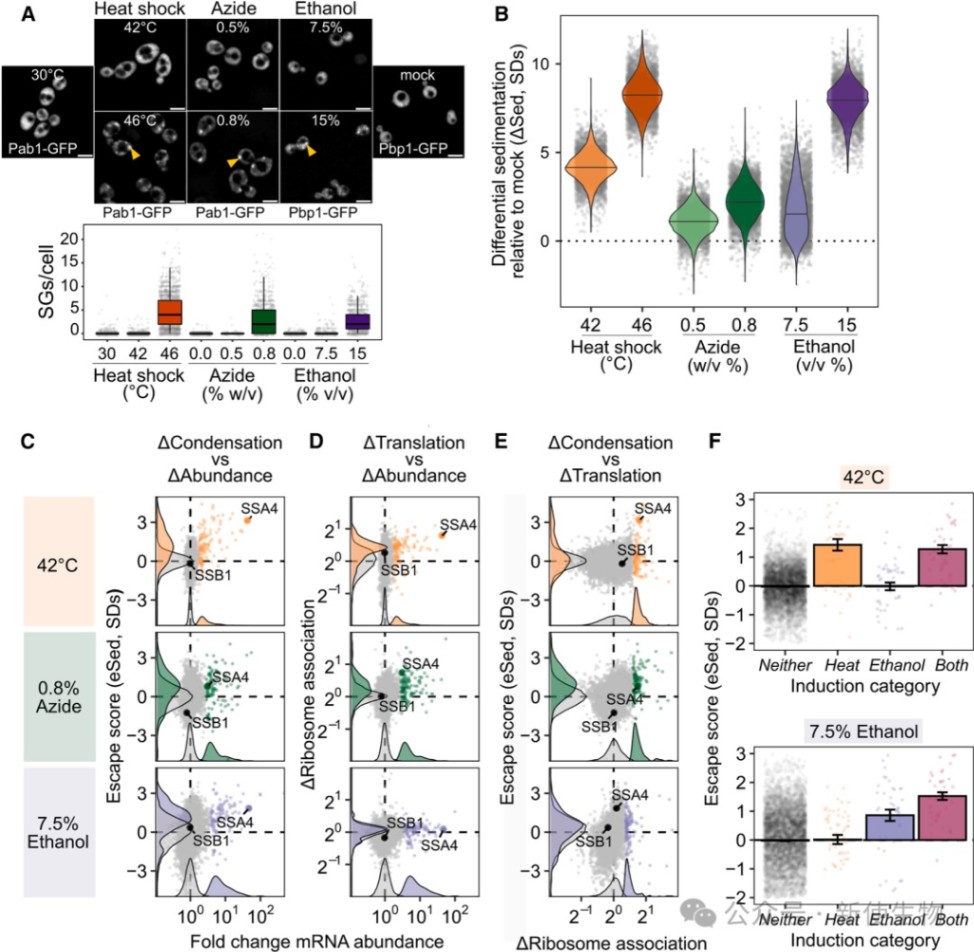
研究人员开发了Sed-seq技术(沉降结合RNA测序),发现在热休克等应激条件下,即使在未形成可见SGs的温和胁迫下,几乎所有转录组的mRNA都会发生凝聚。
与以往认为长mRNA更容易凝聚的观点不同,该研究发现这种应激诱导的凝聚与mRNA长度的相关性很小。
二、应激诱导的mRNA逃逸凝聚并被优先翻译
通过Sed-seq和单分子荧光原位杂交(smFISH)实验发现,在热休克、叠氮化钠等多种应激条件下,由Hsf1和Msn2/4等因子诱导产生的新转录本在转录组范围内表现出逃逸凝聚的现象,并不进入SGs。
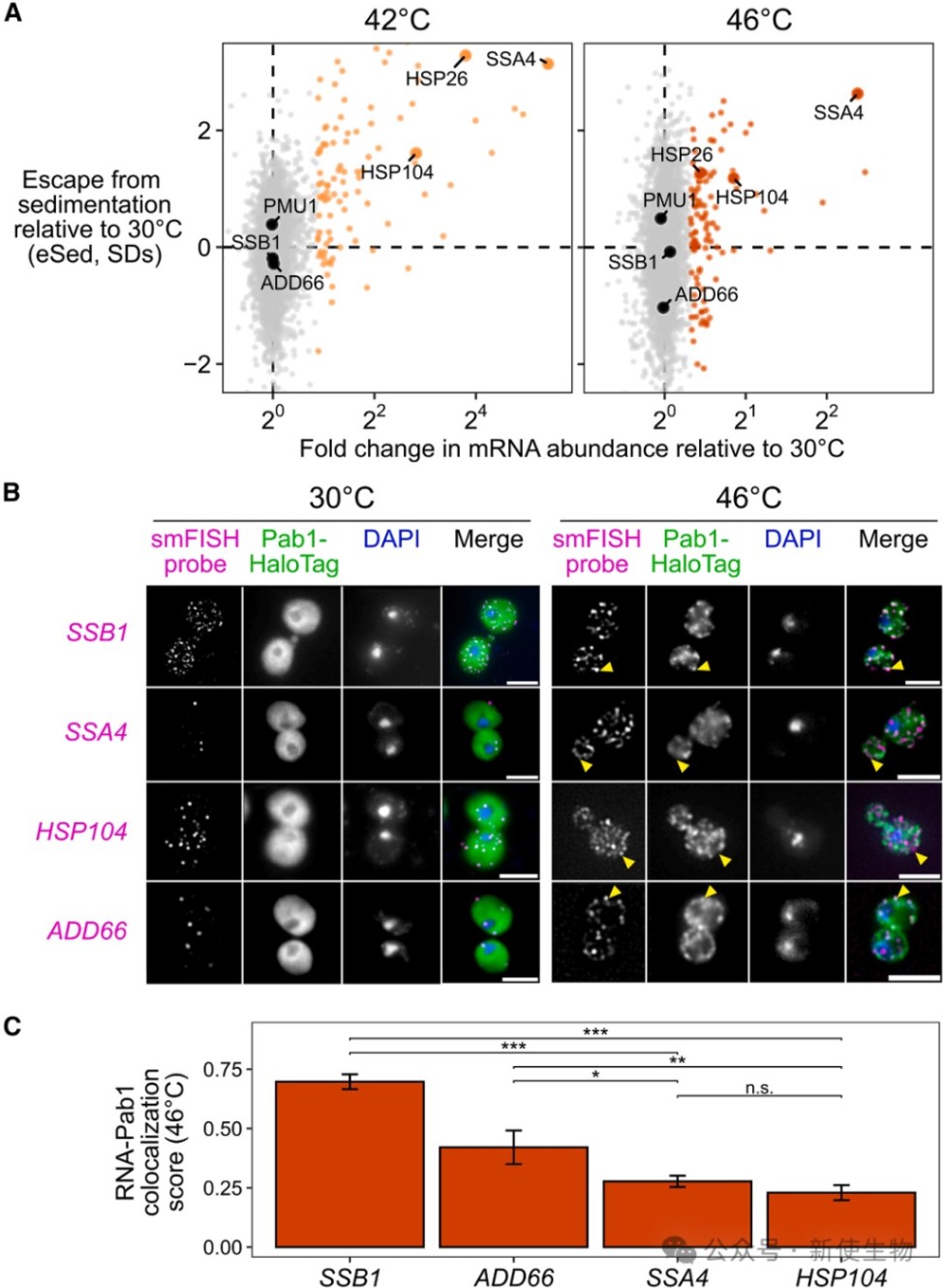
Polysome profiling多聚核糖体分析结合转录组测序(Polysome-seq)进一步证实,这些逃逸凝聚的转录本往往与多聚核糖体结合增加,即被优先翻译,说明转录诱导、翻译活跃与逃逸凝聚是协调发生的。
三、转录本“年龄”和翻译状态独立调控凝聚
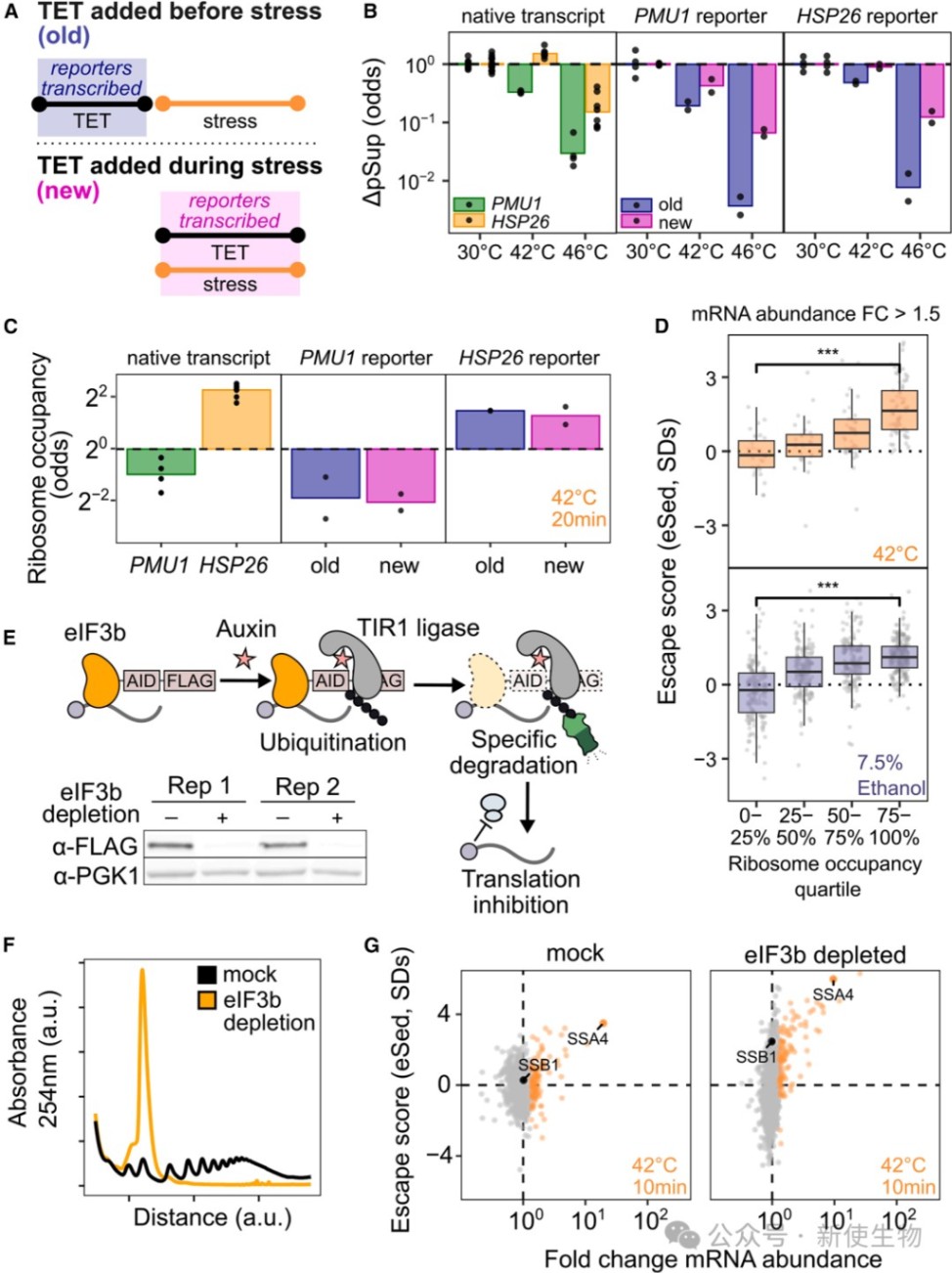
通过构建可诱导的报告基因系统,研究者分别控制转录本的产生时间和翻译状态,发现只有在应激期间新转录的mRNA(新转录本)才能显著逃逸凝聚,而应激前已存在的相同序列mRNA则会凝聚。
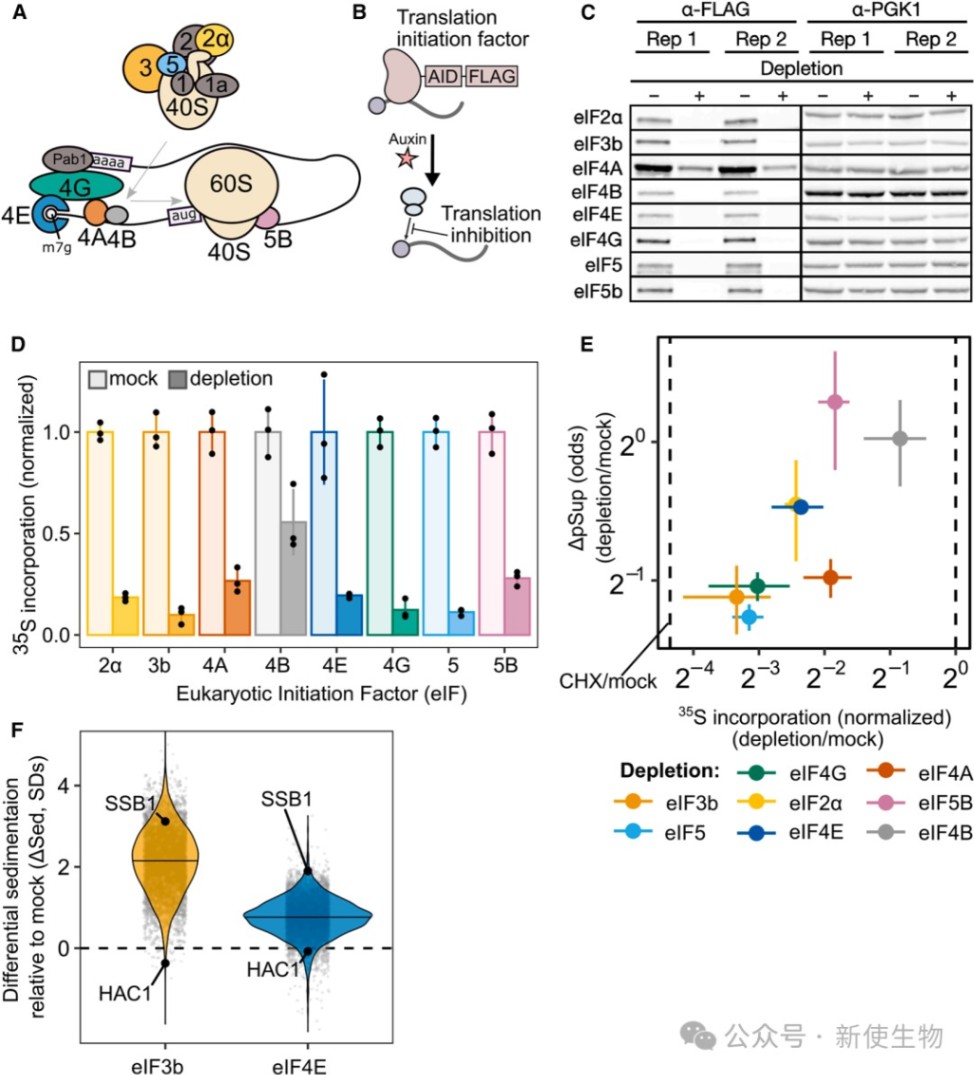
此外,通过生长素诱导降解系统(AID)耗竭翻译起始因子eIF3b导致翻译抑制后,新合成的转录本依然能逃逸凝聚。
四、翻译起始受抑制的凝聚体(TIICs)在无应激细胞中普遍存在
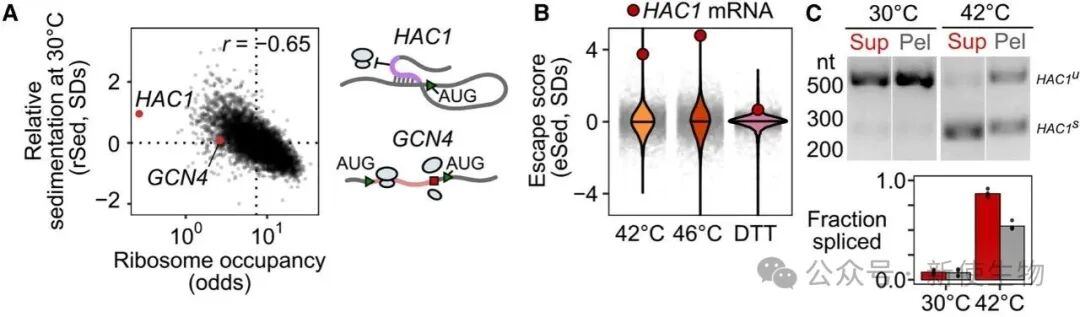
研究发现,即使在无应激的正常细胞中,翻译起始被抑制的mRNA会自发形成凝聚体,而翻译受其他方式调控的mRNA(如GCN4)则不会。
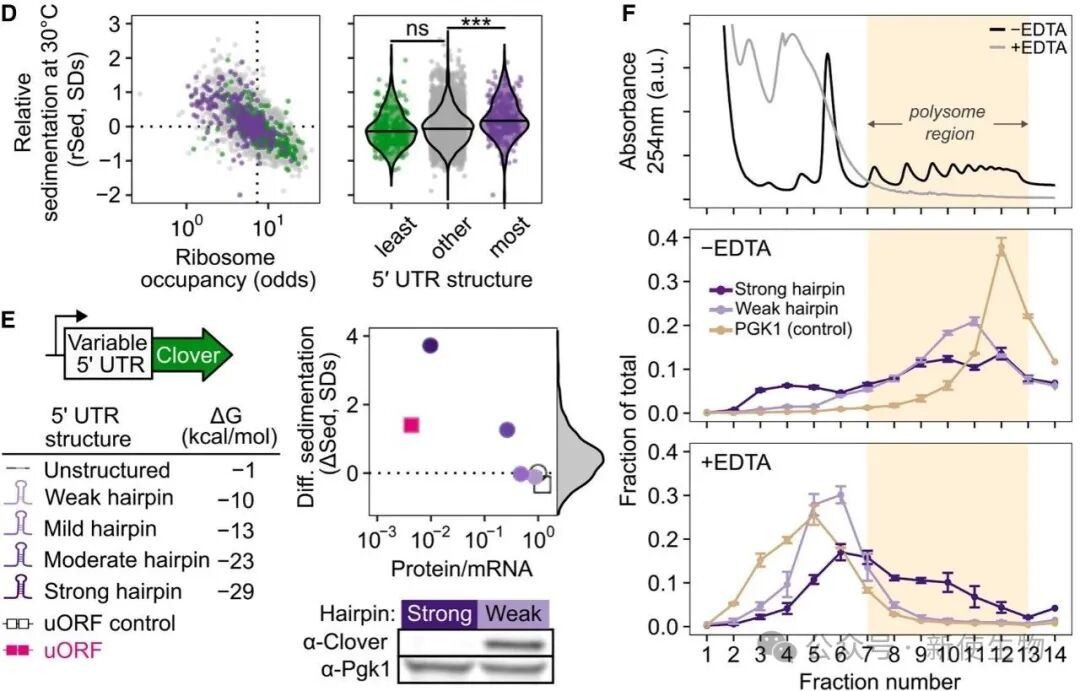
通过构建具有不同5' UTR发夹结构的人工报告基因,研究证实了抑制翻译起始是导致mRNA凝聚的直接原因,并将这些凝聚体命名为TIICs。
五、TIICs是多聚核糖体尺度的mRNP凝聚体
通过Polysome,研究显示TIICs的沉降速度与多聚核糖体相似,处于重组分中,但用EDTA处理解离核糖体后,TIICs依然保持完整并沉降,而普通结合核糖体的mRNA则会移至轻组分。
这证明TIICs是不含核糖体的大分子mRNP复合物,其沉降特性并非源于膜结合,而是源于其自身的凝聚状态。
六、全局性抑制翻译起始会引发全转录组的TIICs形成
通过系统性地耗尽多个不同的翻译起始因子(eIFs),研究发现阻断翻译起始的不同步骤均会导致全转录组范围内的mRNA发生凝聚。这一结果强有力地证明了翻译起始受阻是驱动mRNP凝聚的核心机制。
七、TIICs是应激颗粒(SGs)的前体
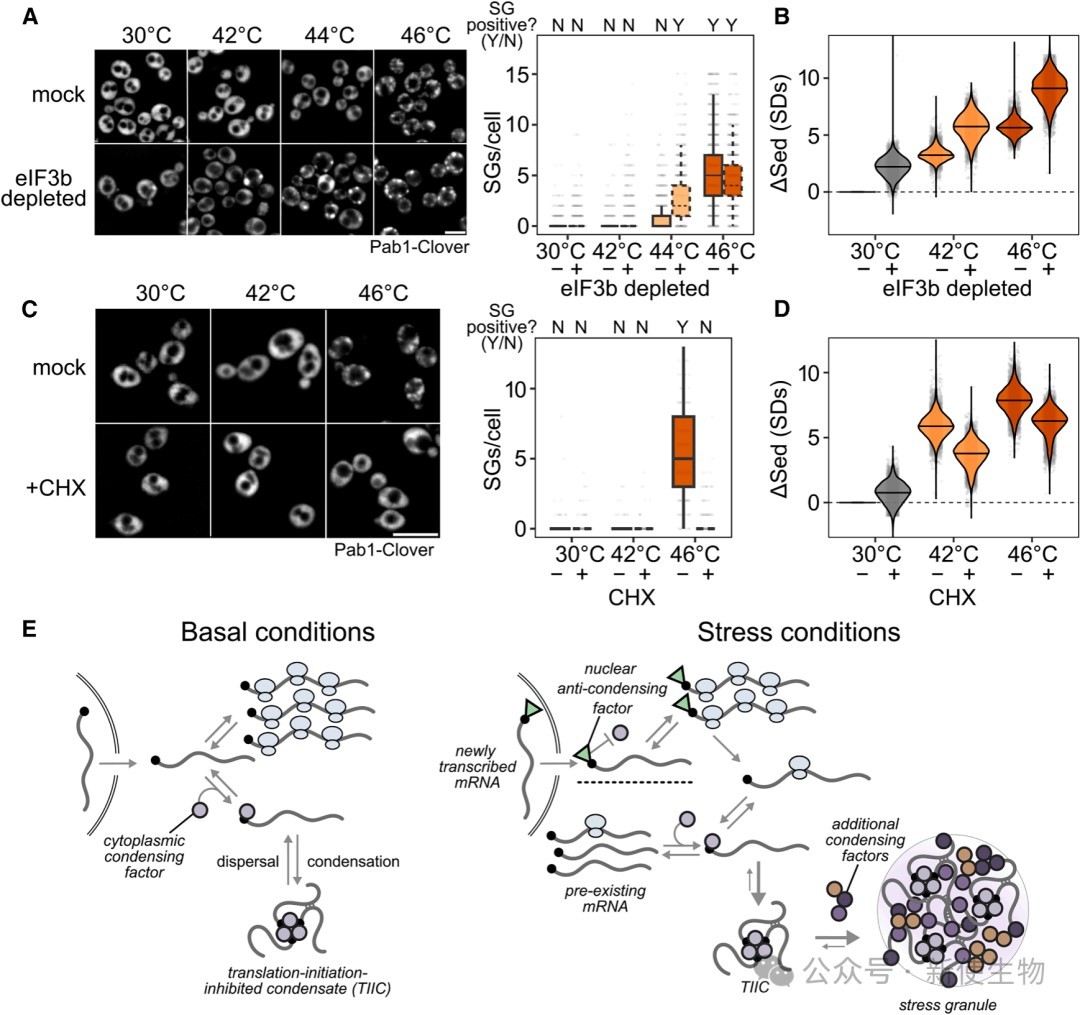
实验表明,单纯耗竭eIF3b导致翻译起始抑制会形成TIICs但不会形成可见的SGs,而在该状态下施加轻微热应激则会迅速诱导SGs形成,说明TIICs的积累促进了SGs的生成。
相反,使用放线菌酮(CHX)锁定翻译延伸虽然能阻止可见SGs的形成,却不能阻止微观尺度上的mRNP凝聚(TIICs),结合5'帽竞争模型。
总结
本研究揭示了mRNP凝聚是一种普遍存在的、与翻译起始抑制紧密相关的细胞现象,它并非只在严重应激下作为SGs的一部分出现。该机制通过隔离旧的mRNA并允许新的mRNA被翻译,为细胞在应激期间重塑其蛋白质组提供了一个高效且具有普适性的调控策略。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们