导读
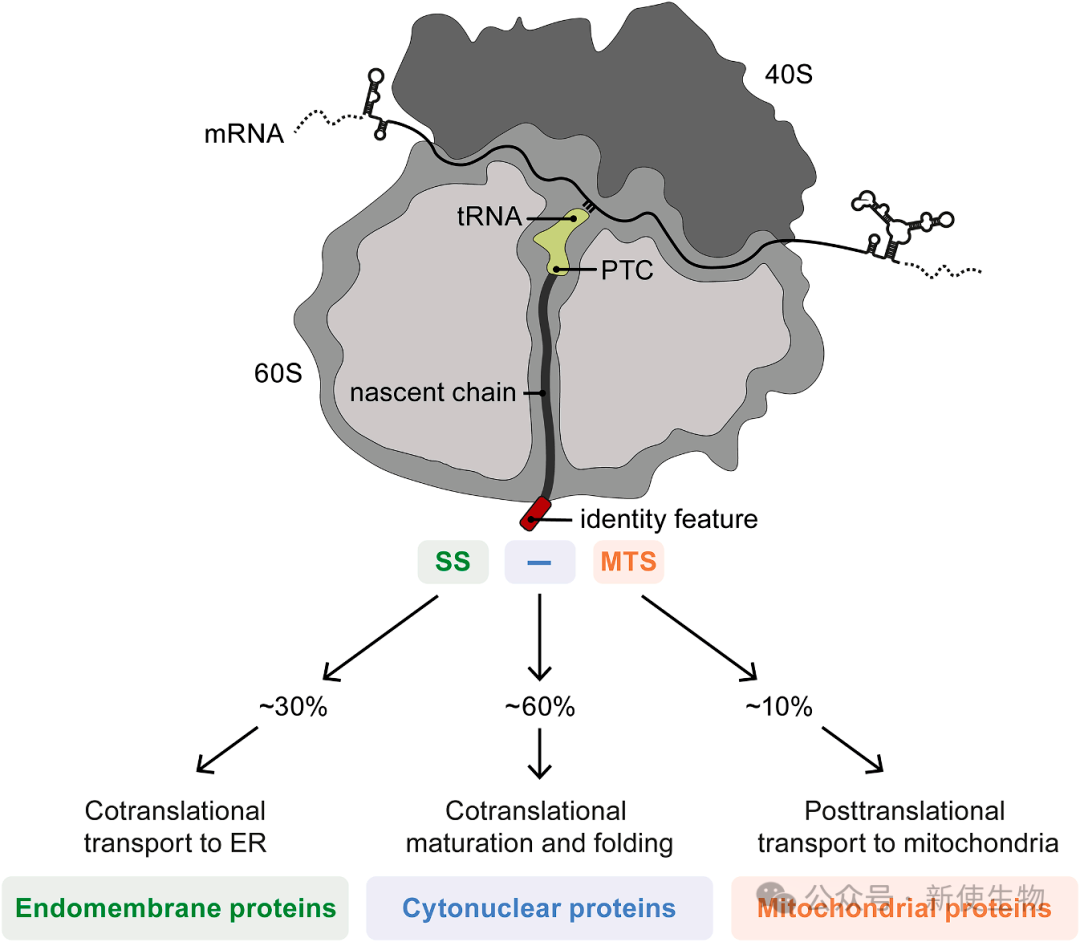
蛋白质的生物合成需要核糖体与多种共翻译因子的协同作用,这些因子共同决定了新生肽链的命运。这一过程必须精准完成,胞质和核蛋白需要立即进行N端成熟和折叠,而靶向内质网(ER)和线粒体的蛋白质则必须维持在未折叠状态以便于转运。
为了协调这些看似矛盾的需求,一个高度选择性的分拣机制在核糖体出口通道处运作。近期研究发现,保守的新生多肽链相关复合物(nascent polypeptide-associated complex, NAC)是这一过程的核心协调者。
2026年2月5日,德国康斯坦茨大学Elke Deuerling团队在Molecular Cell上发表了题为“Ribosome-NAC collaboration: A regulatory platform for cotranslational chaperones, enzymes, and targeting factors”的综述文章。该文系统阐述了NAC如何通过感知新生链上的信号,动态调节其他因子与核糖体的结合,从而将底物引导至正确的成熟或靶向通路,并探讨了NAC作为分子枢纽,如何将共翻译过程组织成高效、有序的蛋白质生物合成路径。

综述整理
一、NAC:新生蛋白的守护者
新生多肽链相关复合物(NAC)是一种在真核生物中普遍保守的异源二聚体,由NACα和NACβ两个亚基组成。
与大多数共翻译因子不同,NAC在细胞中极其丰富,几乎与核糖体等摩尔,并与每一个正在翻译的核糖体结合。其重要性在于,在多细胞生物中敲除NAC会导致胚胎致死。
1.1) NAC的结构与动态结合机制
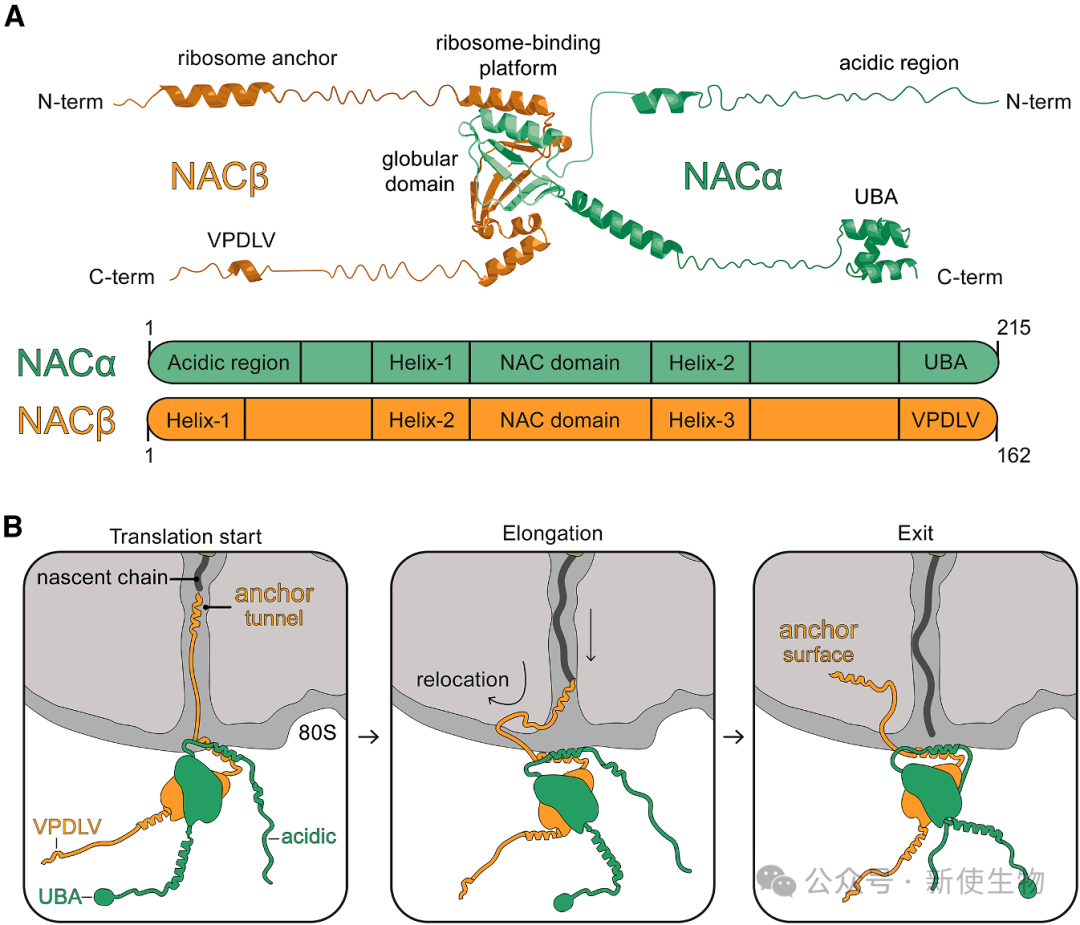
NAC的核心是一个由两个亚基共同形成的球状结构域,从该结构域伸出四个长的、柔性的末端,执行不同的功能。
核糖体锚定: NACβ的N端是主要的核糖体锚点,以高亲和力将NAC栓在核糖体出口通道旁。
动态重排: 在翻译起始时,NACβ的N端会伸入空的出口通道。随着新生肽链的延长,它会被挤出通道,并重新定位到核糖体表面。这一动态过程确保了NAC总是在新生链N端出现的关键时刻就位。
因子招募臂: NAC的两个C端作为柔性手臂,负责招募其他共翻译因子。NACα的C端UBA结构域招募N-乙酰转移酶(如NatA/E)和信号识别颗粒(SRP)。NACβ的C端疏水基序则招募甲硫氨酸氨肽酶(METAP1)和N-肉豆蔻酰转移酶(NMTs)。
通过这种方式,NAC在核糖体出口处局部富集了相关的生物合成机器,为新生肽链的快速、精确加工和分选做好了准备。
二、NAC在胞质蛋白N端修饰中的核心作用
绝大多数(80-90%)的胞质和核蛋白在合成过程中,其N端会经历共翻译修饰,主要包括三类酶的参与:甲硫氨酸氨肽酶(METAPs)、N-乙酰转移酶(NATs)和N-肉豆蔻酰转移酶(NMTs)。
这些修饰必须在新生链刚从核糖体中出来、尚未折叠的短暂窗口期内完成。NAC通过协同招募和组织这些酶,确保了这一过程的高效和有序。
2.1) 甲硫氨酸切除
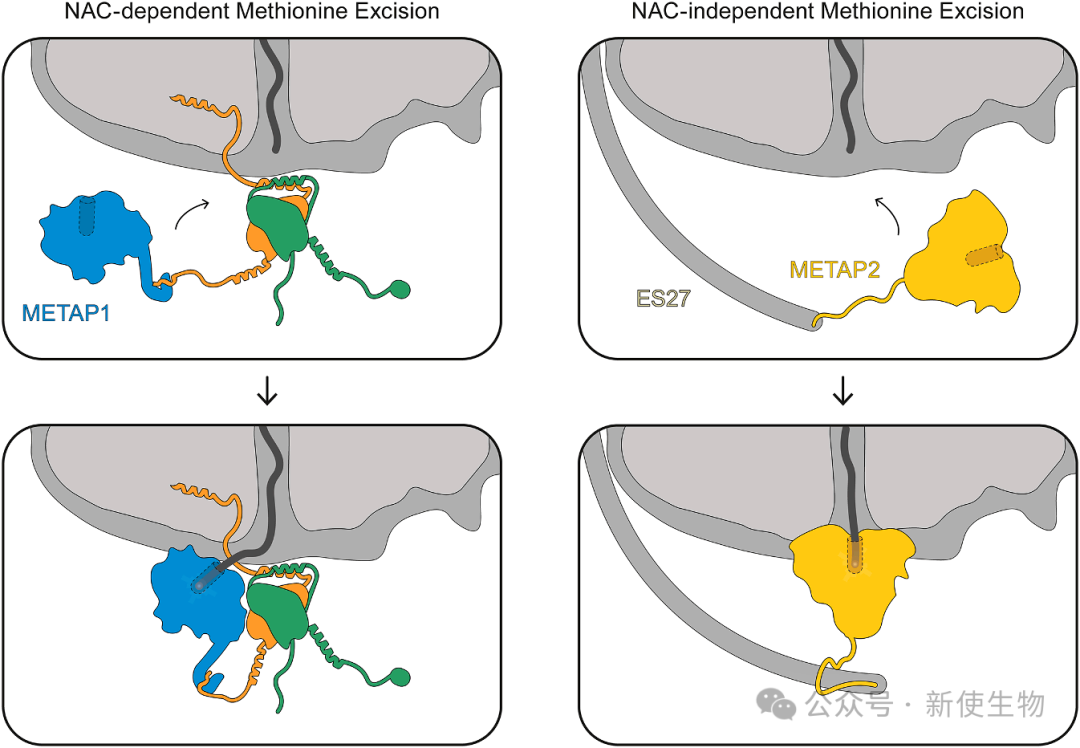
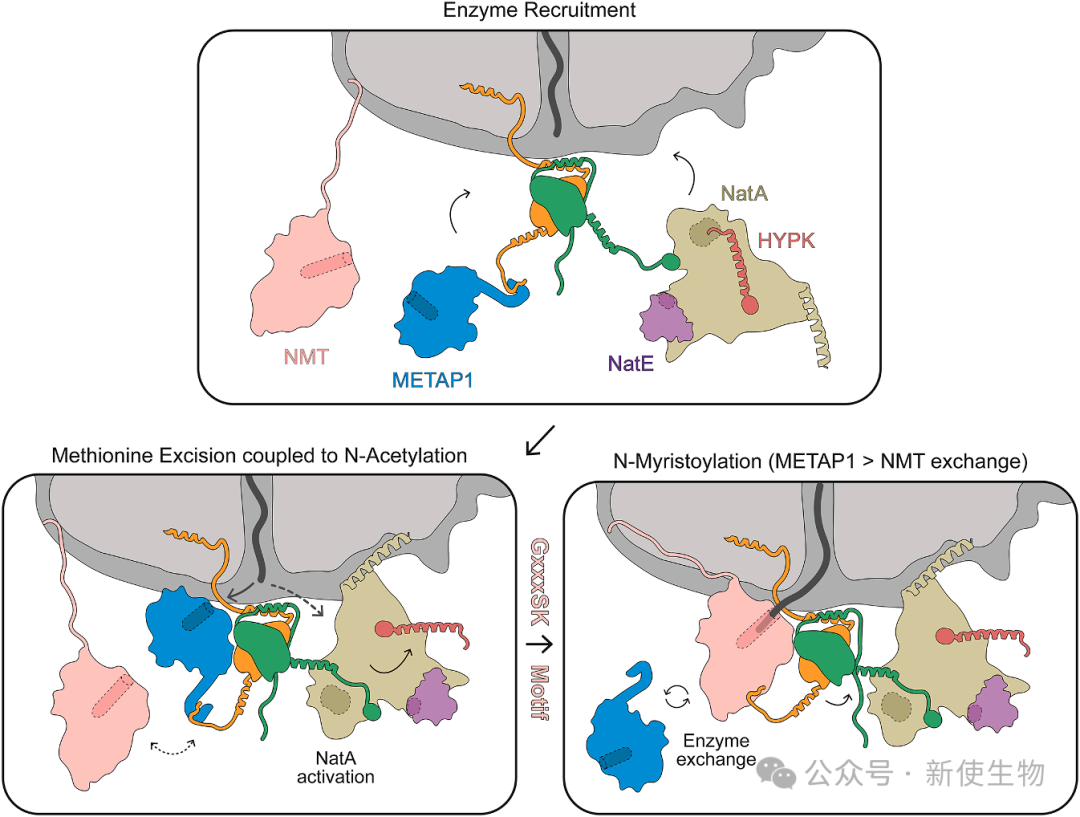
METAP1负责切除起始甲硫氨酸,NAC通过其NACβ的C端臂特异性招募METAP1,并将其精确定位在核糖体出口处。
这种作用使得METAP1的活性位点正对新生链出口,确保了甲硫氨酸在新生链一出现就能被高效切除。而其同源物METAP2则通过一个NAC非依赖的途径,由核糖体RNA的柔性臂ES27招募。
2.2) 蛋白N-乙酰化
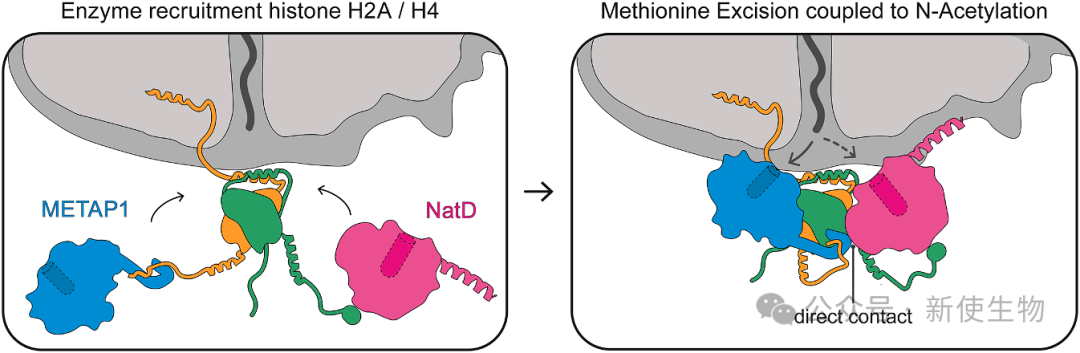
N-乙酰化是最普遍的蛋白修饰之一,NAC能够同时招募METAP1和主要的乙酰转移酶复合物NatA/E。
这两种酶被并排安置在出口通道的两侧,形成一个“多酶复合物”。这种结构确保了甲硫氨酸被切除后,新暴露的N端能被立即、无缝地递送给NatA/E进行乙酰化,将一个随机过程转变为高效的流水线作业。
2.3) 蛋白N-肉豆蔻酰化
N-肉豆蔻酰化是一种脂质修饰,NMTs也通过NACβ的C端臂被招募。
此外,NMTs与METAP1竞争结合同一个NAC位点。这一竞争由新生肽链自身决定,只有当METAP1切除甲硫氨酸并暴露出特定的N端甘氨酸序列后,NMT对核糖体的亲和力才会急剧增加。
三、NAC在内质网(ER)蛋白靶向中的双重角色
与胞质蛋白需要立即折叠和修饰不同,靶向ER的蛋白必须维持未折叠状态,以便被信号识别颗粒(SRP)捕获并递送至ER膜。
3.1) NAC作为ER靶向的拮抗剂
对于正在合成胞质蛋白的核糖体,NAC的球状结构域会占据SRP在核糖体上的结合位点,从而直接阻止SRP的非特异性结合。这种拮抗作用至关重要,因为它防止了胞质蛋白被错误地靶向到ER。
同时,NAC占据的这个位置又恰好是METAP1等修饰酶的停靠平台。因此,NAC在阻止错误靶向的同时,促进了正确的修饰。
3.2) NAC作为ER靶向的协同剂
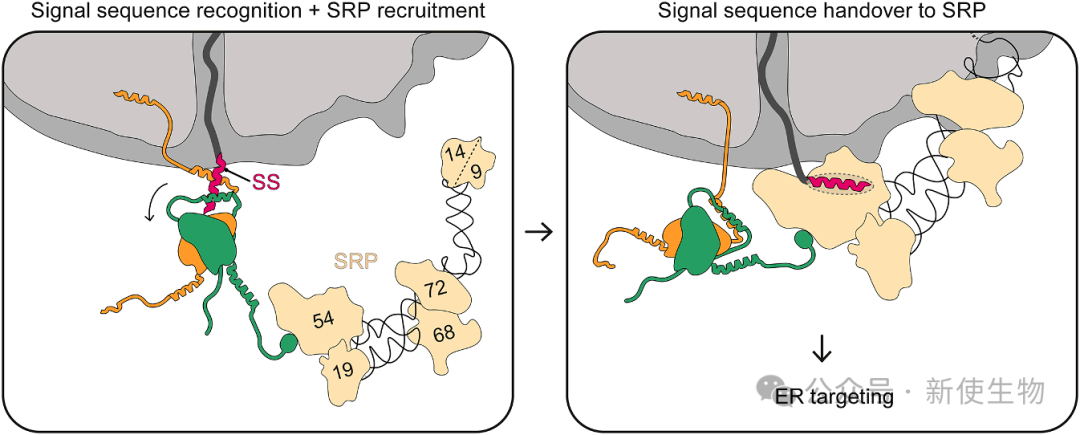
当新生链N端出现疏水的ER信号肽时,该信号肽会与NAC球状结构域下方的一个口袋结合,导致NAC球状结构域从核糖体上脱离,从而暴露了SRP的结合位点。
此时,NAC本身并未离开核糖体,而是通过NACβ的N端锚点继续连接。更重要的是,NAC的角色从抑制者转变为促进者。其NACα的C端臂会直接与SRP结合,稳定SRP与新生链的复合物,高效启动靶向过程。
3.3) NAC介导的核糖体再循环
在ER蛋白翻译和转运完成后,核糖体与ER膜上的Sec61转运通道仍保持高亲和力结合,难以脱离。
此时,NAC再次介入,在翻译终止后,NACβ的N端重新插入空的出口通道,这使得NAC的球状结构域复位到出口处,通过空间位阻挤开Sec61,从而促进核糖体从ER膜上解离和回收,为下一轮翻译做好准备。
四、NAC与线粒体蛋白的共翻译加工
线粒体蛋白的分选机制与内质网截然不同:
翻译后转运:为了不占用有限的线粒体入口,大多数线粒体蛋白合成后才转运。
NAC的构象转换:当线粒体靶向序列(MTS)出现时,NAC会发生构象变化。这种构象既能拮抗SRP(防止误入ER),又不招募修饰酶(防止错误修饰)。
分子伴侣接力:NAC可能协助招募St13/Hip 等共翻译伴侣,使线粒体前体蛋白保持在未折叠且可溶解的状态(Holdase功能),以便后续转运。
总结
NAC是蛋白质生物合成过程中的核心组织者和质量控制者,它的球状结构域会根据新生链的身份信息调控其他因子的进出。其柔性的C端臂则像一个动态枢纽,将各种酶和因子精准地定位在核糖体出口。
未来的研究将进一步揭示这个围绕核糖体的复杂调控网络是如何运作的,包括其他柔性蛋白臂(如来自rRNA或因子本身)如何协同作用,以及mRNA上的顺式元件如何参与其中。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们