导读
人类线粒体核糖体(mitoribosome)负责合成氧化磷酸化(OXPHOS)机器所需的13种线粒体编码蛋白。这一过程受到精细调控,以确保新生肽链能正确折叠并插入线粒体内膜,并与核编码的OXPHOS组分动态组装。
近年来,我们对线粒体翻译的理解正在迅速加深,高分辨率结构研究、线粒体核糖体谱分析等创新方法为揭示其调控网络提供了全面的见解。
然而,抗生素引起的核糖体停滞等问题,既可能在部分个体中引发严重的副作用,也可能在另一些疾病(如癌症)中产生治疗效益,其背后的机制仍有待阐明。
近日,卡罗林斯卡学院Joanna Rorbach与德国哥廷根大学医学中心Ricarda Richter-Dennerlein团队等在Nature Reviews Molecular Cell Biology上发表了题为“Mechanisms and disease relevance of mitochondrial translation in humans”的综述文章。该文系统阐述了人类线粒体翻译的独特机制,包括翻译的起始、延伸、终止,核糖体的生物合成,氧化还原感知,以及线粒体核糖体拯救等质量控制途径,并深入探讨了其在癌症、免疫等疾病中的新兴作用和临床意义。

综述整理
一、线粒体翻译的基本原理
尽管起源于细菌,但人类线粒体翻译系统在进化中经历了巨大的重塑,形成了独特的结构和功能机制。
1.1) 线粒体翻译机器的独特性
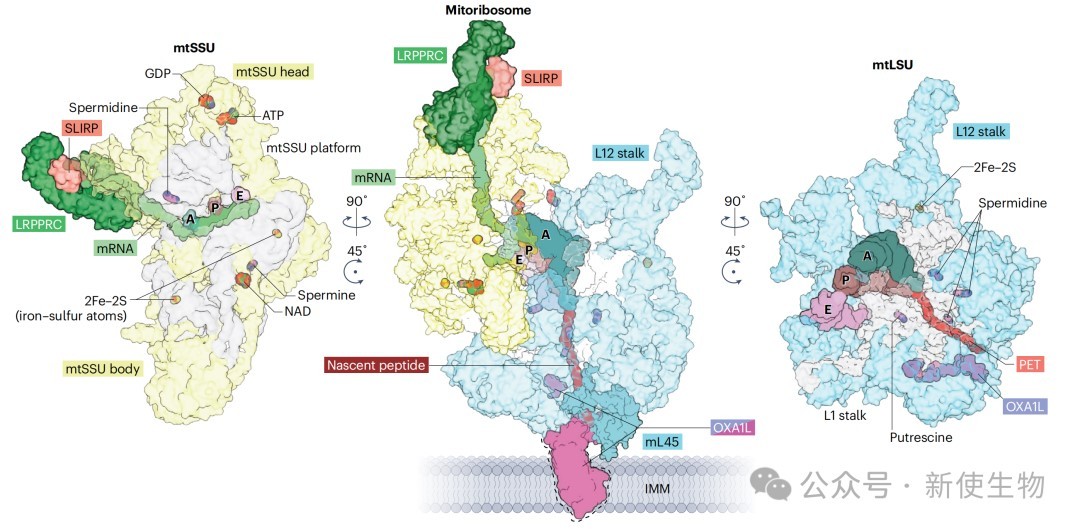
结构重塑: 人类线粒体核糖体是一个55S颗粒,相比于富含rRNA的细菌70S核糖体,其rRNA含量减少,蛋白质质量增加,形成了更为疏松的结构。36种线粒体特异性蛋白的加入,替代了部分丢失的rRNA和细菌来源的核糖体蛋白,重塑了其外围结构。
多肽出口通道(PET) 的适应性: PET具有更强的疏水性,这可能有助于新生肽链在疏水环境中正确折叠,并减慢翻译速度,为跨膜结构域的共翻译插入提供充足时间。核糖体蛋白mL45负责将线粒体核糖体锚定在线粒体内膜(IMM)上,并与插入酶OXA1L协同,实现新生肽链的共翻译插入。
铁硫簇(Fe-S) 的新功能: 线粒体大小亚基中均含有铁硫簇。这些结构不仅起到稳定核糖体结构的作用,还可能作为氧化还原传感器,使线粒体翻译能够响应细胞的氧化应激状态。
mRNA入口通道的改变: 由于缺少uS4等蛋白,mRNA入口通道被重塑。这要求线粒体mRNA在进入核糖体前必须是单链形式,这一过程由LRPPRC-SLIRP等蛋白复合物辅助完成。
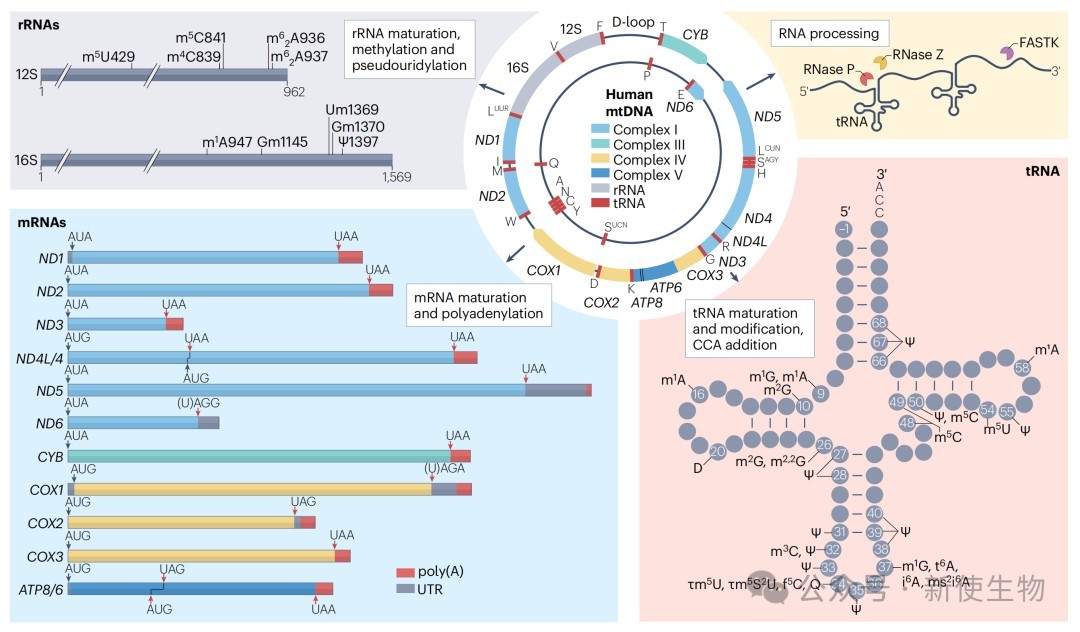
1.2) 翻译过程
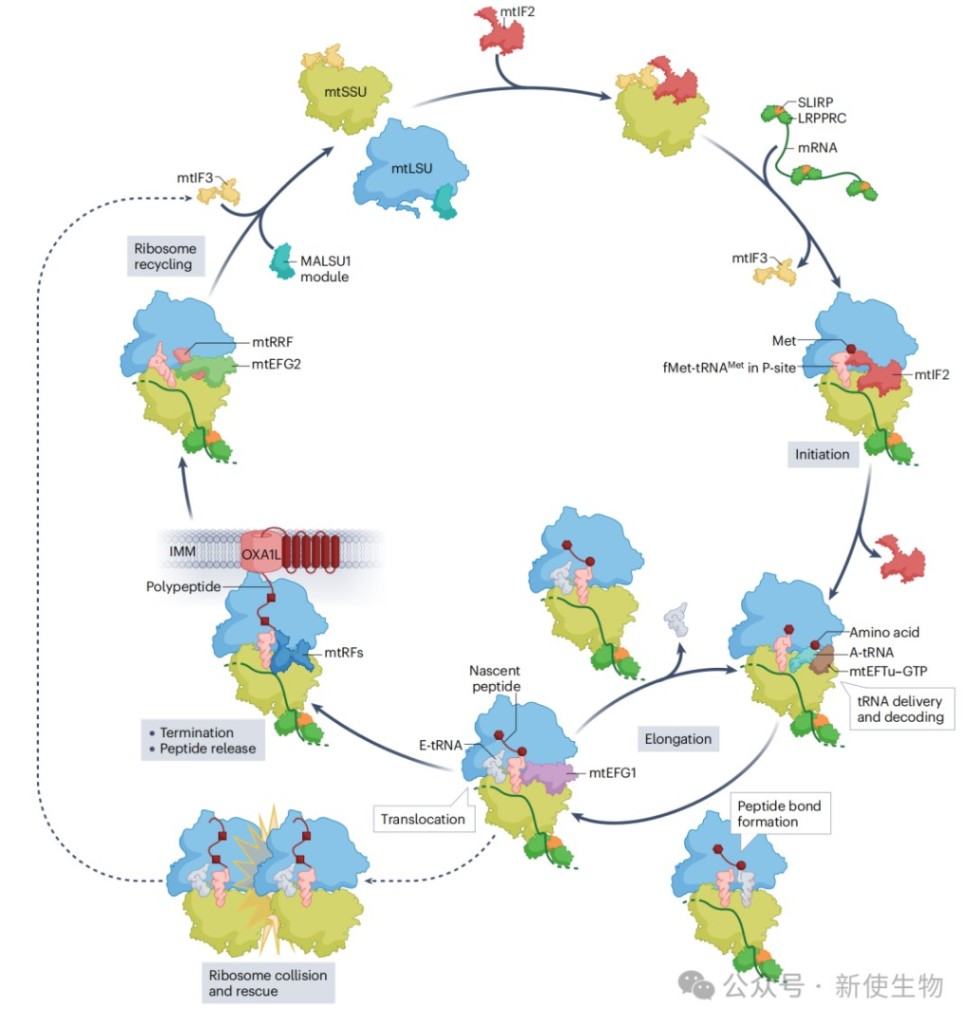
起始(Initiation): 线粒体mRNA是无引导序列 (leaderless)的,其起始机制与细菌不同。mtIF2负责递送起始tRNA(fMet-tRNA),而mtIF3则作为质量控制因子,防止未成熟的小亚基过早与大亚基结合。翻译起始可能直接在完整的55S核糖体上发生。
延伸(Elongation): 延伸过程相对保守。mtEFTu负责递送氨酰-tRNA至A位点,mtEFG1则催化核糖体沿mRNA的易位。
终止与回收(Termination and Recycling): 线粒体使用了独特的遗传密码,其中AGA和AGG被重新指定为终止密码子。mtRF1负责识别这两种非经典终止密码子,而mtRF1a则识别经典的UAA和UAG。翻译完成后,mtRRF和mtEFG2协同作用,促使核糖体大小亚基解离,完成回收。
1.3) 线粒体翻译的调控
线粒体翻译受到多层次的精细调控,以确保与核基因编码的蛋白协同组装。
与核糖体生物合成的偶联: mtIF3等因子既参与翻译起始,也参与小亚基的晚期成熟,从而将核糖体的制造与使用联系起来,确保只有功能完整的核糖体才能进入翻译循环。
mRNA成熟与折叠的作用: mRNA的二级结构可以调控翻译速度。例如,在翻译ATP8-ATP6这个双顺反子mRNA时,其重叠区域的茎环结构能诱导程序性核糖体移码,导致ATP8翻译提前终止,从而使核糖体能够重新起始ATP6的翻译。
翻译可塑性: 线粒体蛋白的合成速率受到核编码亚基可用性的调控。最典型的例子是COX1的合成,其翻译效率依赖于核编码的COX4亚基的输入。如果COX4供应不足,COX1的翻译就会减慢或暂停,避免了未组装蛋白的过度积累。
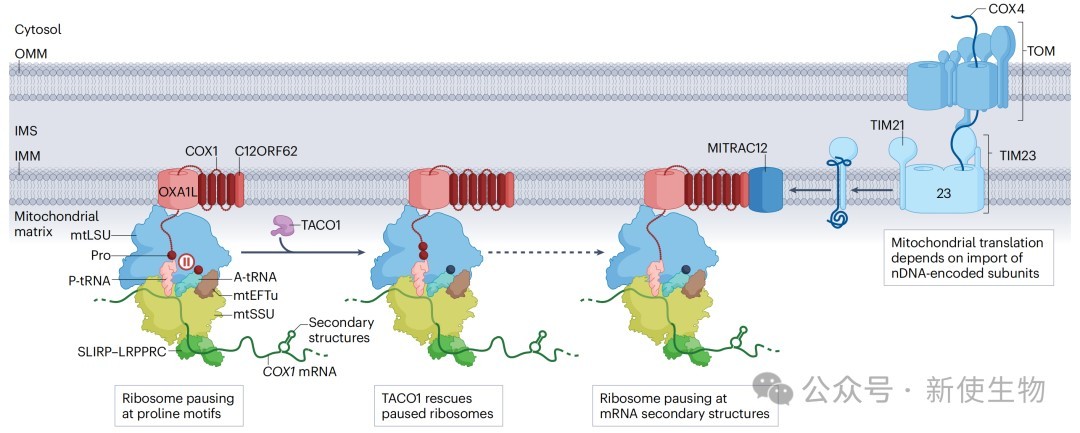
二、线粒体核糖体暂停与停滞
核糖体暂停是翻译过程中的一种生理现象,有助于新生肽链的共翻译折叠。然而,异常的、不可逆的停滞则会触发细胞的质量控制和拯救机制。
2.1) 生理性与病理性停滞的诱因
生理性暂停:连续的脯氨酸会因其刚性结构导致核糖体暂停。TACO1蛋白被发现是解决这一问题的关键因子,它能帮助核糖体跨越脯氨酸“减速带”。TACO1基因突变会导致COX1(富含脯氨酸)合成障碍,引发Leigh综合征。
病理性停滞:由异常事件触发,需要被清除。
i. No-go停滞:由mRNA损伤或异常tRNA修饰引起,导致核糖体卡在转录本中间。
ii. Non-stop停滞:当核糖体翻译到mRNA末端却没有遇到终止密码子时发生。
iii. 疾病关联:在MELAS综合征患者(携带m.3243A>G tRNA突变)的细胞中,观察到核糖体在特定密码子上的“排队”现象。
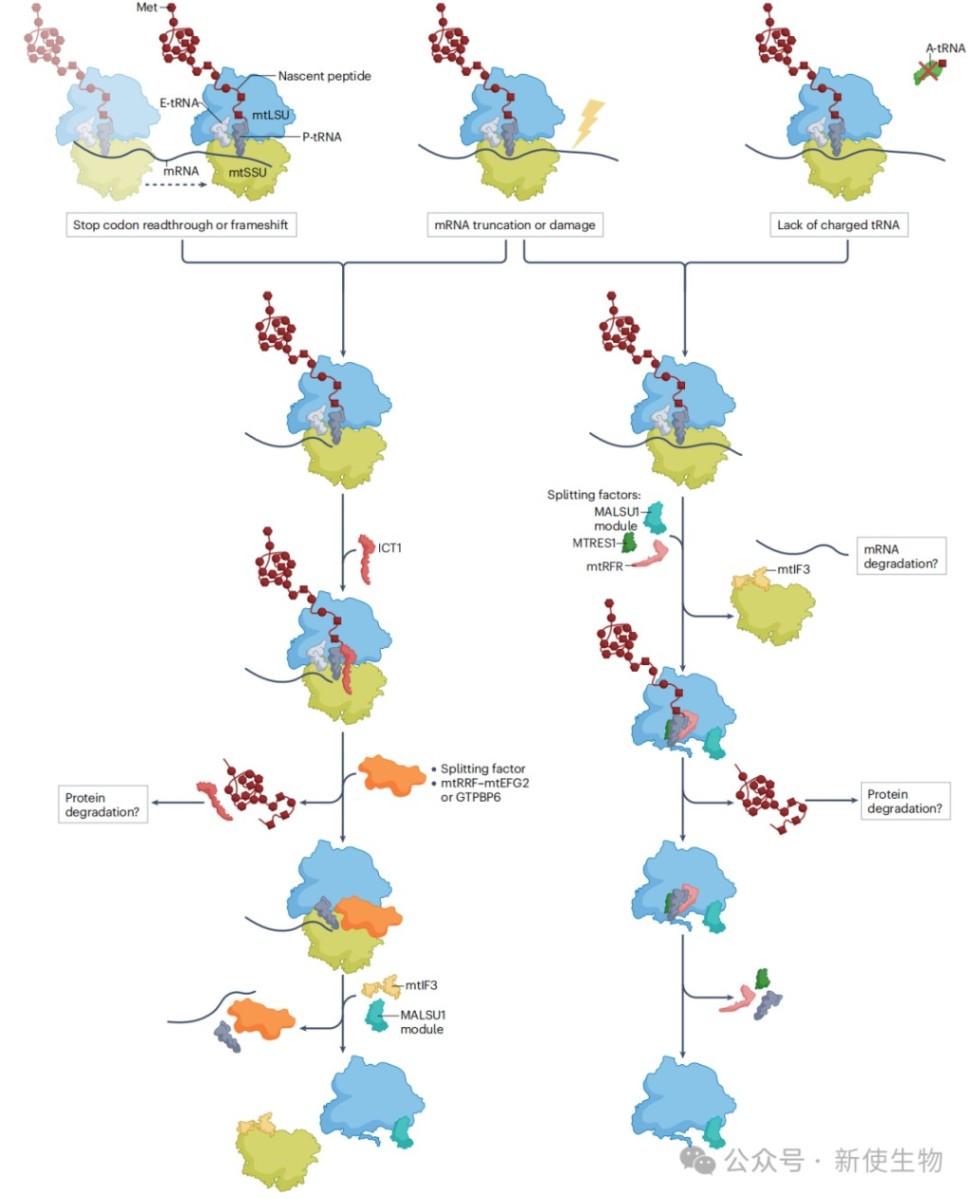
2.2) 质量控制与拯救机制
近期研究揭示了多个蛋白参与的线粒体核糖体拯救通路。
ICT1通路:ICT1是大亚基的组成部分,但它也能识别并结合在“non-stop”停滞核糖体的空A位点上,水解新生肽链,释放被困的核糖体。
mtRFR与mtRQC通路:该通路处理“no-go”等中途停滞的核糖体。当停滞的核糖体被某个未知因子分裂后,mtRFR与MTRES1会结合到保留着新生肽链的大亚基上,水解肽链,完成拯救。这被称为线粒体核糖体相关质量控制 (mtRQC)。它与细菌机制的关键区别在于不发生CAT尾化。
其他辅助因子:
i. mtEF4:通过减慢翻译速度来维持蛋白质质量,其缺失会导致蛋白质不稳定和雄性不育。
ii. TMEM126A:与OXA1L协同作用,当蛋白插入过程受阻时,它会触发对堵塞的插入酶和底物的蛋白酶降解,保护线粒体内膜的完整性。
三、线粒体翻译与人类疾病
线粒体翻译的失调与多种人类疾病密切相关,包括遗传病、癌症和免疫功能异常。
3.1) 线粒体翻译缺陷导致的人类疾病
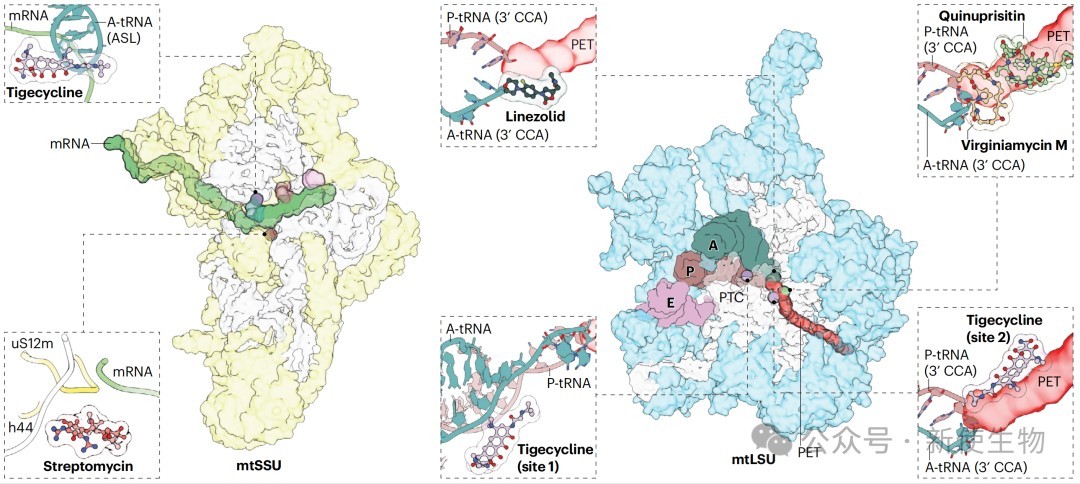
遗传性线粒体疾病常由参与翻译过程的基因突变引起,如mt-tRNA、tRNA合成酶和核糖体蛋白的突变。此外,某些常用抗生素由于其与细菌核糖体的同源性,也会抑制线粒体翻译,产生“脱靶”毒性。
抗生素的副作用与治疗潜力:
i. 副作用: 链霉素在特定12S rRNA突变个体中可导致耳聋;利奈唑胺可引起严重代谢副作用。
ii. 治疗潜力: 四环素类抗生素在某些线粒体病模型(如Leigh综合征)中显示出有益效果,可能是通过诱导线粒体应激(mitohormesis)的适应性反应。
3.2) 线粒体翻译在癌症中的作用
许多癌细胞依赖OXPHOS获取能量,因此抑制线粒体翻译成为一种新兴的抗癌策略。
靶向治疗: 替加环素(一种四环素类抗生素)等药物已在慢性髓系白血病等临床试验中显示出抗肿瘤活性。
代谢重塑: NSUN3等tRNA修饰酶通过影响翻译效率,调控癌细胞在糖酵解和OXPHOS之间的切换,其缺失能显著抑制肿瘤转移。
3.3) 线粒体翻译在免疫应答中的调控作用
免疫细胞的激活、增殖和分化需要大量的能量,高度依赖线粒体功能。
先天免疫: 线粒体翻译的副产物N-甲酰化多肽,可作为一种损伤相关分子模式(DAMPs)被先天免疫细胞识别,从而驱动炎症反应。
适应性免疫: CD8+ T细胞的持续杀伤活性、B细胞的抗体亲和力成熟等过程,均需要线粒体翻译和OXPHOS的支持。
免疫调控: 抑制线粒体翻译的药物(如利奈唑胺)已被证明能缓解自身免疫性疾病模型(如多发性硬化症)的症状,表明线粒体翻译是免疫调节的一个重要靶点。
总结与展望
近年来,我们对线粒体翻译的理解取得了长足进步,但仍有许多未解之谜。未来的研究重点包括:
1. 高分辨率原位成像: 利用原位冷冻电镜断层成像(in situ cryo-ET)等技术,在细胞内观察线粒体核糖体的真实工作状态及其与线粒体内膜的相互作用。
2. 功能异质性研究: 探索是否存在针对特定mRNA的特化线粒体核糖体,以及在不同组织和细胞状态下,线粒体翻译是如何被选择性调控的。
3. 疾病模型与治疗: 结合mtDNA编辑等基因工程技术,深入研究翻译缺陷的致病机理,并开发靶向线粒体翻译的新型小分子药物或基因疗法。
随着我们对线粒体翻译机制的深入了解,靶向这一核心生命过程有望为癌症、免疫疾病和遗传性线粒体病等多种重大疾病提供全新的治疗策略。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们