导读
配子发生是生物有性生殖的核心过程,涉及生殖细胞向成熟卵母细胞的复杂分化。在果蝇卵巢发育中,生殖干细胞通过不对称分裂产生囊胚,随后经历多次不完全有丝分裂形成16细胞囊胚。
在此过程中,细胞必须完成从生殖细胞特异性转录程序向母体转录程序的关键转换。这一转换过程伴随着生殖细胞基因的异染色质化沉默,以确保卵母细胞命运的稳固建立。
然而,驱动这种转录状态转换的翻译调控机制及其与染色质重塑的协同关系尚不明确。此外,雷帕霉素靶蛋白复合物1(TORC1)作为营养与生长信号的枢纽,其在卵母细胞特异化过程中的动态调控作用及其对下游基因表达的影响仍有待深入研究。
2026年1月26日,西奈山艾卡恩医学院的Prashanth Rangan 团队在 The EMBO Journal上发表了题为“TORC1-dependent translation drives chromatin remodeling during the germ-cell-to-maternal transition in Drosophila”的研究论文。该研究发现,在果蝇卵子发生过程中,TORC1信号通路依赖的翻译活动激增,这驱动了关键的染色质重塑过程,从而确保生殖细胞基因被沉默并完成向母源程序的转变。

文章索引
【标题】TORC1-dependent translation drives chromatin remodeling during the germ-cell-to-maternal transition in Drosophila
【发表期刊】The EMBO Journal
【发表日期】2026年1月26日
【作者及团队】美国西奈山艾卡恩医学院Prashanth Rangan团队
【IF】8.3
研究结果
一、核糖体生物发生和TORC1活性是沉默生殖细胞基因的必要条件
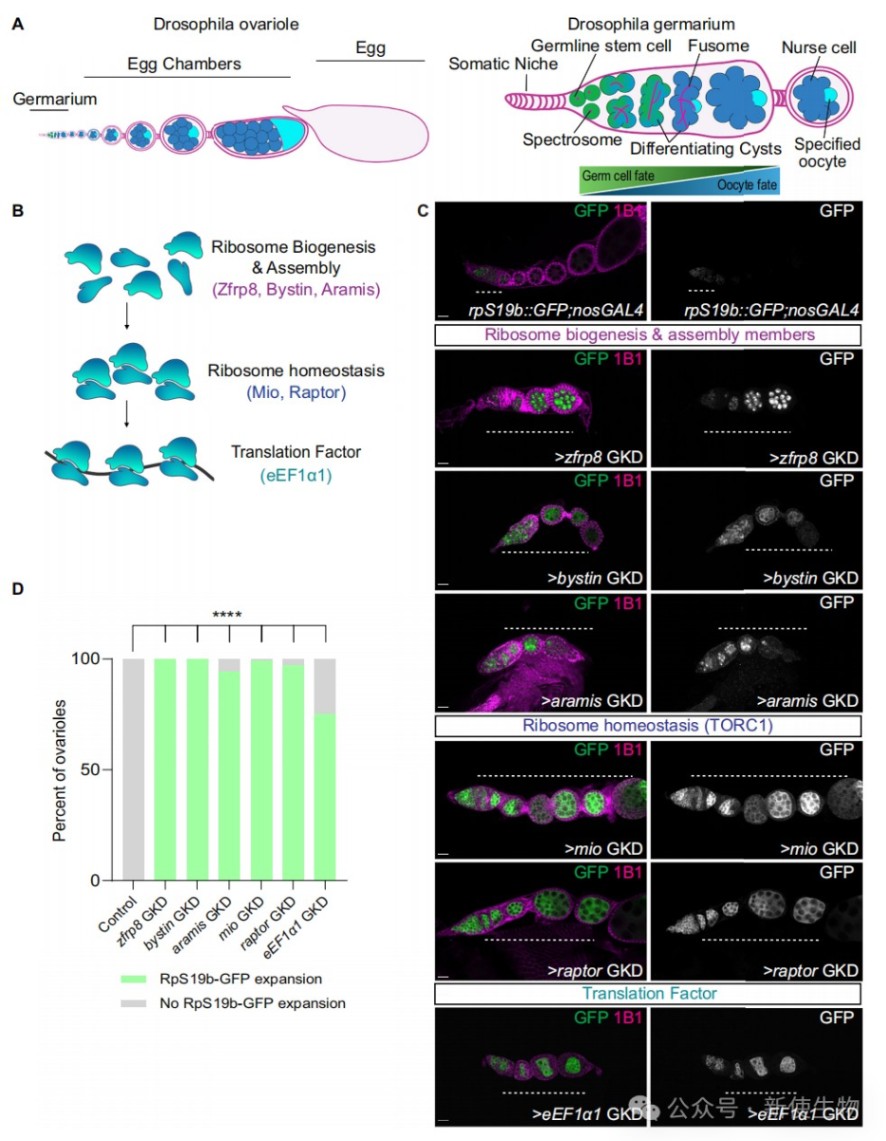
研究人员通过RNAi技术在果蝇生殖系中敲降核糖体生物发生、TORC1通路及翻译延伸因子等相关基因。
结果发现,这些基因的缺失导致生殖细胞基因报告分子rpS19b::GFP和Blanks在分化的卵室中异常表达,表明翻译相关过程对于启动生殖细胞基因的沉默至关重要。
二、翻译支持组件广泛调控生殖细胞基因的表达程序
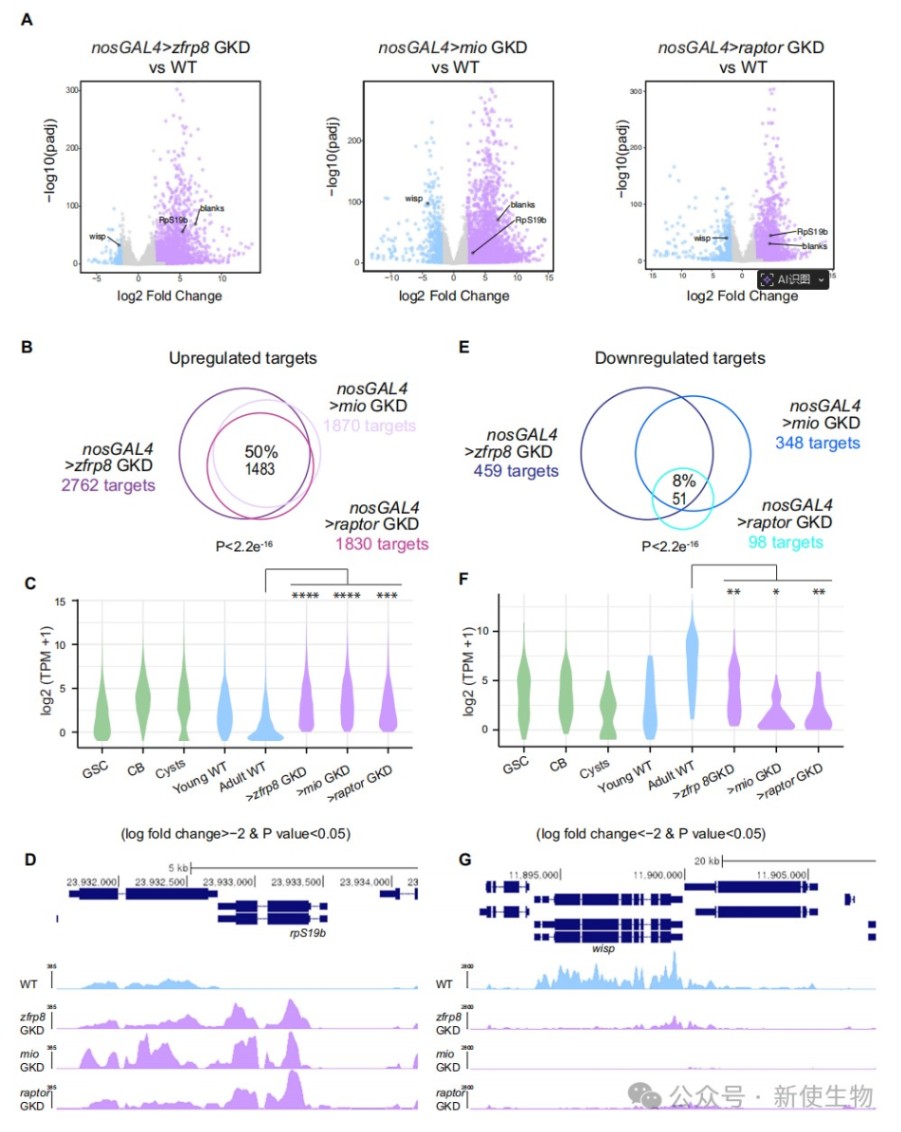
通过对zfrp8、mio和raptor敲降后的卵巢进行RNA-seq分析,研究发现大量通常在未分化阶段表达的生殖细胞基因被错误地上调。
同时,一小部分在分化卵室中高表达的母源基因(如wispy)则被下调,证明核糖体和TORC1活性是协调生殖细胞-母源基因表达程序转换所必需的。
三、翻译调控与异染色质机制共同作用于基因沉默
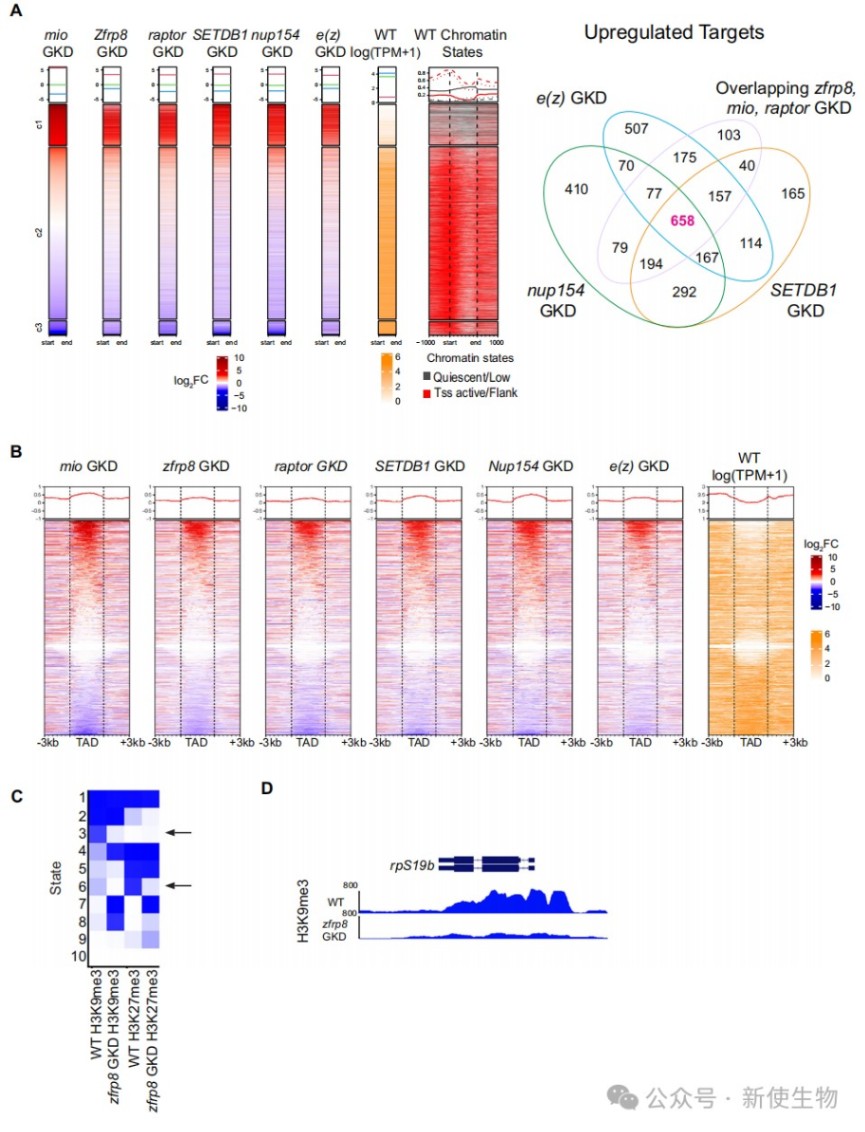
将本研究的RNA-seq数据与已发表的异染色质调节因子敲降数据进行比较,发现它们共同调控一个核心的生殖细胞基因群。
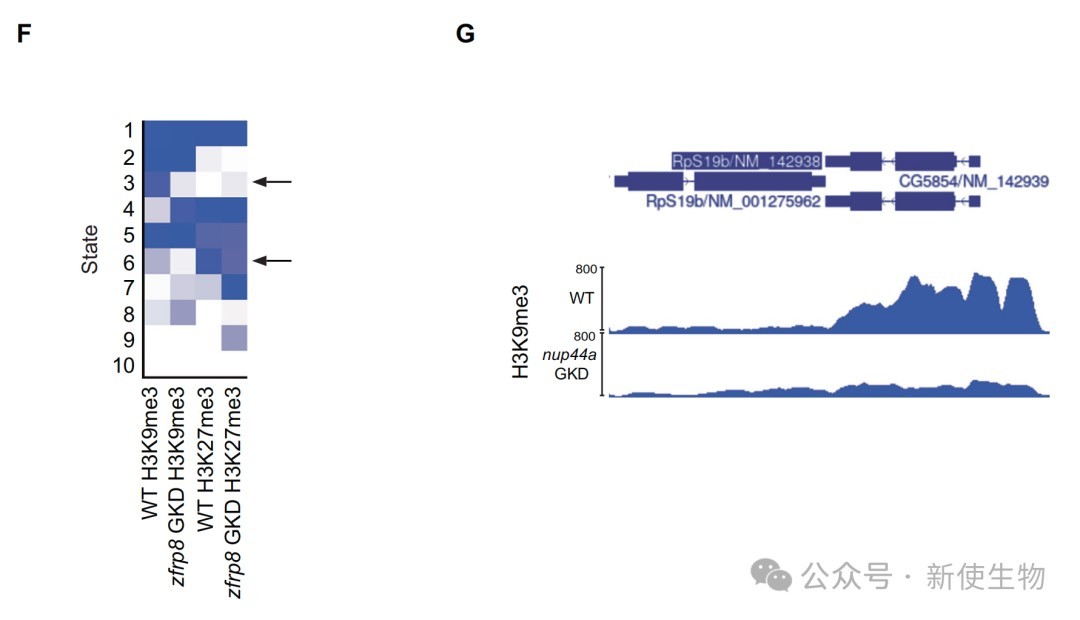
进一步通过CUT&RUN技术检测发现,在zfrp8敲降的卵巢中,一些基因(如rpS19b)启动子区域的异染色质标记H3K9me3显著减少,表明翻译水平的降低损害了异染色质的维持。
四、核糖体生物发生促进核孔复合物组分Nup44A的翻译
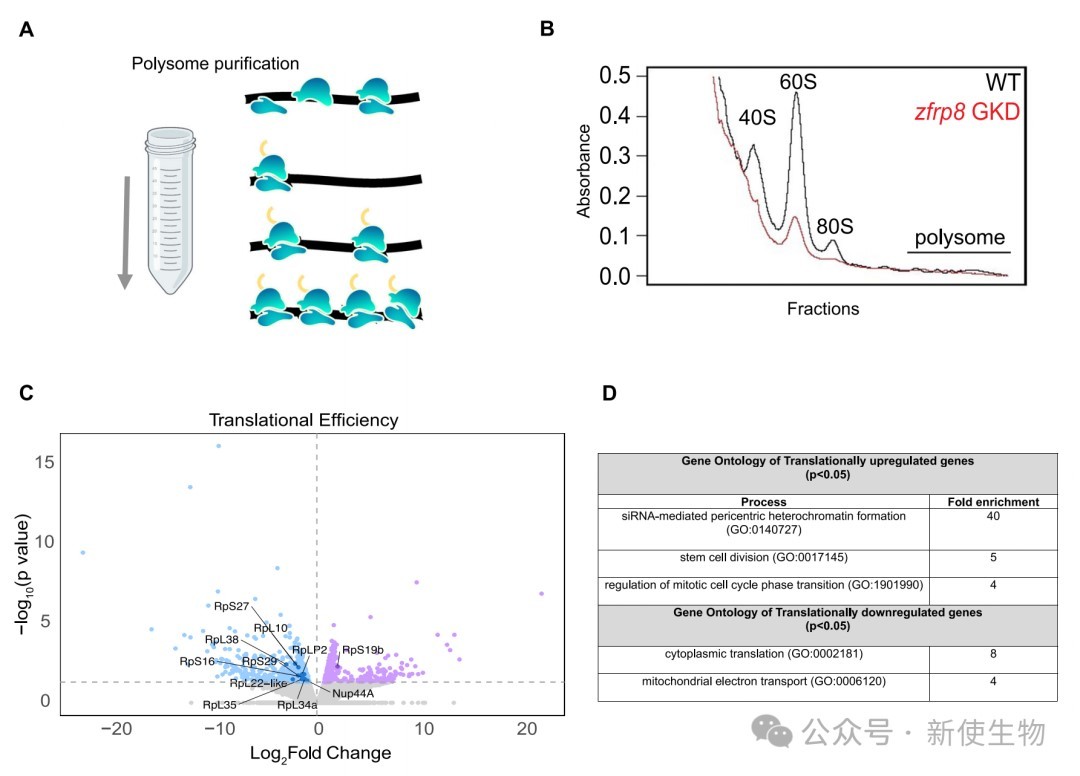
为了探究翻译如何影响染色质,研究人员对zfrp8敲降的卵巢进行了Polysome-seq多聚核糖体测序。
结果显示,敲降zfrp8导致翻译效率普遍失调,其中核孔复合物(NPC)的关键组分Nup44A的翻译被显著下调,暗示翻译通过调控NPC的合成来影响细胞核结构和基因表达。
五、Nup44A是介导生殖细胞基因沉默和染色质稳定的关键因子
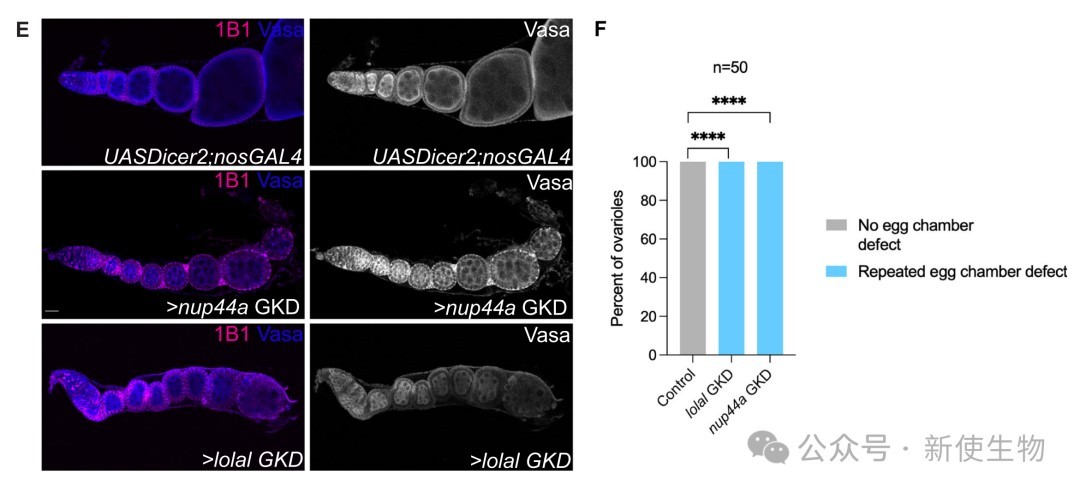
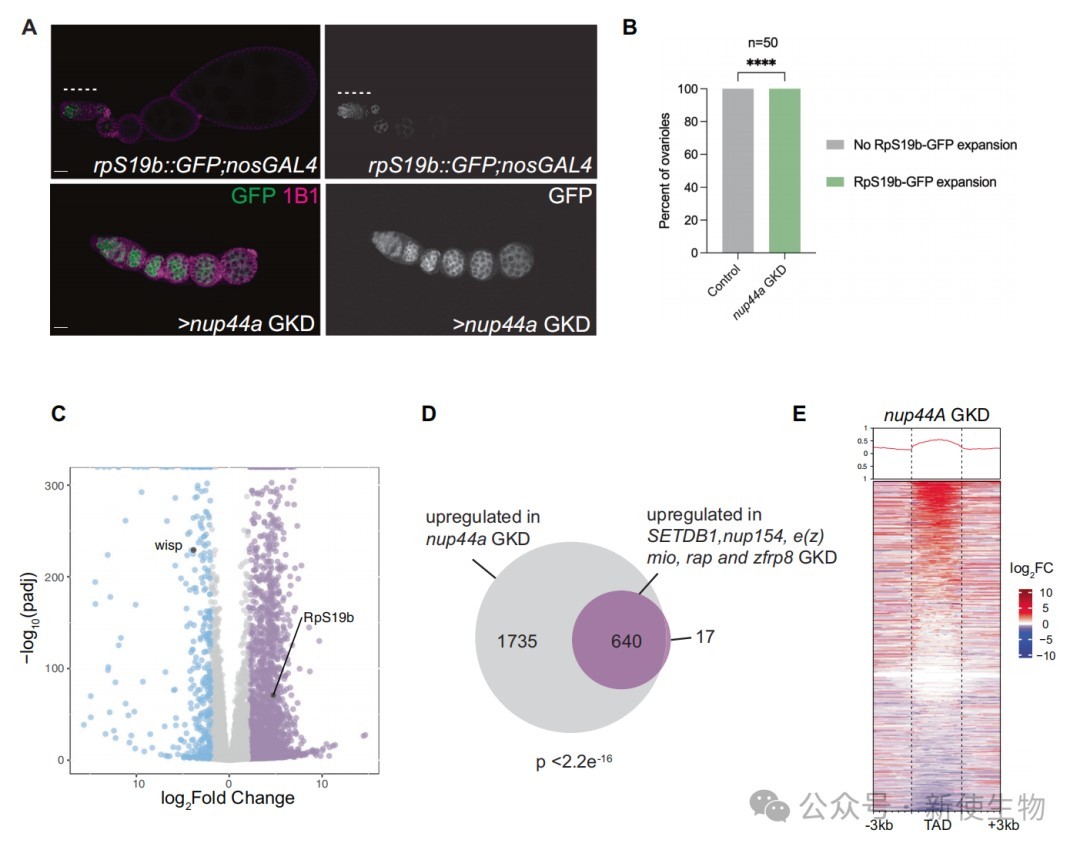
研究人员通过RNAi敲降Nup44A,发现其表型与核糖体或TORC1因子敲降高度一致,均表现出生殖细胞基因的异位表达和染色质标记的丢失。
数据分析表明,Nup44A调控的基因群与翻译和异染色质调节因子调控的基因群高度重合,证实Nup44A是连接翻译与染色质调控的关键枢纽。
六、Nup44A通过前馈环路整合TORC1信号与核糖体生物发生
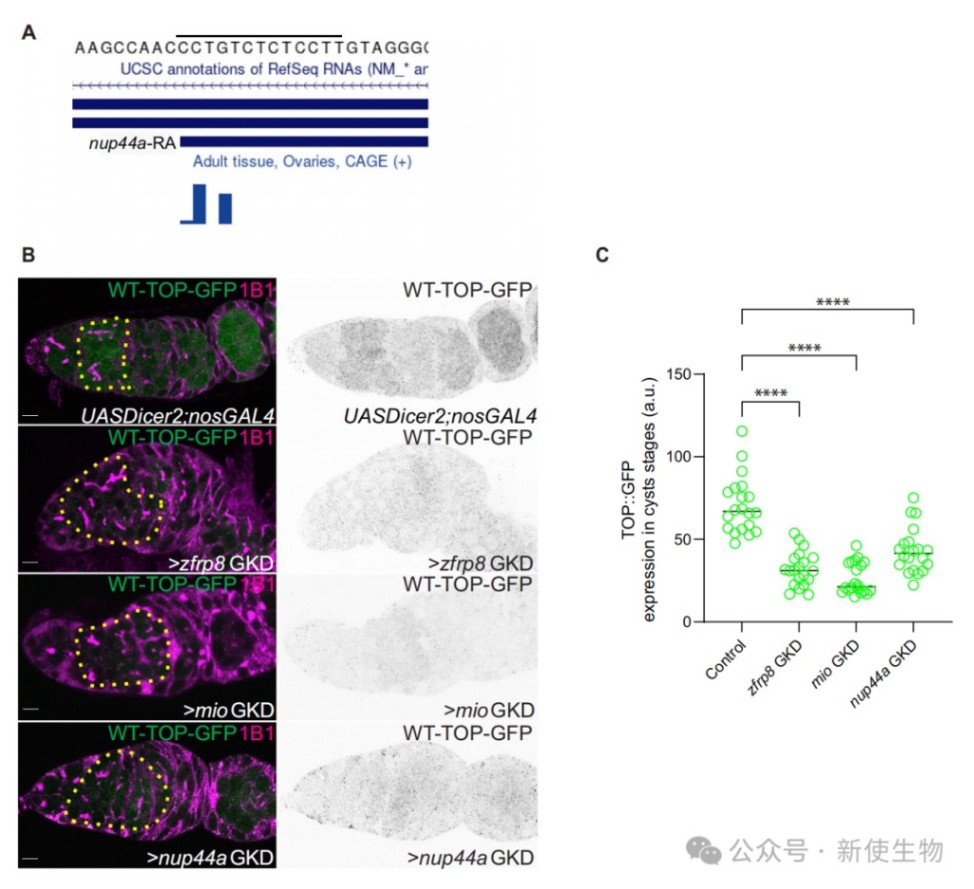
通过序列分析发现Nup44A的mRNA含有一个TOP序列,这类mRNA的翻译对TORC1信号敏感。
实验证明,当zfrp8、mio或Nup44A自身被敲降时,TOP报告基因的翻译水平均显著下降。
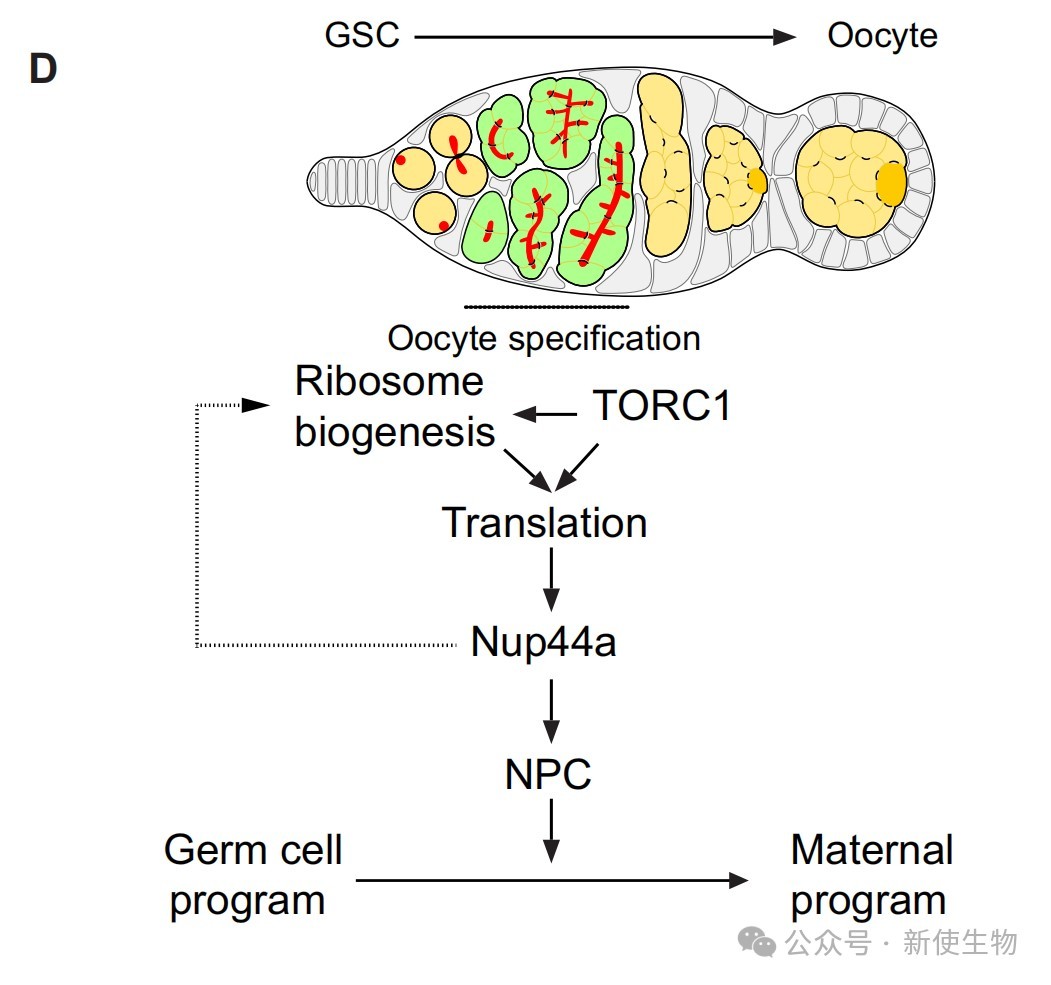
这表明Zfrp8和TORC1通过促进TOP依赖的翻译来合成Nup44A,而Nup44A自身又能反馈调节TORC1信号,形成一个前馈放大环路,共同驱动卵子发生。
总结
该研究揭示了在果蝇卵子发生过程中,一个由翻译驱动的染色质重塑程序对于细胞命运的正确转变至关重要。研究证明,TORC1通路激活后增强的翻译活动,特别是对核孔蛋白Nup44A的翻译,是建立和维持异染色质状态以沉默生殖细胞基因的关键,从而确保了从生殖细胞向卵母细胞的不可逆转变。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们