导读
肺癌是全球最常见且致死率最高的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占绝大多数病例。尽管治疗方法取得了显著进展,但NSCLC患者的五年生存率仍然很低,因此迫切需要阐明其发病机制并寻找新的治疗靶点。
病理学研究早已发现,癌细胞的恶性程度与其细胞核仁形态的改变(如核仁增大或形态不规则)密切相关。核仁是细胞内合成核糖体的主要场所,这一过程对于满足肿瘤细胞旺盛的蛋白质合成需求至关重要。
核糖体DNA(rDNA)转录成pre-45S rRNA是核糖体生物合成的限速步骤,其异常上调与多种癌症的发生发展有关。然而,驱动NSCLC中rDNA转录上调的具体分子机制仍不完全清楚。
2025年9月1日,Journal of Biological Chemistry上线了一篇题为“Nucleolar protein DCAF13 promotes non–small cell lung cancer cell proliferation via facilitating rDNA transcription and ribosome biogenesis”的论文。该研究发现核仁蛋白DCAF13在非小细胞肺癌中高表达,并通过与RNA聚合酶I转录机器的关键组分TAF1A相互作用,促进rDNA转录和核糖体生物合成,从而驱动癌细胞增殖。

文章索引
【标题】Nucleolar protein DCAF13 promotes non–small cell lung cancer cell proliferation via facilitating rDNA transcription and ribosome biogenesis
【发表期刊】Journal of Biological Chemistry
【发表日期】2025年9月1日
【IF】8.2
研究结果
一、Pre-45S rRNA在非小细胞肺癌中高表达
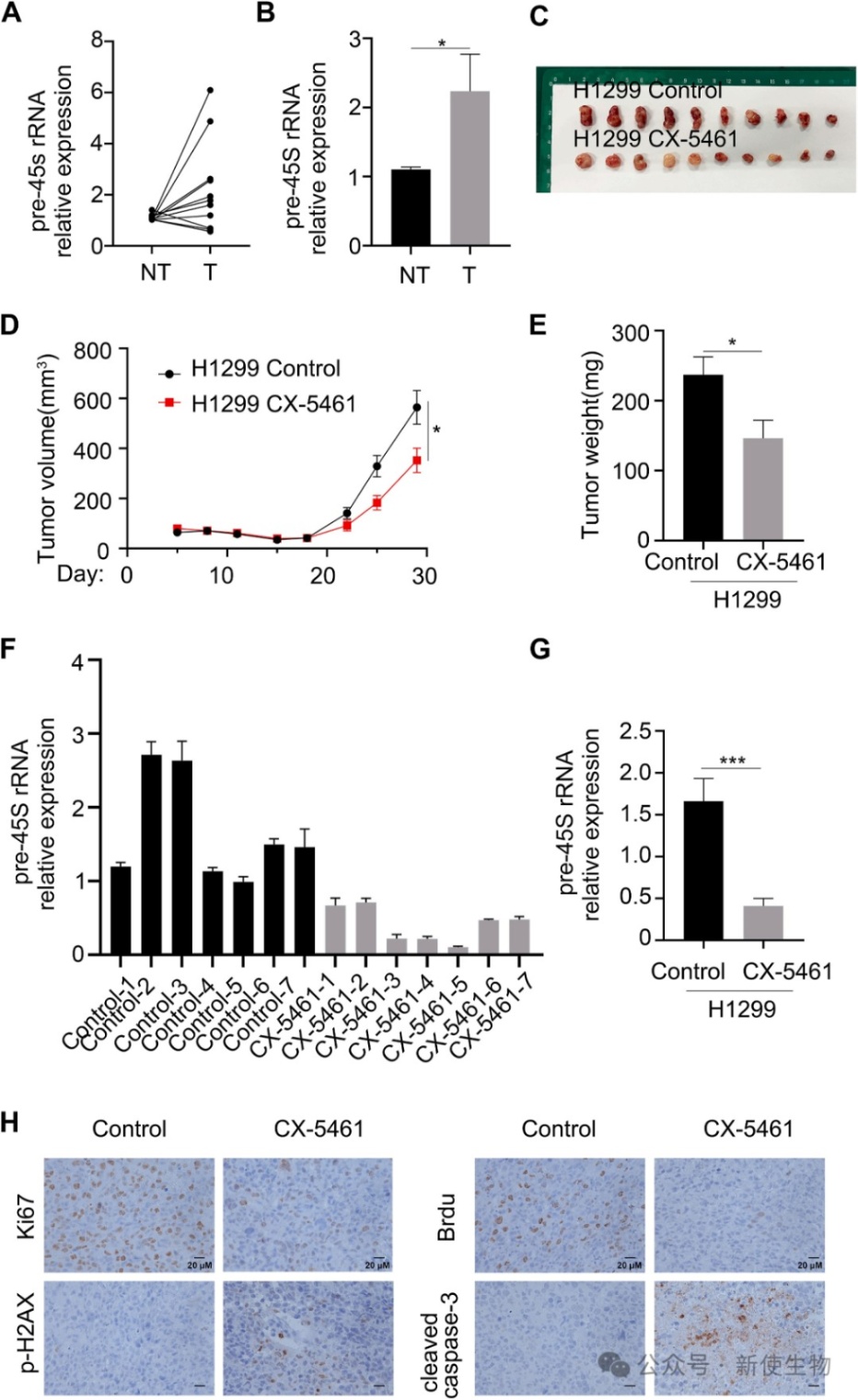
通过对临床样本的分析,研究人员发现NSCLC肿瘤组织中的pre-45S rRNA水平显著高于癌旁正常组织。
在荷瘤小鼠模型中,使用rDNA转录抑制剂CX-5461能够有效抑制肿瘤生长,表明rDNA转录对NSCLC的增殖至关重要。
二、抑制pre-45S rRNA的表达可降低非小细胞肺癌细胞的生长
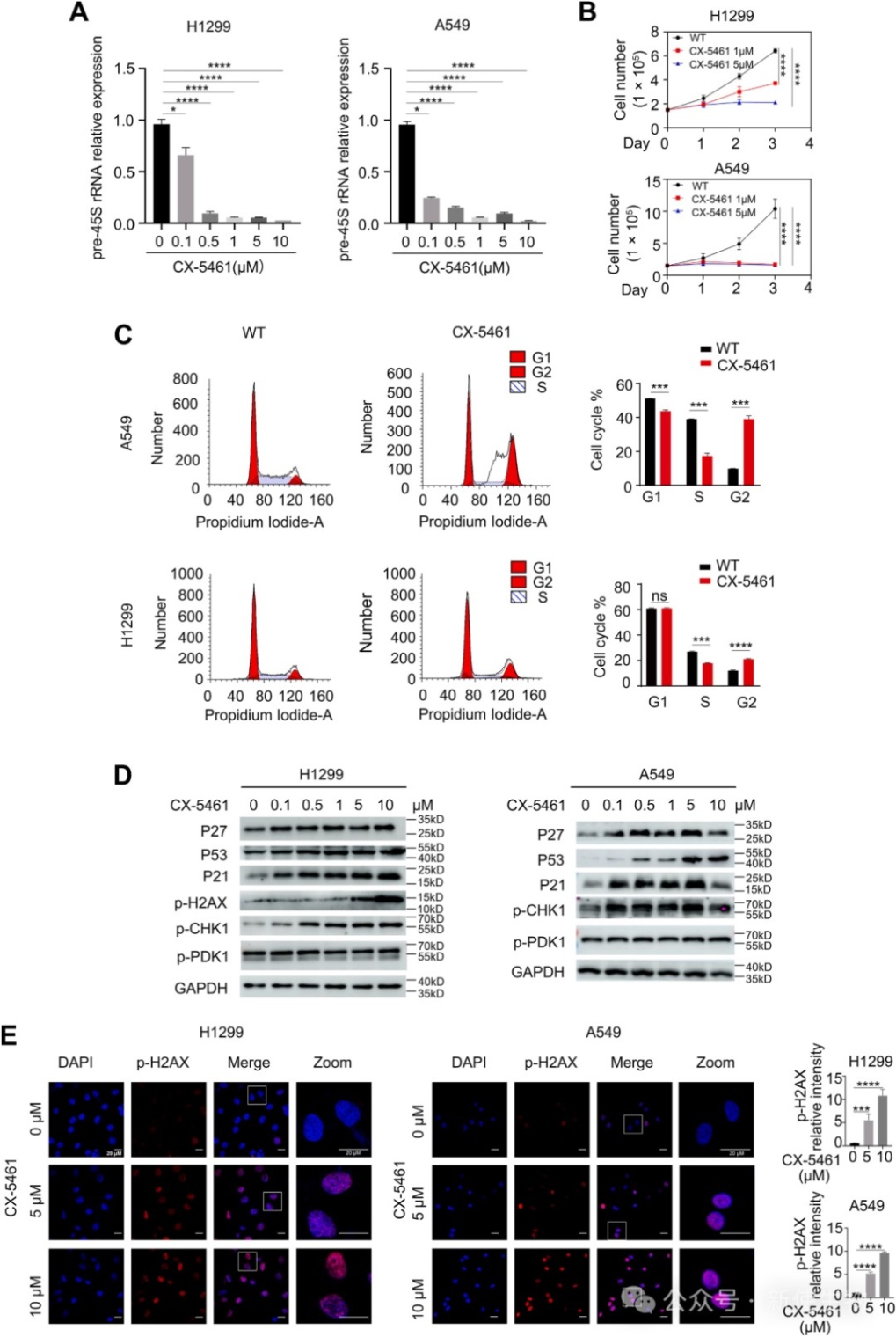
在细胞水平上,CX-5461处理显著抑制了NSCLC细胞系中pre-45S rRNA的表达和细胞增殖。
进一步研究发现,CX-5461诱导了细胞周期G2期阻滞、DNA损伤反应以及细胞凋亡。
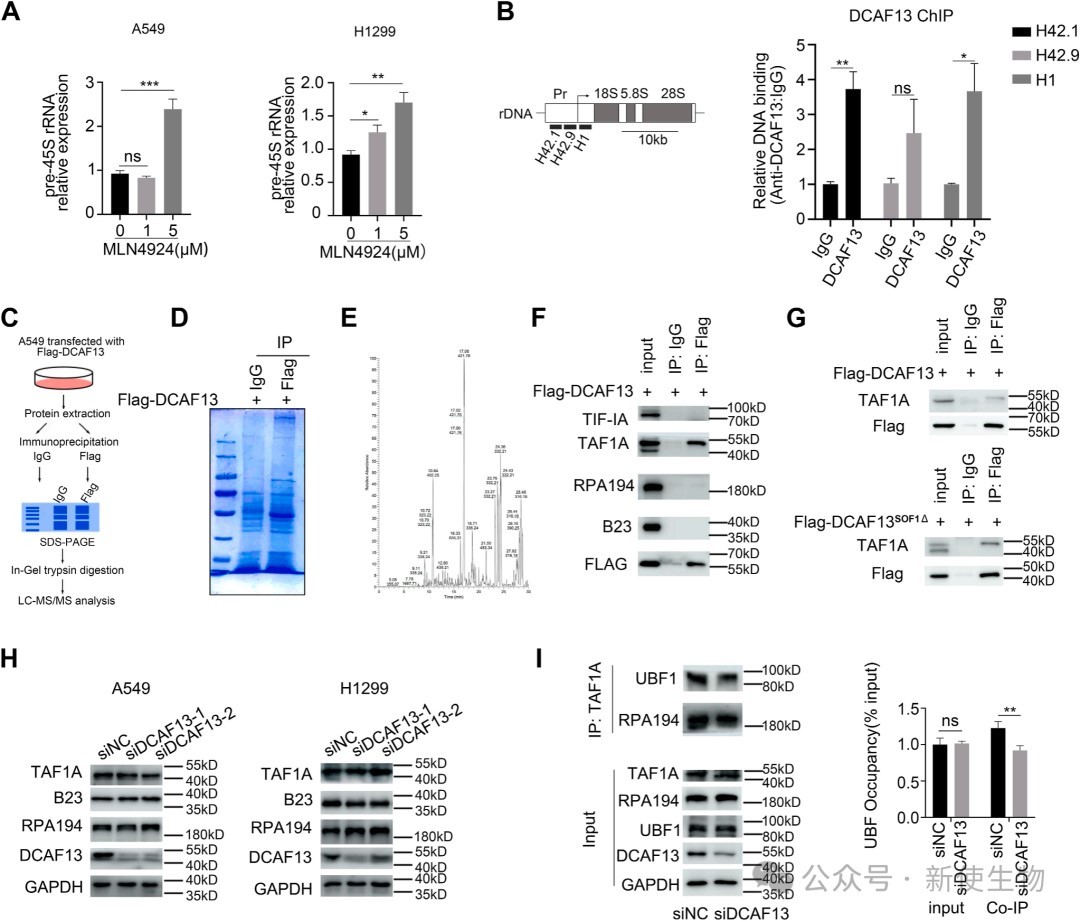
三、核仁蛋白DCAF13在非小细胞肺癌细胞中调节pre-45S rRNA的表达
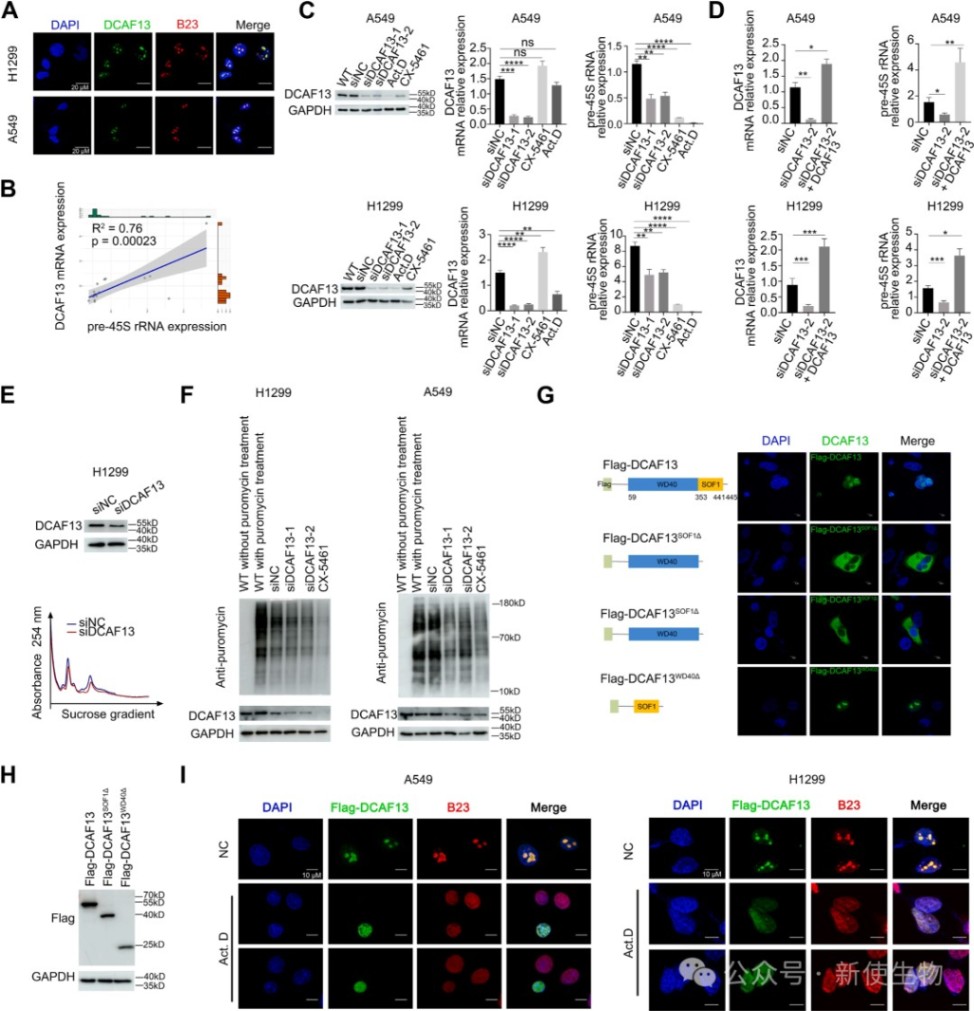
研究发现DCAF13是一种主要定位于NSCLC细胞核仁的蛋白,其表达水平与pre-45S rRNA呈正相关。
通过siRNA干扰和Polysome profiling多聚核糖体分析,作者证实敲低DCAF13后,细胞的pre-45S rRNA水平、多聚核糖体组装能力以及全局蛋白质合成水平均显著下降。
四、DCAF13与TAF1A相互作用且对RNA聚合酶I预起始复合物的组装是必需的
通过免疫沉淀-质谱联用(IP-MS)和共免疫沉淀(Co-IP)等实验,研究者发现DCAF13与rDNA转录预起始复合物的组分TAF1A直接相互作用。
敲低DCAF13会削弱TAF1A与上游结合因子UBF1的结合,表明DCAF13对于rDNA转录机器的正确组装是必需的。
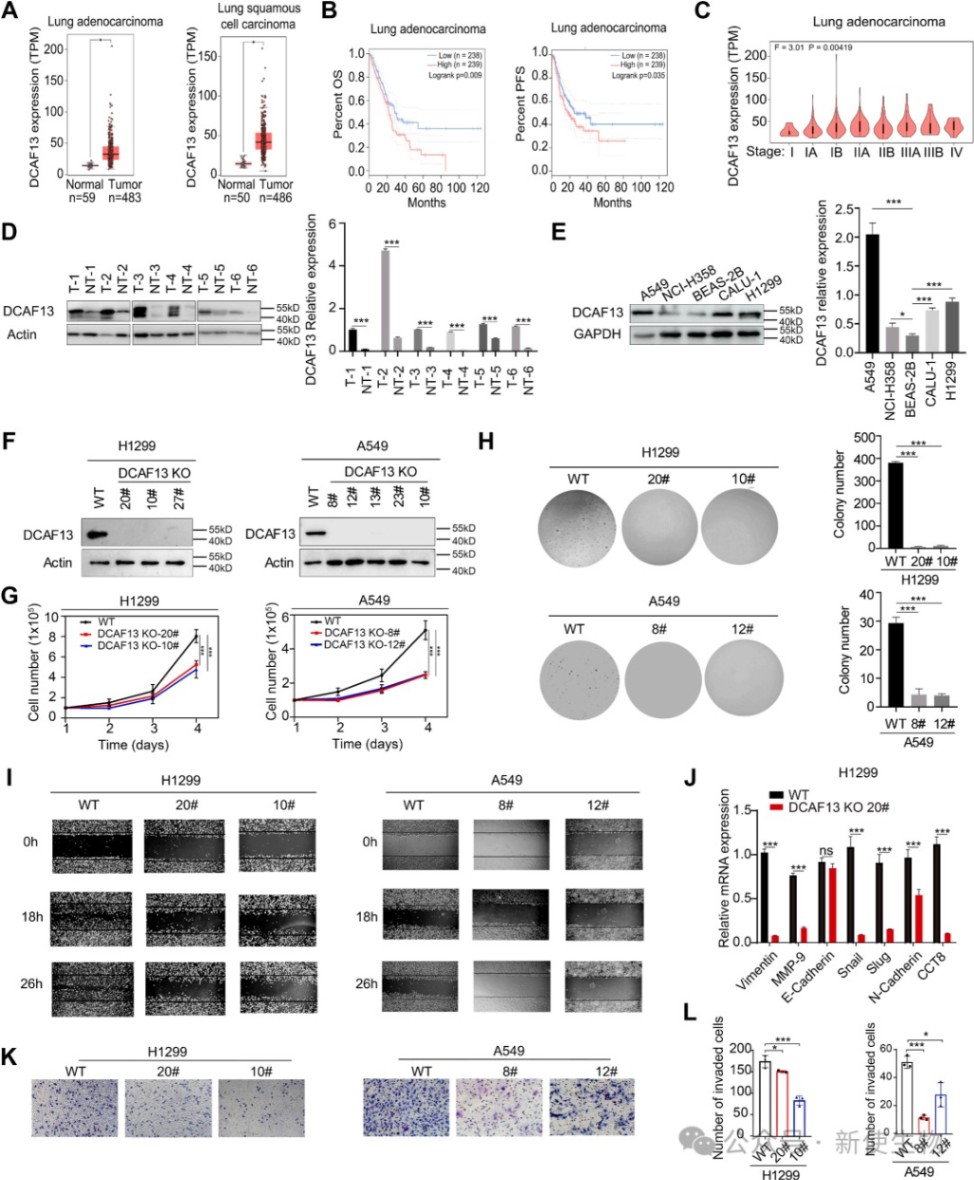
五、DCAF13促进非小细胞肺癌的进展
生物信息学分析和临床样本验证均表明,DCAF13在NSCLC肿瘤组织中高表达,且其高表达与患者的不良预后和更高的临床分期相关。
利用CRISPR/Cas9技术敲除DCAF13后,NSCLC细胞的增殖、克隆形成和迁移能力均受到显著抑制。
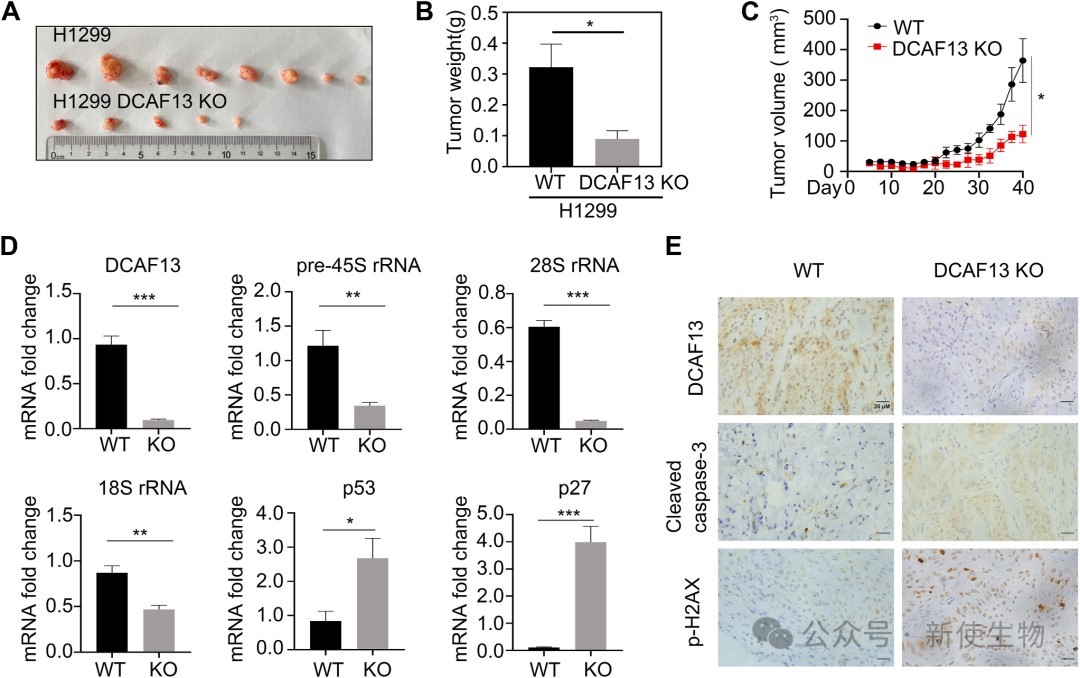
六、DCAF13基因敲除抑制了非小细胞肺癌细胞的体内增殖
在裸鼠皮下成瘤实验中,DCAF13敲除的H1299细胞所形成的肿瘤体积和重量显著小于野生型细胞组,这进一步证实了DCAF13在体内促进NSCLC细胞增殖的重要作用。
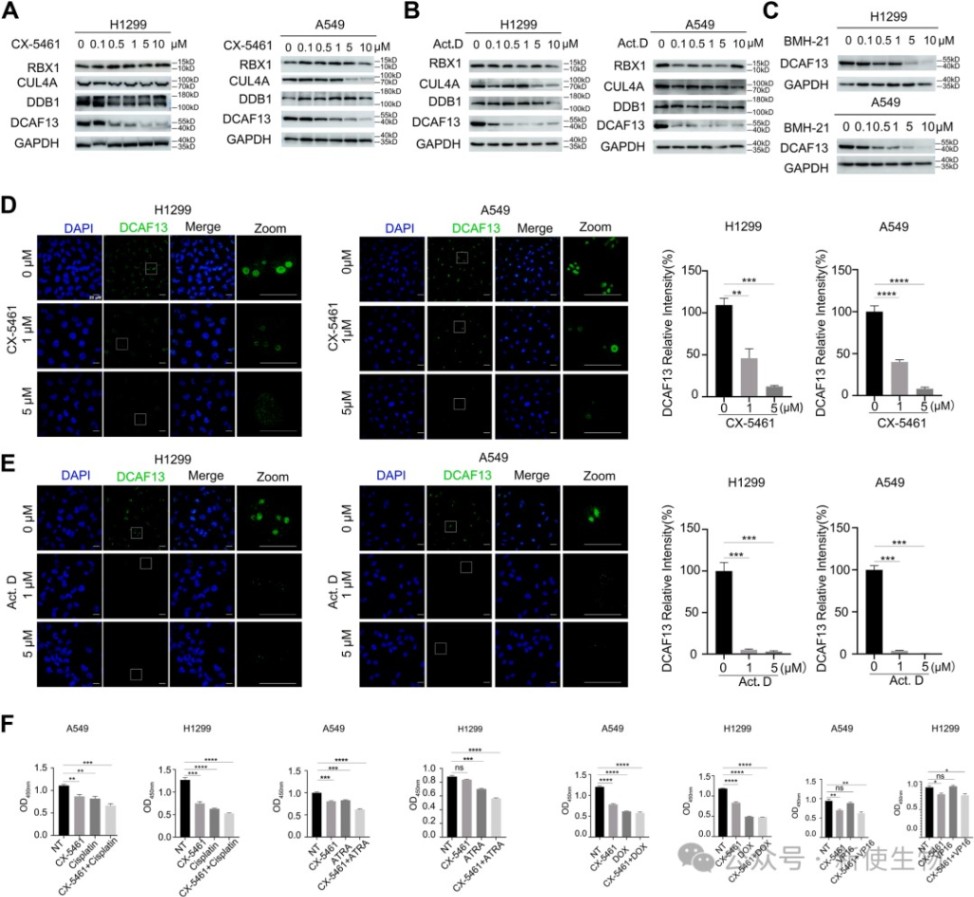
七、rDNA转录抑制剂通过靶向DCAF13抑制非小细胞肺癌细胞增殖
研究发现,多种rDNA转录抑制剂在抑制rDNA转录的同时,也显著降低了DCAF13蛋白的表达水平。
此外,CX-5461与顺铂等化疗药物联用时表现出协同抗癌效应,提示靶向DCAF13通路具有潜在的临床应用价值。
总结
本研究首次揭示了核仁蛋白DCAF13作为rDNA转录的正向调控因子在非小细胞肺癌中的促癌功能。通过与TAF1A协同作用,DCAF13促进rDNA转录和核糖体生物合成,以维持癌细胞的高速增殖。这些发现不仅深化了对NSCLC发病机制的理解,也为开发靶向核糖体生物合成的抗癌疗法提供了新的思路和实验依据。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们