导读
炎症是机体防御感染的重要宿主保护机制,但失调或过度的炎症会导致严重的组织损伤及全身炎症反应综合征等致命病理过程。肿瘤坏死因子(TNF)作为一种关键的促炎细胞因子,主要通过与其受体TNFR1结合来协调免疫反应。
TNFR1不仅激活炎症基因表达,还能在特定环境下诱发程序性细胞死亡,其信号传导的平衡对组织稳态至关重要。虽然TNFR1激活后的下游信号通路已有广泛研究,但细胞如何精密调节TNFR1本身的蛋白丰度以维持组织耐受性仍不清楚。
mRNA的5' UTR区域包含多种顺式作用元件,其中上游开放阅读框(uORF)被认为能调节主编码区的翻译效率。深入探究免疫受体水平的翻译调控机制,对于理解机体如何防止过度免疫反应并开发炎症性疾病的新疗法具有重要意义。
2026年4月3日,牛津大学Mads Gyrd-Hansen与马彪团队合作,在Science Immunology上发表了题为“Upstream ORFs control TNFR1 abundance and tissue tolerance to TNF”的论文。该研究发现TNFR1的蛋白表达水平受到其mRNA中5’ UTR内两个上游开放阅读框(uORF1和uORF2)的精密调控,其中uORF2起主导限制作用。

文章索引
【标题】Upstream ORFs control TNFR1 abundance and tissue tolerance to TNF
【发表期刊】Science Immunology
【发表日期】2026年4月3日
【作者及团队】牛津大学Mads Gyrd-Hansen和马彪团队
【IF】16.3
研究结果
一、TNFRSF1A中保守的上游开放阅读框限制了TNFR1的翻译
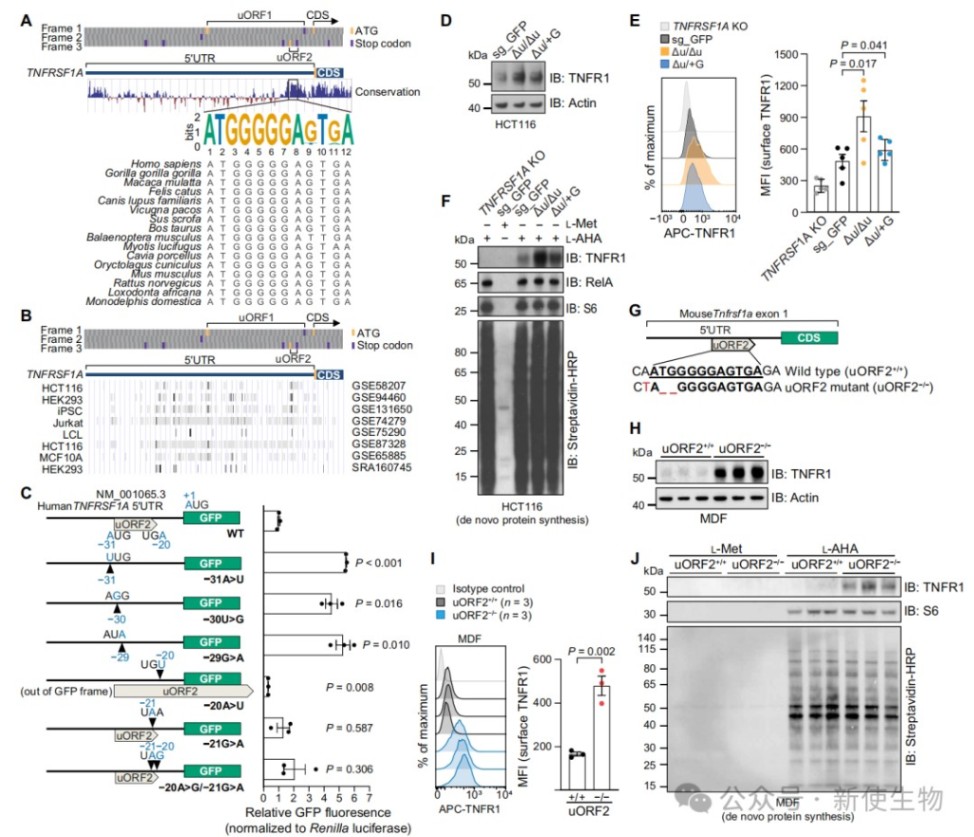
研究通过序列比对和Ribo-seq核糖体印迹分析发现,TNFRSF1A的5' UTR存在两个保守的uORF。
利用绿色荧光蛋白报告系统及基因编辑技术,证实uORF2是限制TNFR1翻译的主导元件,其突变会导致TNFR1蛋白合成及表面表达显著增加。
二、TNFR1丰度是TNF信号转导和细胞死亡的限速因素
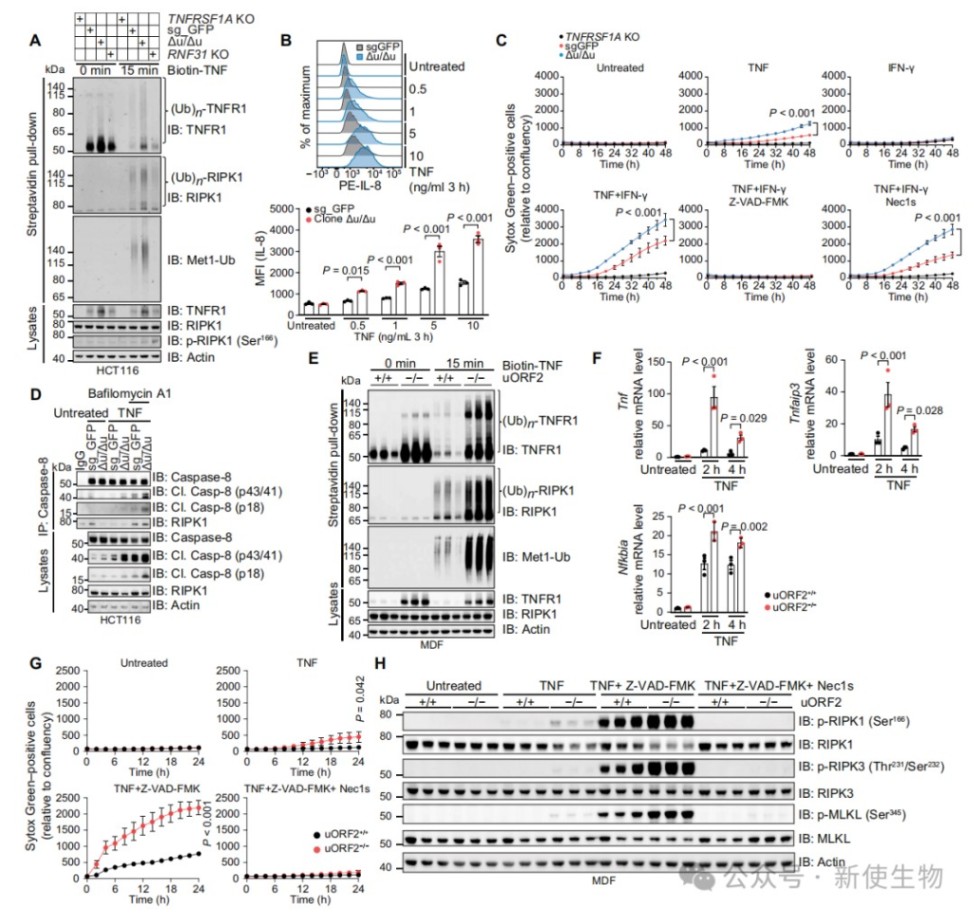
通过对比野生型与uORF2突变细胞,发现TNFR1水平升高增强了TNF诱导的NF-κB信号激活及促炎因子IL-8的产生。
同时,高水平的TNFR1使细胞对TNF诱导的凋亡和坏死性凋亡更加敏感。
三、TNFR1水平升高导致免疫失调
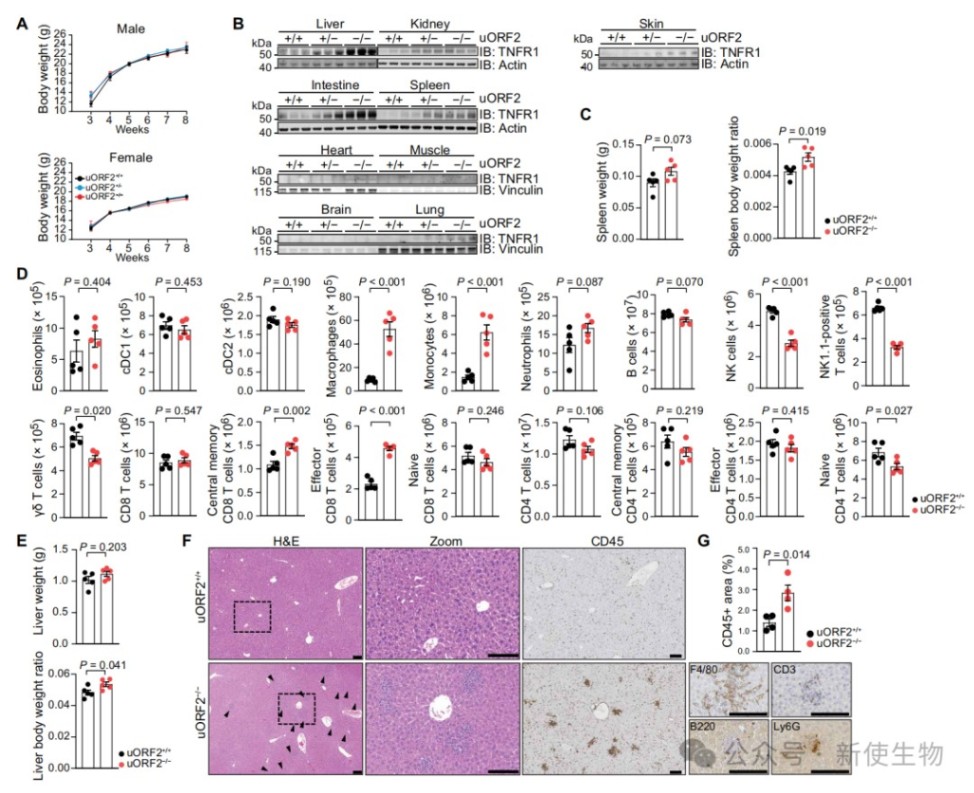
在小鼠模型中,破坏uORF2导致多种组织中TNFR1表达水平升高。
尽管小鼠发育正常,但其脾脏和肝脏表现出明显的免疫细胞浸润及免疫表型改变,证实了TNFR1丰度对免疫稳态的重要性。
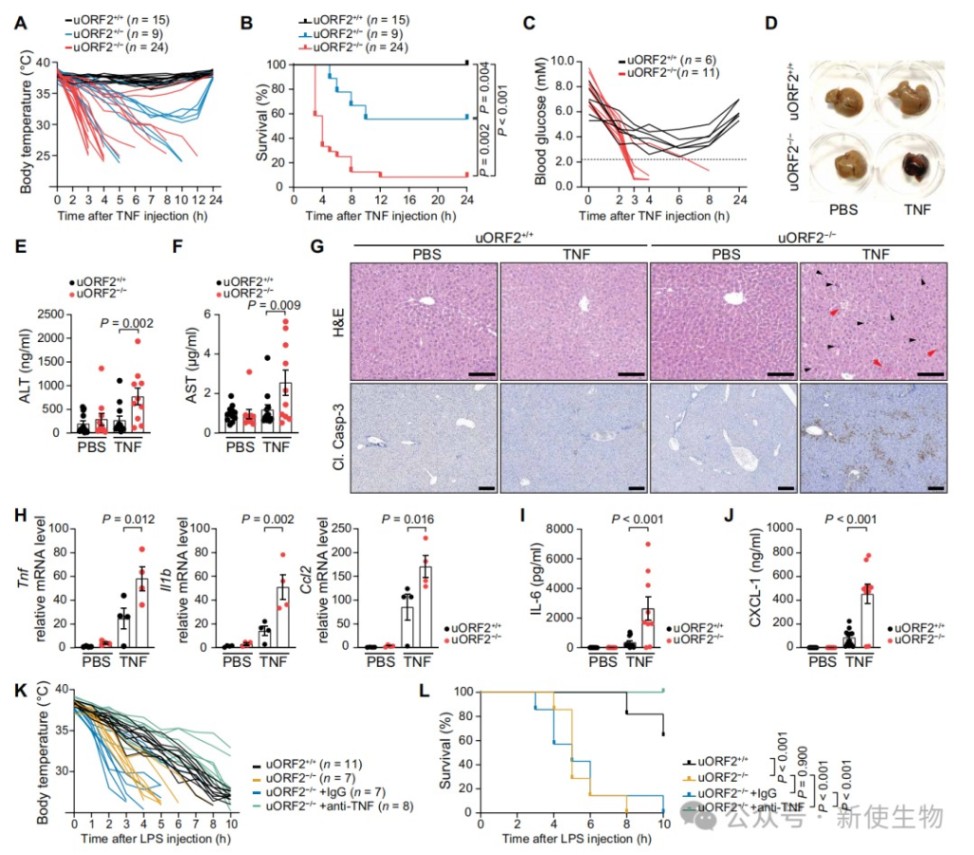
四、TNFRSF1A的uORF2促进了对TNF的组织耐受性
uORF2突变小鼠在TNF刺激下表现出严重的系统性炎症反应综合征,包括体温过低、低血糖及肝脏损伤。
骨髓嵌合实验表明,非造血细胞中TNFR1的翻译调控对于维持组织对TNF的耐受性至关重要。
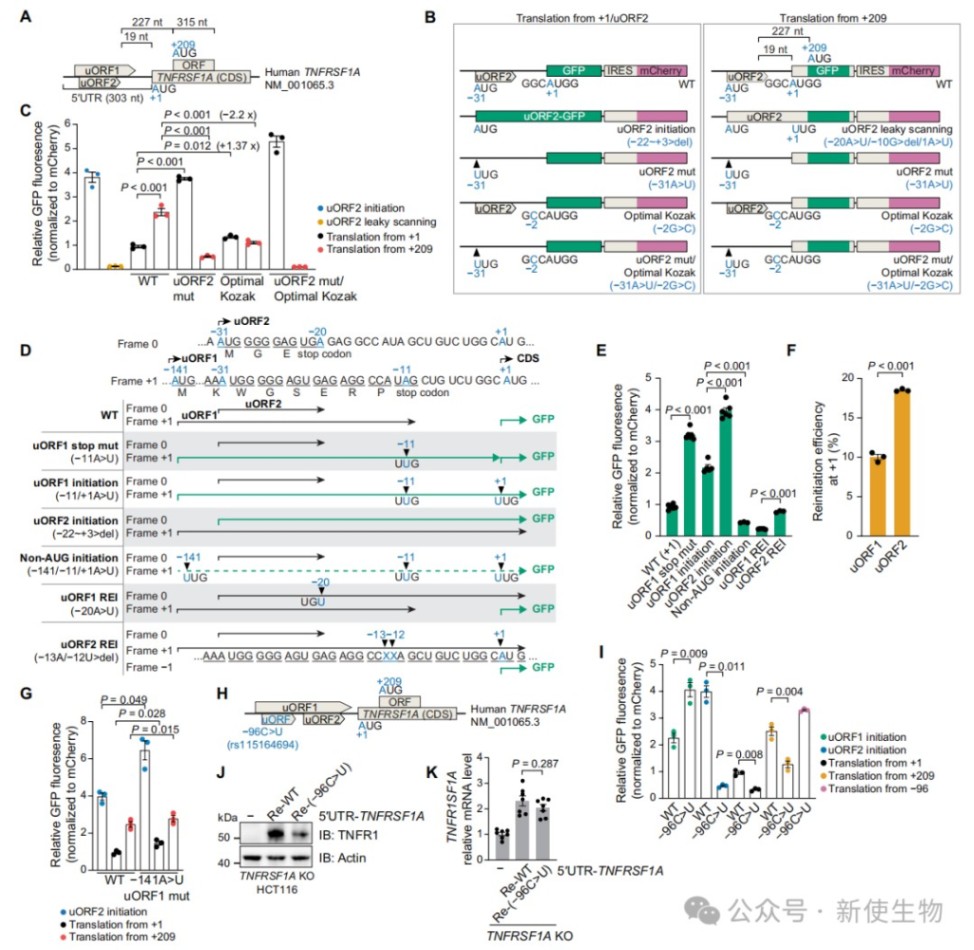
五、uORF2的翻译促进核糖体漏扫描,从而降低TNFRSF1A起始密码子的起始效率
机制研究表明,uORF2通过促进核糖体在主编码序列起始密码子处的漏扫描来抑制翻译。
此外,研究鉴定出的一种人类患者相关的SNP(rs115164694)会在5’ UTR产生新的uORF进一步降低了TNFR1的翻译水平。
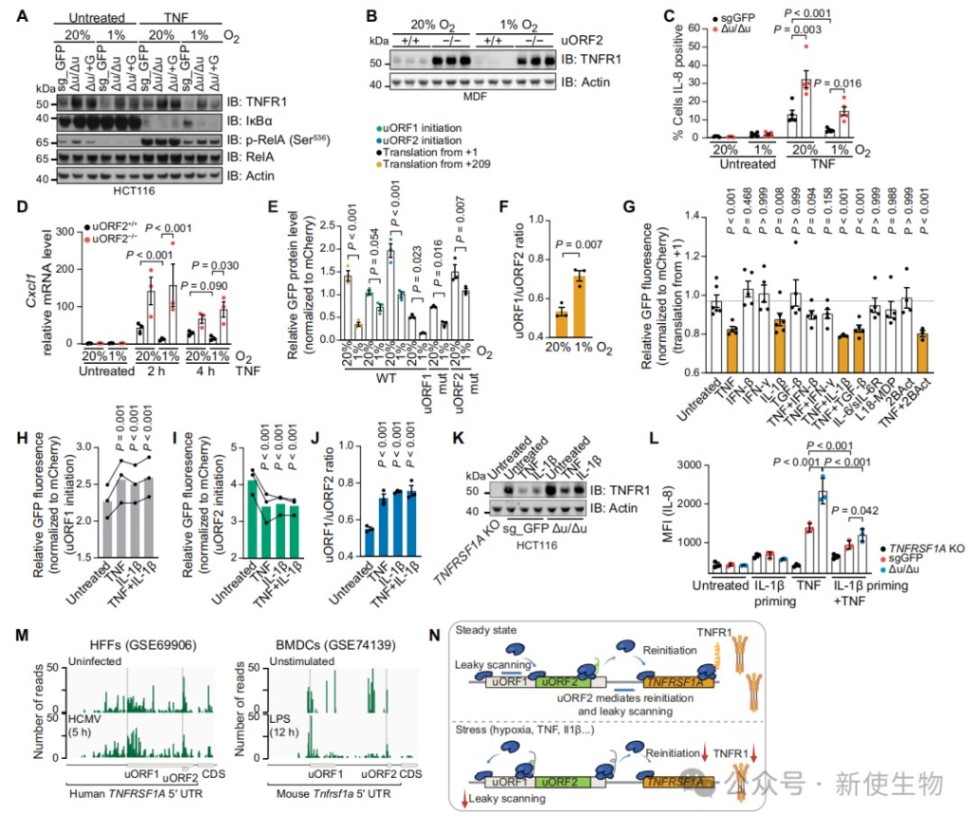
六、应激条件增加uORF1的使用,从而抑制uORF2介导的TNFR1翻译再起始
缺氧及炎症因子刺激会改变uORF1与uORF2的利用比例,导致TNFR1翻译受抑。
这种应激诱导的翻译调控机制使细胞能够根据微环境变化动态调整TNFR1的表达水平。
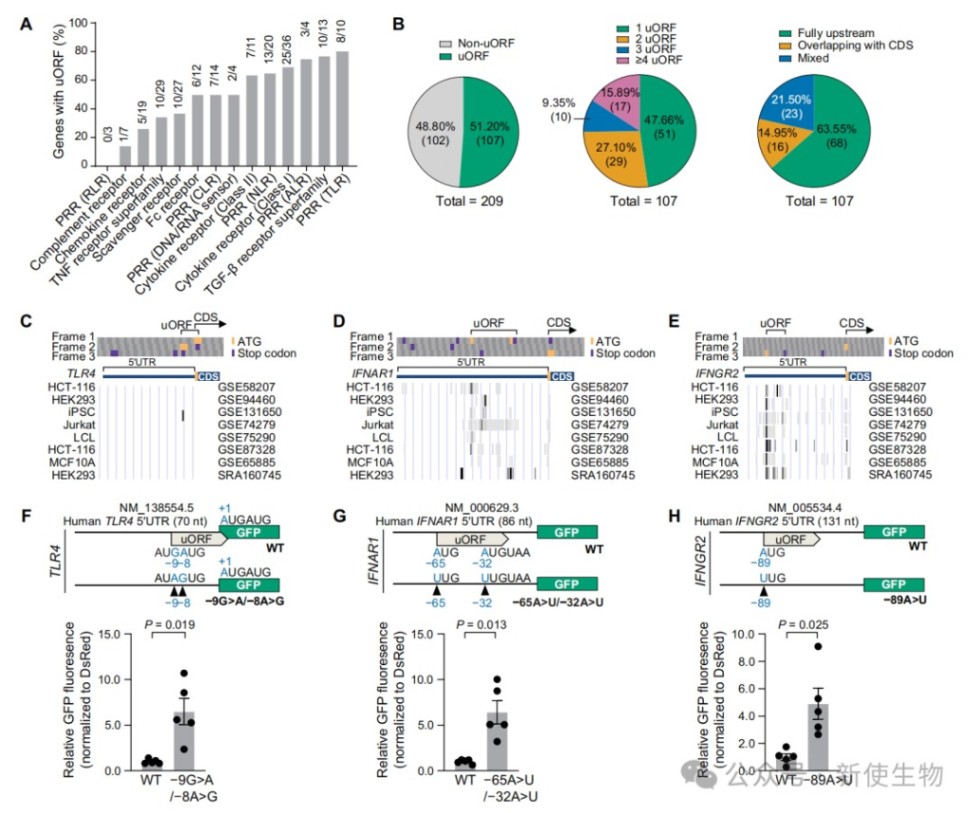
七、uORF负向调控多种免疫受体的翻译
通过生物信息学分析和报告基因实验,发现TLR4、IFNAR1和IFNGR2等多种免疫受体基因的5' UTR同样含有功能性uORF。
这些uORF能够显著抑制下游蛋白的翻译,表明uORF介导的翻译调控是免疫受体表达的一种普遍调控策略。
总结
本研究发现TNFRSF1A基因的uORF通过翻译调控机制精确限制TNFR1的丰度,从而防止过度的TNF信号转导引发的组织损伤。这一发现不仅阐明了组织对TNF耐受性的分子基础,还揭示了uORF在调控免疫受体表达及维持机体免疫稳态中的广泛作用。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们