导读
在表型正常的组织中发现致癌突变在多种成人的器官中都很常见。这表明肿瘤的发生需要多种事件协同作用,并且组织分化等多种生理过程可能具有抑制癌症发生的作用。
在肝脏中,WNT–β-catenin信号通路在维持肝脏稳态过程中的区域化分化中发挥着关键作用。肝小叶沿门静脉-中央静脉轴可分为三个功能不同的区域(1区、2区和3区)。
然而,编码β-catenin的CTNNB1癌基因在肝细胞癌中也经常发生突变,导致WNT信号异常激活并促进细胞生长。因此,深入理解CTNNB1突变如何影响肝细胞的区域化特征,并揭示其在促进分化与驱动肿瘤发生这对矛盾角色之间的平衡机制,对于阐明肝癌的起源至关重要。
2025年11月19日,英国癌症研究中心苏格兰研究所Owen J. Sansom团队在Nature上发表了一篇题为“Hepatic zonation determines tumorigenic potential of mutant β-catenin”的论文。该研究深入解析了WNT驱动的生长与分化之间的拮抗作用,揭示了肝脏分区特征如何决定肝细胞对肿瘤发生的敏感性。

文章索引
【标题】Hepatic zonation determines tumorigenic potential of mutant β-catenin
【发表期刊】Nature
【发表日期】2025年11月19日
【作者及团队】英国癌症研究中心苏格兰研究所Owen J. Sansom团队
【IF】48.5
研究结果
一、MYC是WNT驱动肝癌发生的必要协同因子
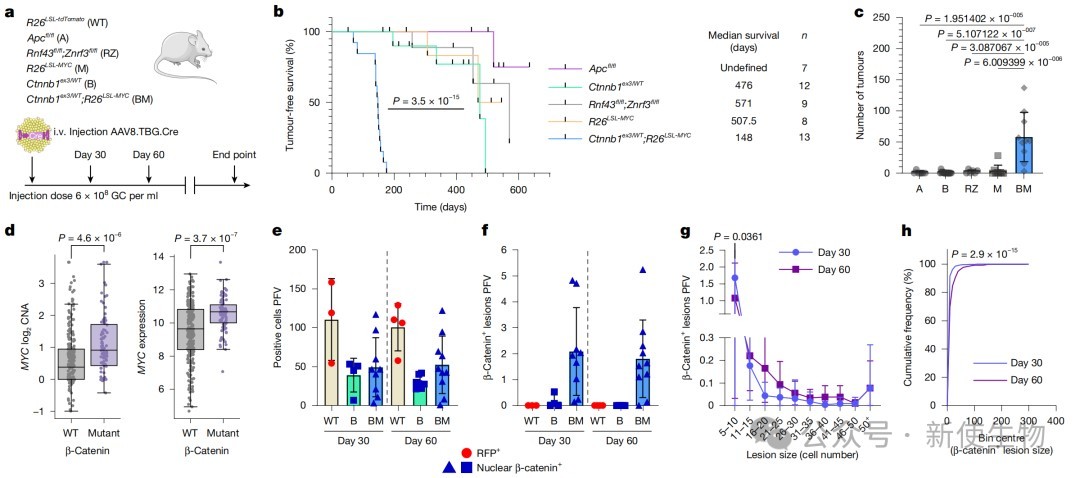
研究发现,在小鼠肝脏中,单独的WNT通路突变(如Ctnnb1激活突变或Apc缺失)致瘤性很弱。
与人类肝细胞癌中CTNNB1突变常伴随MYC扩增的现象一致,在小鼠模型中共同激活Ctnnb1和MYC能显著促进肿瘤发生,并驱动与mRNA翻译相关的增殖性基因程序。
二、肿瘤的启动需要下调WNT信号并激活促生长通路
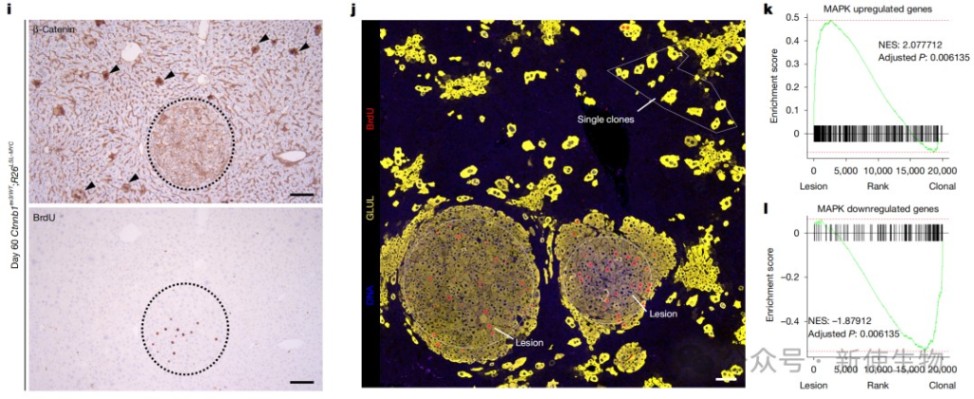
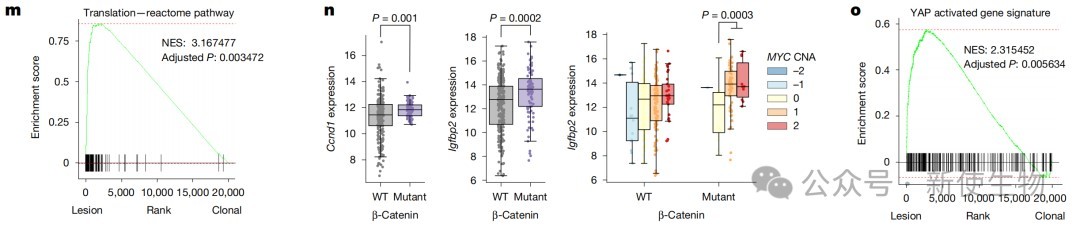
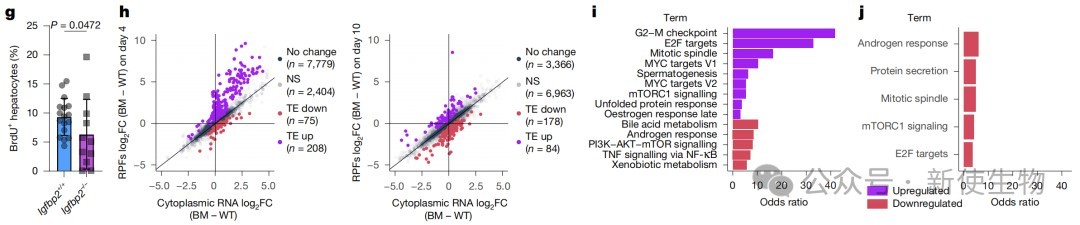
空间转录组学和免疫组化显示,增殖性病变重新激活了通常与2区肝细胞稳态增殖相关的因子,包括IGFBP2、mTOR活性和CCND1。
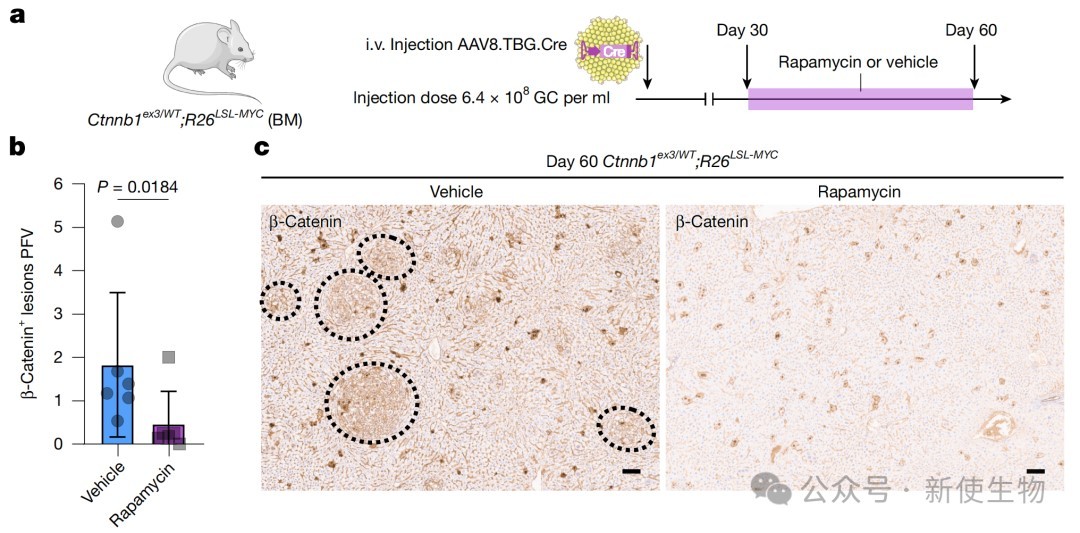
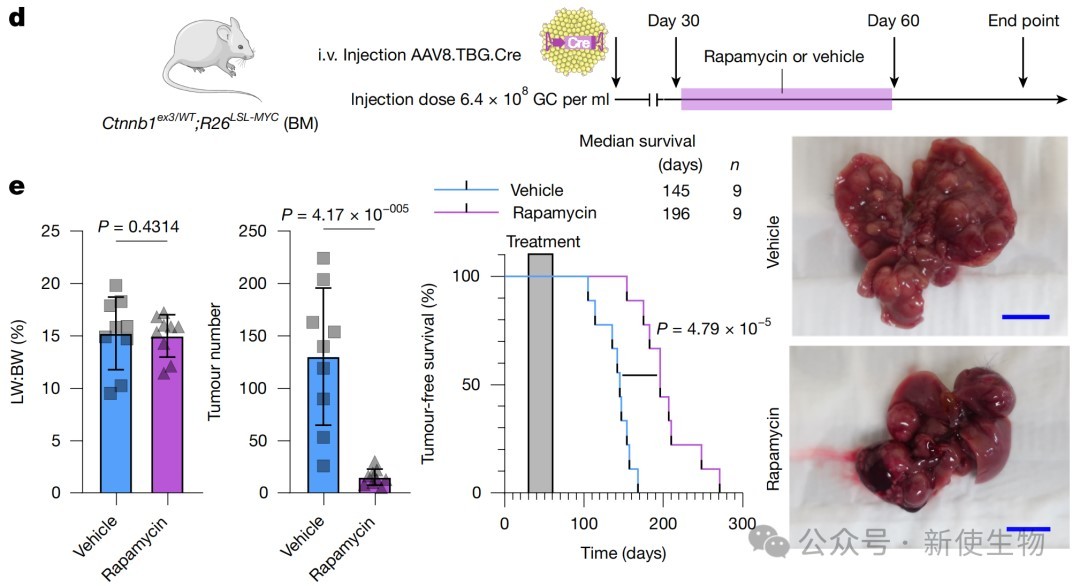
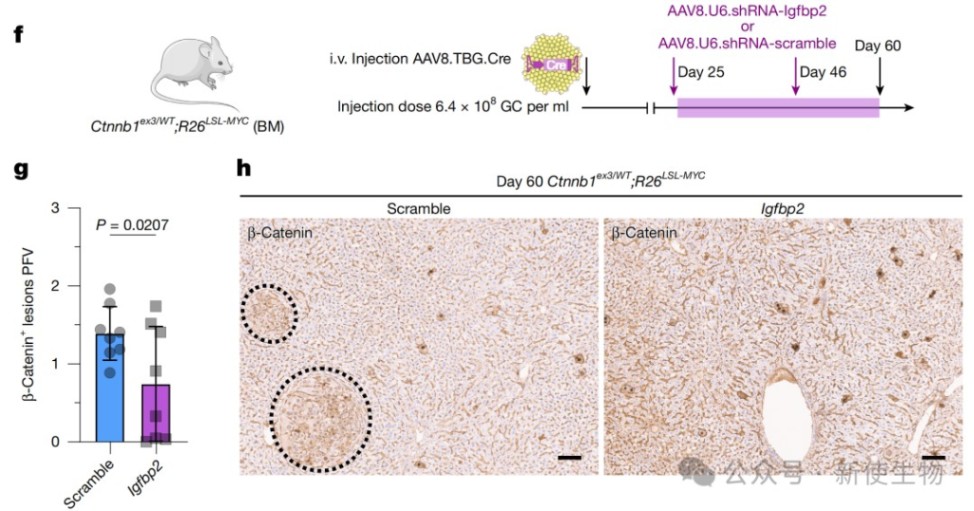
功能性实验证实,在病变形成期间使用雷帕霉素抑制mTOR,或者敲低Igfbp2,均能显著抑制病变的形成和肿瘤的发展。
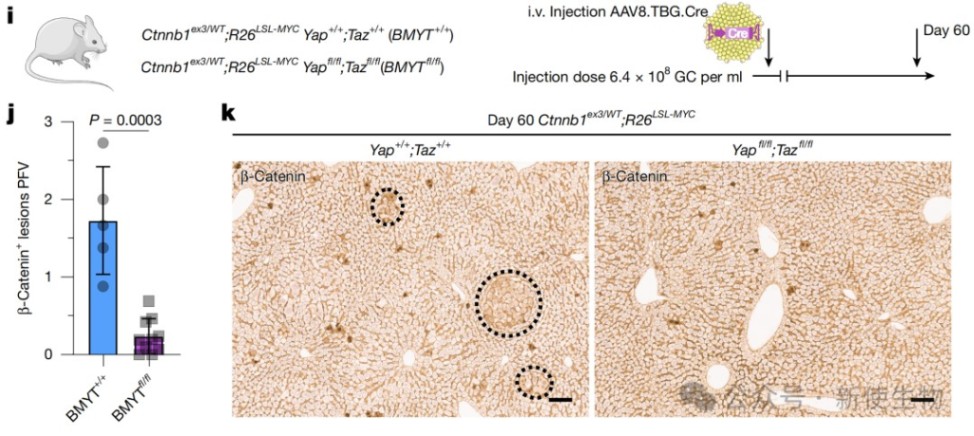
同时,敲除Yap和Taz也完全阻止了病变形成,表明这些因子对于克服WNT诱导的分化抑制至关重要。
三、WNT和MYC信号的急性激活导致短暂增殖和最终的3区化分化
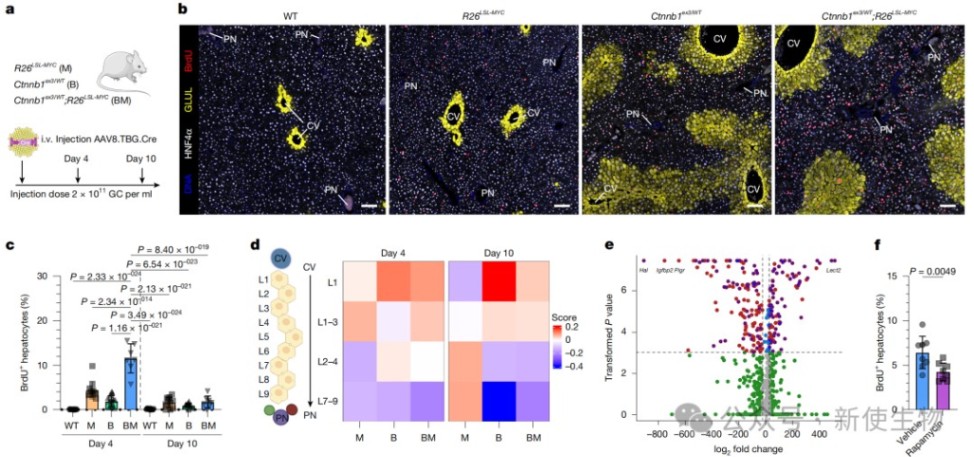
研究人员在整个肝脏中急性、同步激活Ctnnb1和MYC突变,观察到肝细胞在第4天出现一过性的爆发式增殖,主要发生在1区和2区。
然而,到第10天,增殖基本停止,整个肝小叶的细胞都分化为表达3区标志物GLUL的成熟状态。
这表明WNT信号最终会强制细胞进入分化状态,从而终止增殖。
四、Lgr5+肝细胞抵抗WNT驱动的肿瘤发生
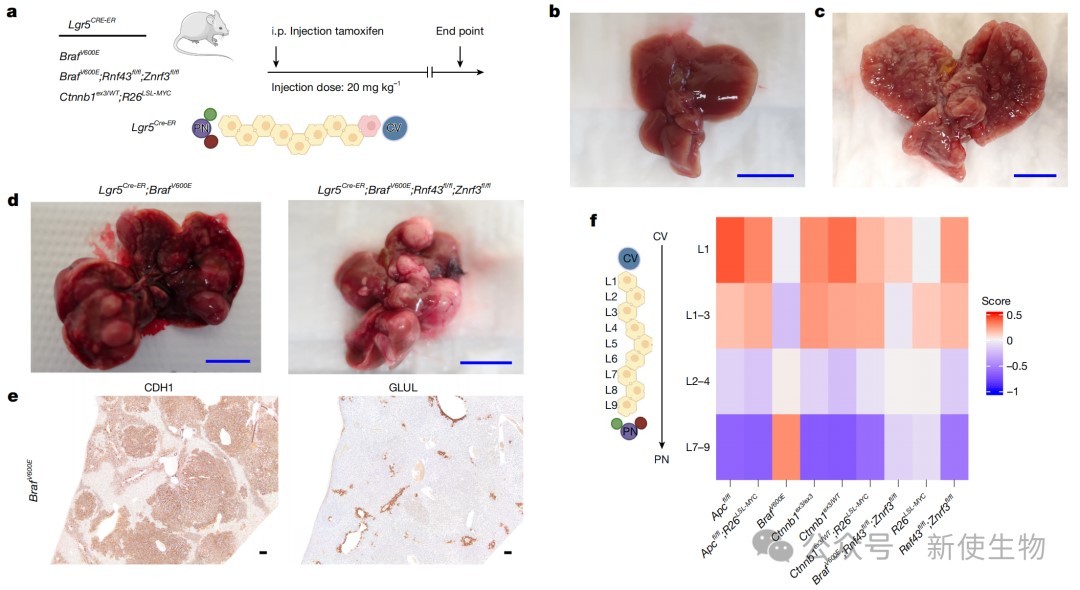
研究发现,肝小叶中最靠近中央静脉的3区肝细胞(GLUL+/Lgr5+)对WNT/MYC驱动的肿瘤发生具有天然的抵抗力。
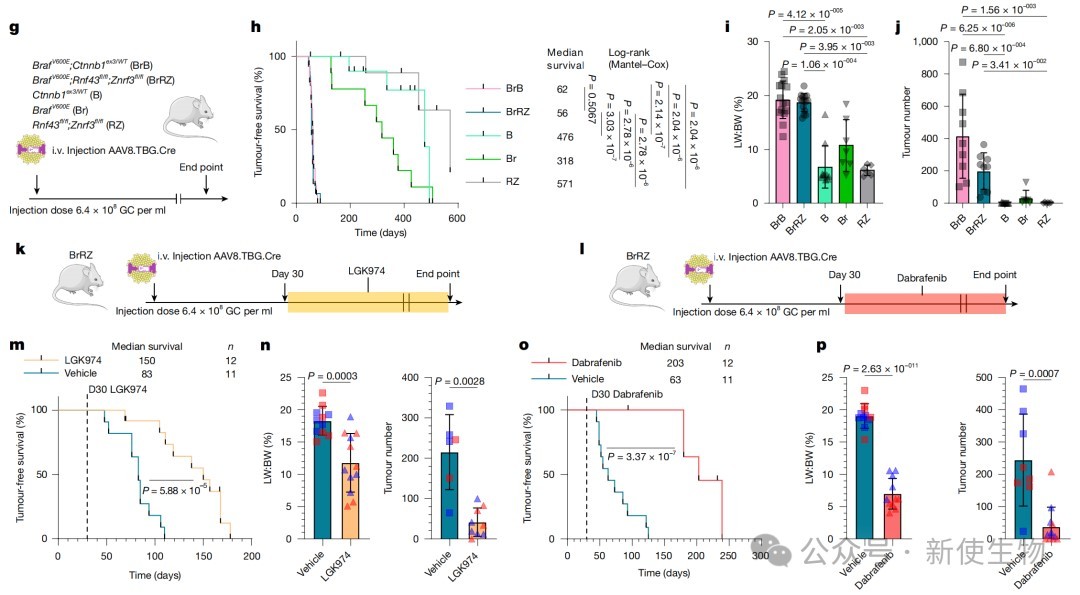
然而,如果在这些细胞中额外引入激活MAPK通路的Braf V600E突变,它们便能成功形成肿瘤。
这表明,MAPK信号能够有效对抗WNT驱动的3区化分化,使原本具有抵抗力的细胞变得易感。
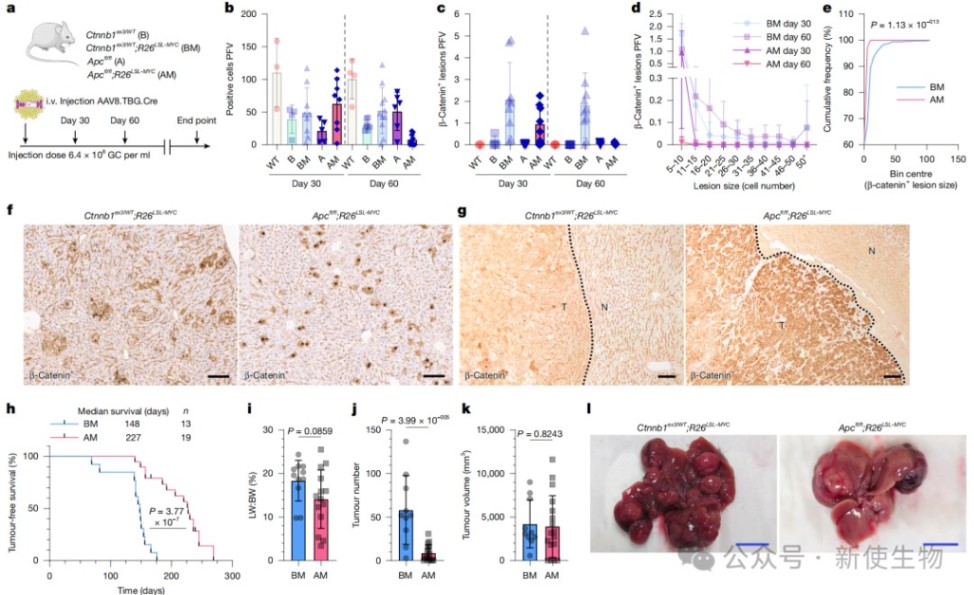
五、Apc缺失导致过高的WNT活性,反而不利于肝癌发生
对比分析显示,人类肝癌中绝大多数WNT突变是CTNNB1外显子3的点突变,而非结直肠癌中常见的APC缺失。
实验表明,Apc缺失会导致极高水平的WNT信号,这会强制肝细胞处于高分化的3区状态,反而抑制了病变形成。
相比之下,CTNNB1点突变产生的WNT活性处于最合适的水平,既能提供一定的生长信号,又容易通过其他机制逃脱分化陷阱,从而更利于肿瘤发生。
总结
本研究系统地揭示了WNT信号在肝脏中的双重作用:生理上促进分化,病理上驱动癌症。研究证明,肝细胞的区域化分化状态是其抵抗癌症发生的天然屏障,突变细胞必须通过调节WNT信号强度并劫持其他生长通路来逃避分化,才能最终演变为肿瘤,这为理解肝癌的早期发生机制和开发化学预防策略提供了新的理论依据。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
我们能够针对微量细胞或组织,如卵母细胞、卵巢、临床穿刺样品等产出高质量翻译组数据结果。
超高的准确性为研究非经典的开放阅读框(ORFs)提供极大便利,提高微肽(肿瘤新生抗原)的挖掘效率。
另外新使生物提供多物种多聚核糖体分析(Polysome profiling),了解更多翻译组技术信息可登录 www.neoribo.com。
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们