导读
核糖体蛋白突变所导致的核糖体病与人类癌症风险增加相关。近年来,大规模癌症测序研究在多种实体瘤和血液恶性肿瘤中发现了核糖体蛋白突变,进一步暗示它们可能是癌症的驱动因素。
例如,在慢性淋巴细胞白血病(CLL)中,已发现核糖体蛋白基因RPS15存在复发性热点突变。然而,核糖体蛋白功能异常通常会激活p53等重要的肿瘤抑制因子,从而抑制细胞增殖,这与癌症的发生形成了悖论。
这一从增殖减退状态向增殖亢进的癌症易感状态的转变,被称为“Dameshek之谜”。尽管先前有研究在其他疾病模型中将此现象与氧化应激和基因组不稳定性联系起来,但对于RPS15突变在CLL中的体内致病机制,及其是否为真正的癌症驱动因素仍是未解之谜。
2026年3月30日,哈佛医学院Catherine J. Wu团队在Nature Communications上发表了一篇题为“Mutant ribosomal protein RPS15 drives B cell malignancy through oxidative stress and genomic instability”的论文。该研究明确了RPS15突变是CLL的驱动因素,发现该突变通过诱导翻译缺陷,引发氧化应激和基因组不稳定性,最初导致细胞低增殖,但为后续获得如TP53缺失等二次打击、最终触发恶性转化创造了条件。

文章索引
【标题】Mutant ribosomal protein RPS15 drives B cell malignancy through oxidative stress and genomic instability
【发表期刊】Nature Communications
【发表日期】2026年3月30日
【作者及团队】哈佛医学院Catherine J. Wu团队
【IF】15.7
研究结果
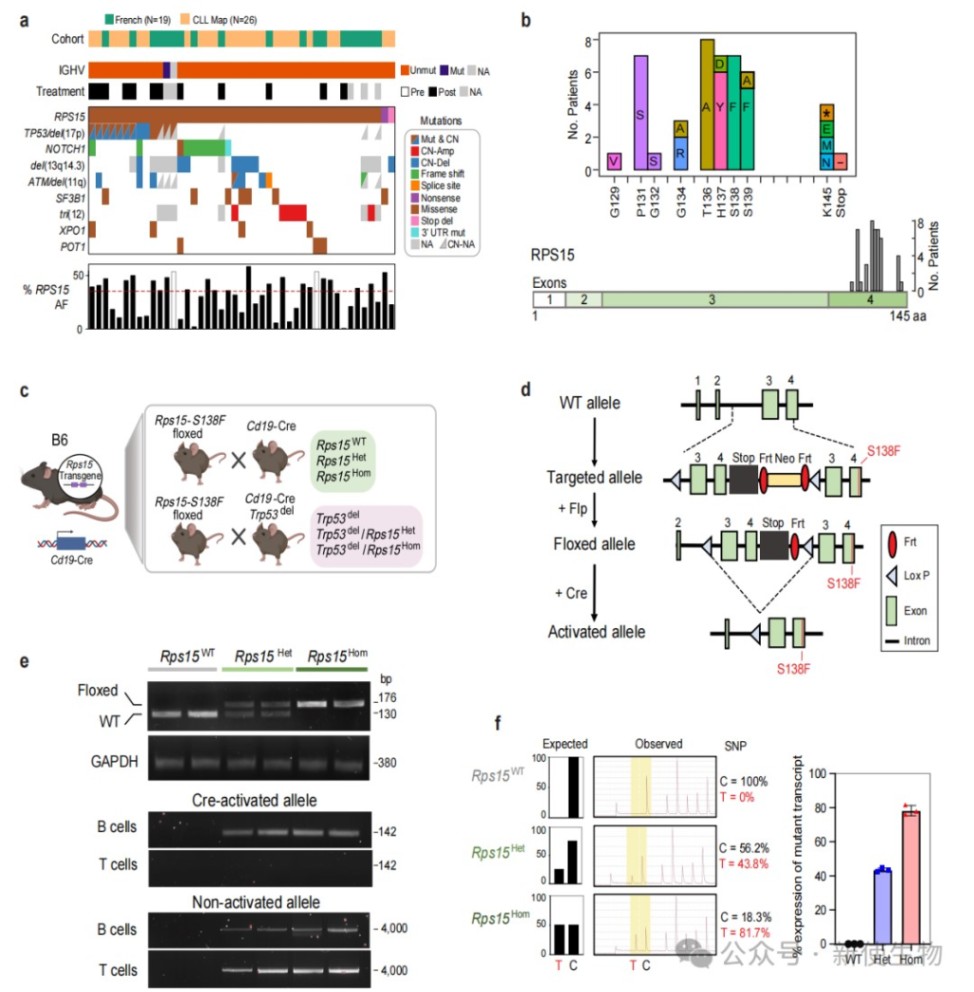
一、RPS15突变是CLL的驱动因素,与TP53突变共存并驱动B细胞恶性转化
通过分析两个CLL患者队列,研究发现RPS15突变常与TP53缺陷共存。
利用Cd19-Cre/loxP系统构建的Rps15-S138F突变小鼠模型,在高龄杂合子小鼠中成功诱发了CLL样疾病,证实了其在体内的致癌驱动作用。
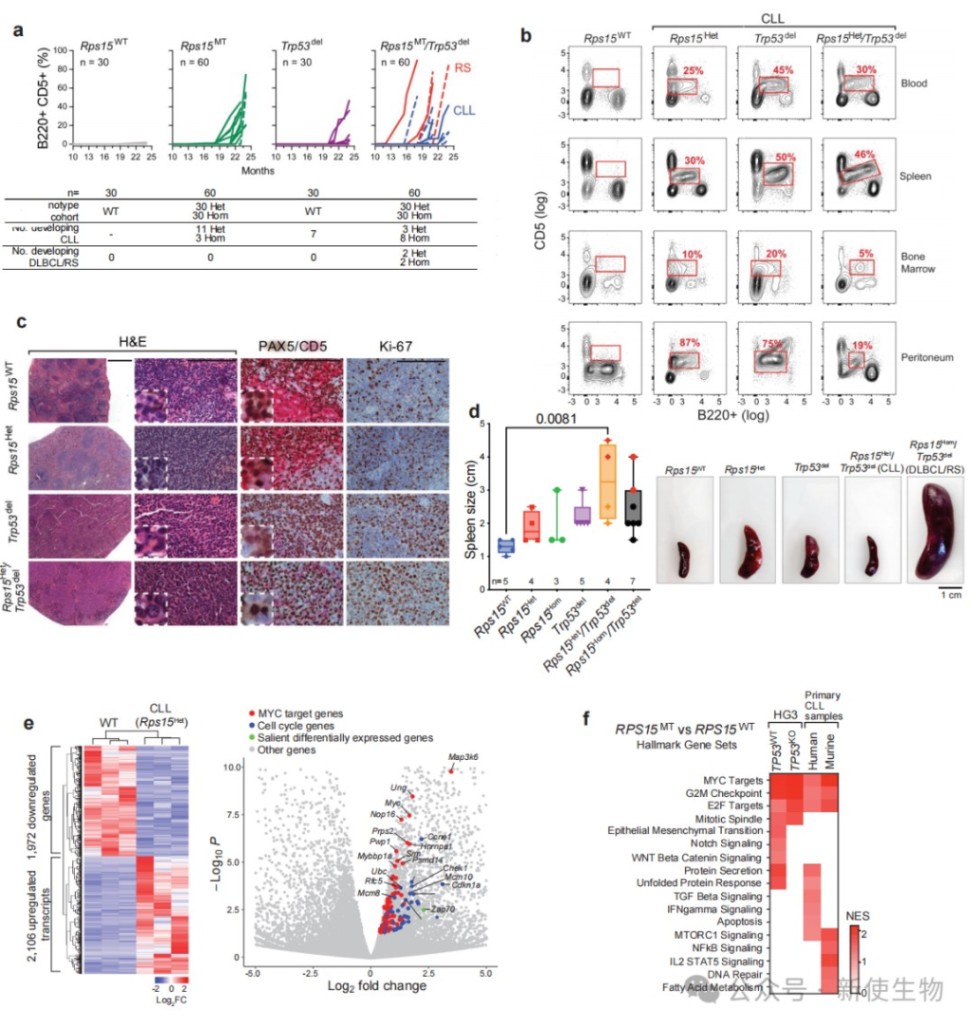
二、Rps15突变在白血病前期诱导增殖减退,但在肿瘤中表现为增殖亢进
对白血病前期和白血病期B细胞的RNA-seq分析显示,前期细胞表现出Myc靶基因下调和细胞周期抑制的增殖减退特征。
相反,已形成的CLL样肿瘤细胞则表现出强烈的Myc信号和增殖亢进特征,揭示了疾病发展过程中的表型转换。
三、白血病前期Rps15突变B细胞累积氧化应激和DNA损伤
通过流式细胞术检测,发现突变B细胞的线粒体活性氧(ROS)水平和DNA双链断裂标志物γH2AX显著升高。
对肿瘤样本的全基因组测序(WGS)进一步揭示了过氧化物损伤特有的突变特征,表明氧化应激是导致DNA损伤的关键上游事件。
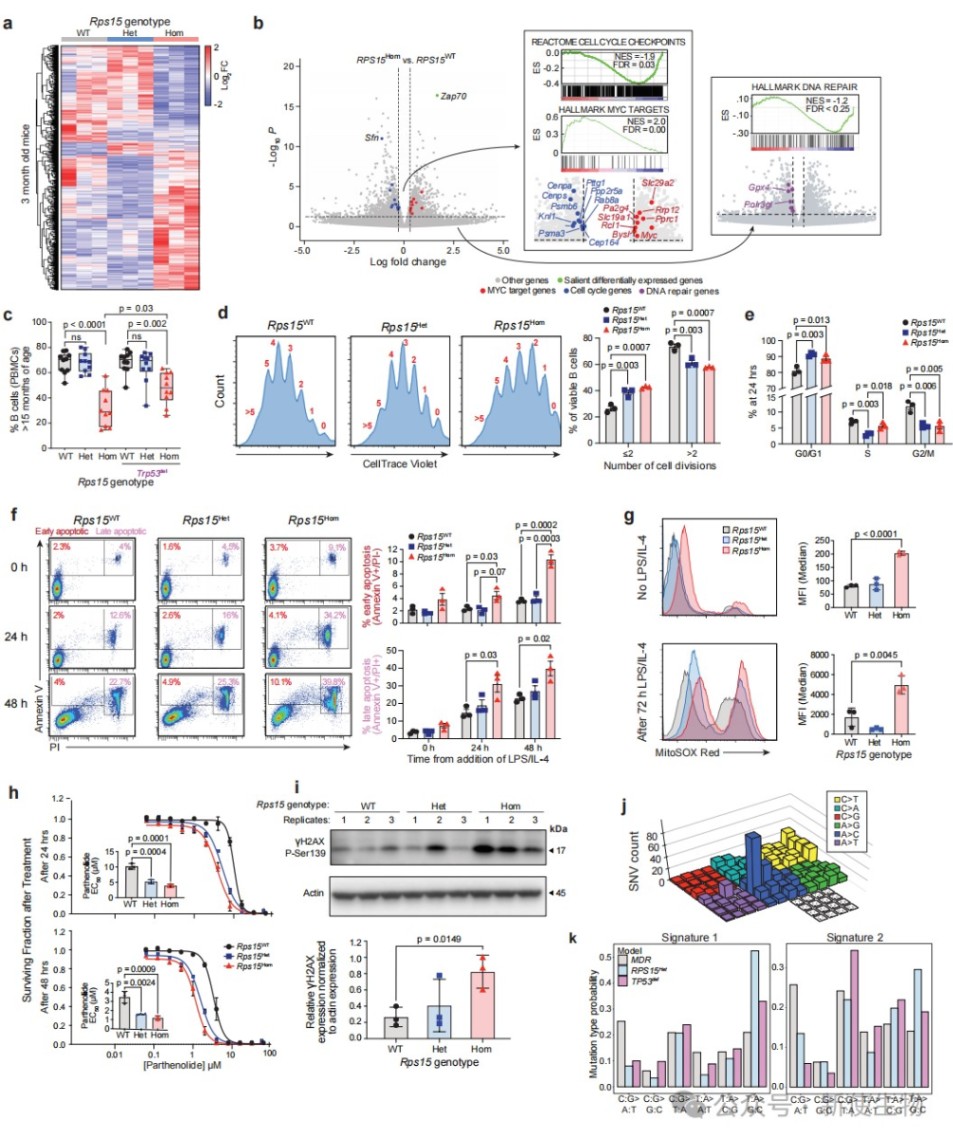
四、p53介导的反应是增殖减退的关键,其缺失可逆转该表型
使用抗氧化剂NAC处理可部分恢复突变细胞的增殖能力,表明氧化应激抑制了细胞增殖。
在Rps15突变背景下敲除一个拷贝的Trp53基因,完全逆转了细胞的增殖减退表型并加剧了DNA损伤,证明p53在抑制细胞周期和维持基因组稳定中发挥了关键的保护作用。
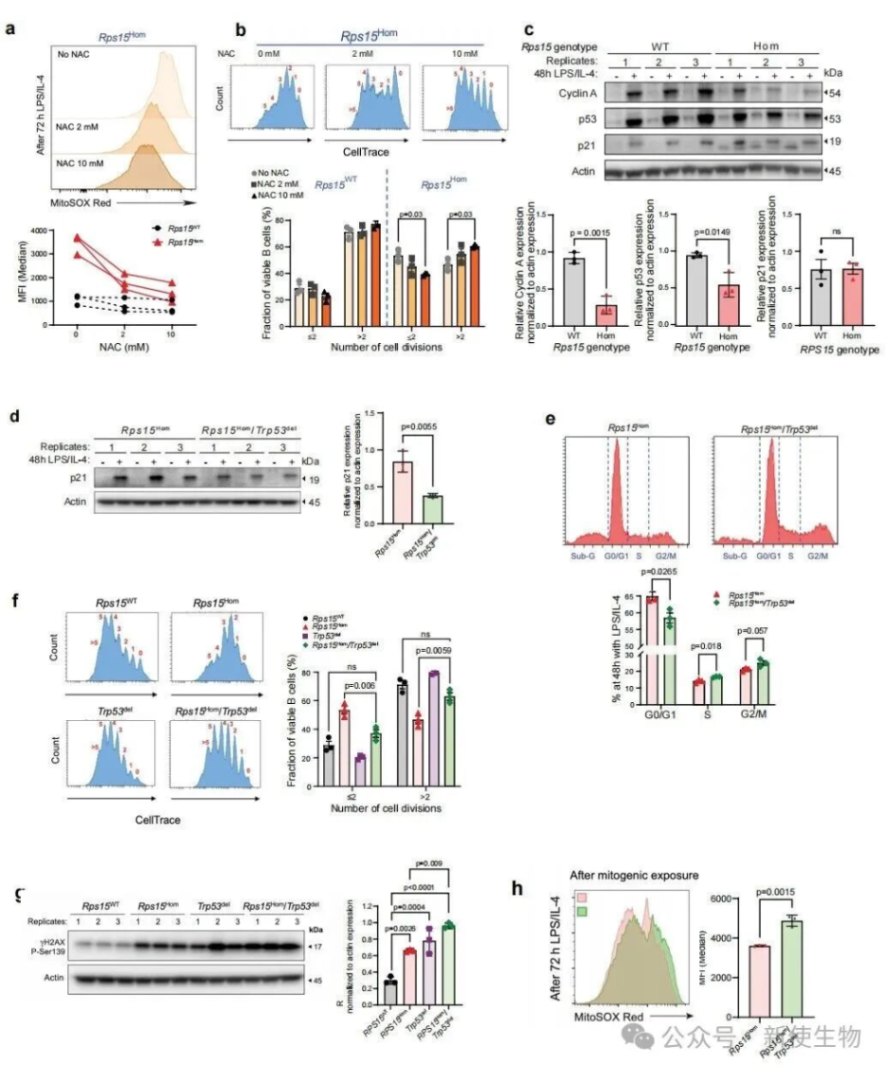
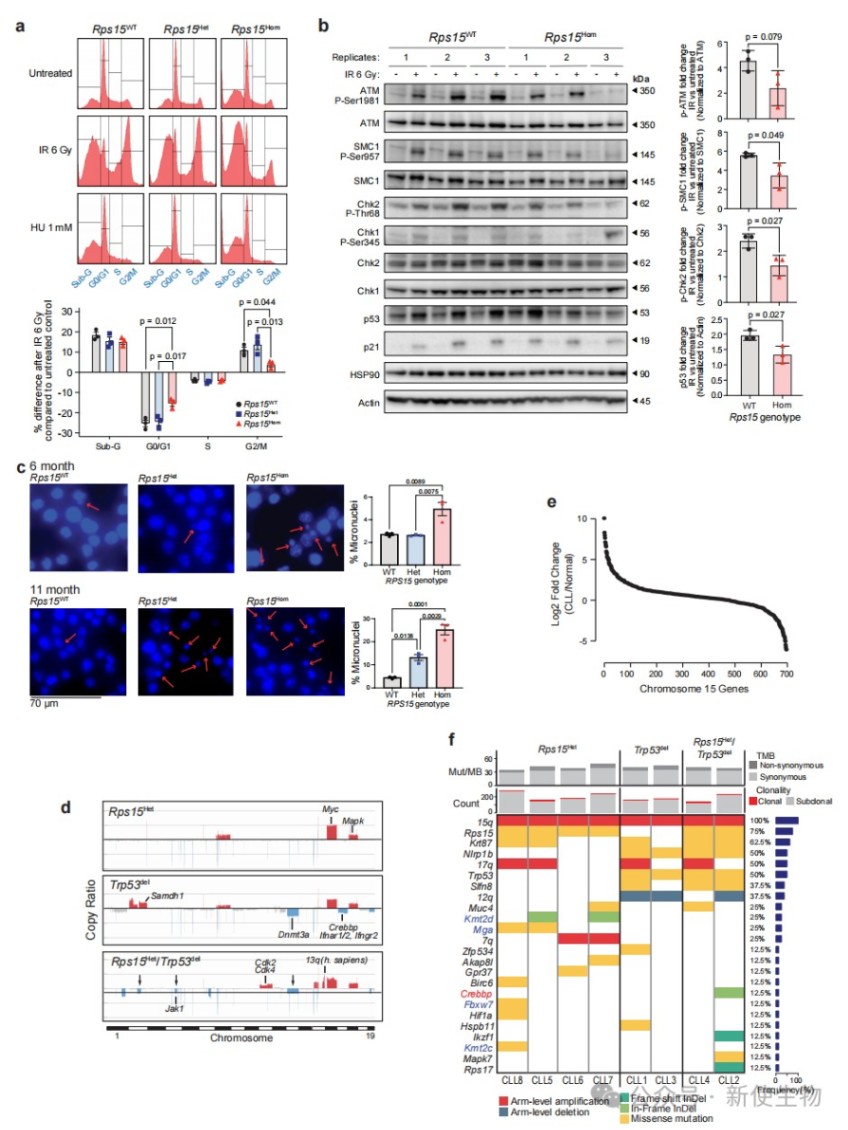
五、Rps15突变导致DNA损伤反应缺陷和基因组不稳定性
功能实验表明,Rps15突变细胞在应对电离辐射(IR)诱导的DNA损伤时,其ATM-Chk2信号通路活化受损。
同时,这些细胞表现出微核形成率增加和染色体不稳定性,最终在肿瘤中累积了包括Myc扩增在内的大量基因组变异。
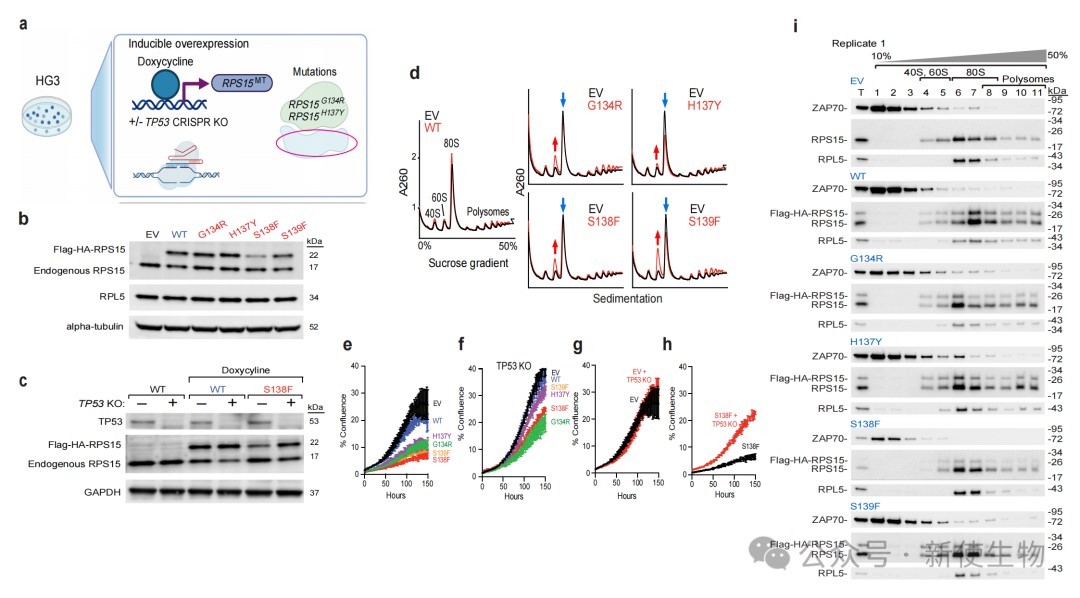
六、RPS15突变干扰核糖体组装和成熟
在HG3细胞系模型中,Polysome profiling多聚核糖体分析显示RPS15突变导致40S亚基成熟缺陷,表现为80S单体减少和游离60S亚基积累。
尽管蛋白稳定性下降,但突变型RPS15仍能整合进核糖体中并分布于细胞质和核仁。
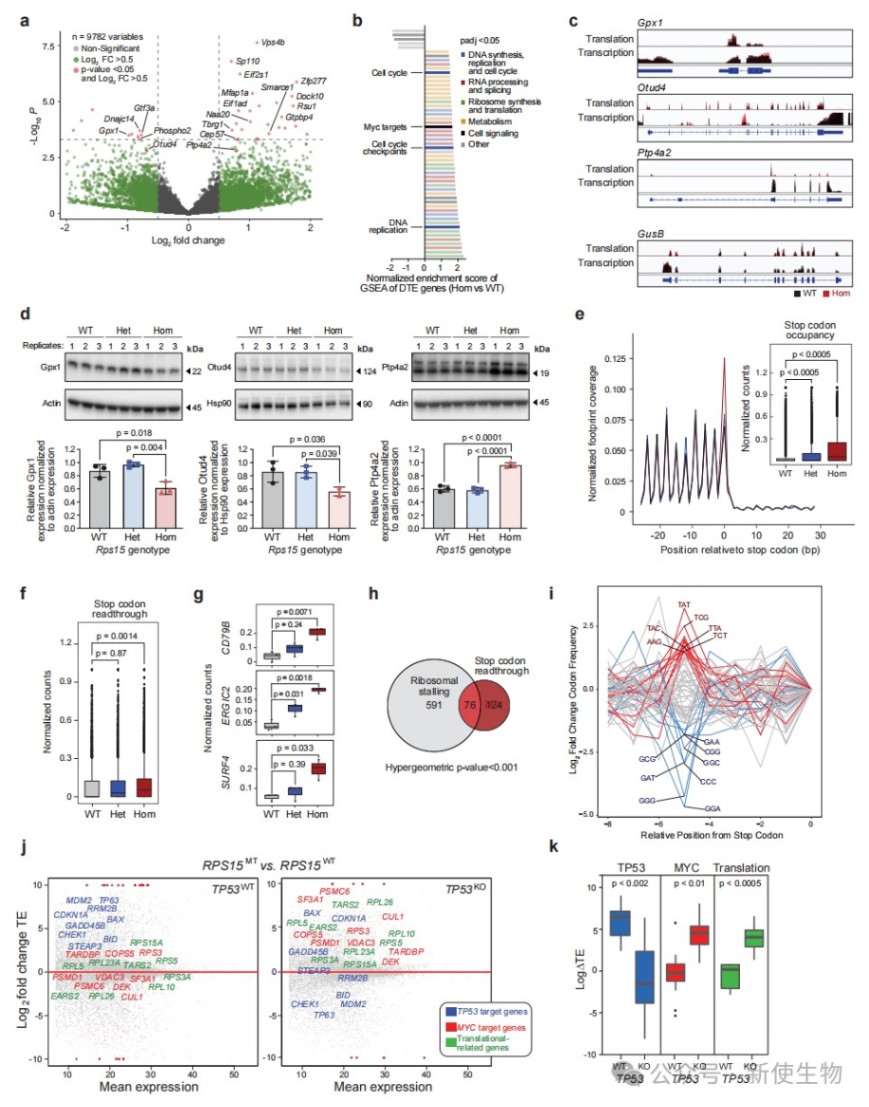
七、突变型核糖体通过改变翻译效率和终止通读驱动转化
此外,研究还观察到显著的核糖体在终止密码子处的停滞以及终止密码子通读现象,直接导致了细胞蛋白组的紊乱。
总结
本研究通过构建首个RPS15突变小鼠模型,系统阐明了该突变驱动B细胞恶性肿瘤的完整分子路径。研究揭示了RPS15突变在致癌过程中的双重作用:它通过扰乱翻译程序引发氧化应激和p53依赖的细胞增殖抑制,但同时造成的基因组不稳定性为后续突变的发生提供了温床,最终推动细胞向不受控制的增殖和癌变演进。
| 新使生物专业翻译组一站式服务平台 |
| 产品名称 |
点击图片查看
点击图片查看


 关于我们
关于我们 产品中心
产品中心 技术服务
技术服务 技术中心
技术中心 联系我们
联系我们